
IDENTIFICATION
Caractéristiques biologiques
Corps court et haut, un peu comprimé latéralement, sa hauteur plus grande que la longueur de la tête; tête très grande, sa hauteur dépassant la moitié de la longueur de la tête; corps couvert de grandes écailles cycloïdes bien visibles, tête dépourvue d’écailles; museau carrément arrondi; yeux grands et visibles de dessous la tête; bouche large et tournée vers le haut avec lèvre inférieure proéminente; lèvre supérieure absente, lèvre inférieure très épaisse; pas de barbeau; lèvre inférieure avec articulation à la symphyse, sans processus proéminent; branchiospines longues et fines; dents pharyngiennes en trois rangées et disposition 5.3.2/2.3.5; nageoire dorsale insérée un peu en avant des nageoires pelviennes, avec 14 à 16 rayons branchus, les rayons simples non osseux; nageoire anale courte; longues nageoires pectorales s’étendant jusqu’aux nageoires pelviennes; nageoire caudale fourchue; ligne latérale avec 40 à 43 écailles. Grisâtre sur le dos et les flancs, argenté-blanc en dessous; nageoires foncées.
Galerie d'images
 |
Catla catla |
PROFIL
Contexte historique
Catla est endémique dans le système fluvial du nord de l’Inde, de la plaine de l’Indus et des collines adjacentes du Pakistan, Bangladesh, Népal et Myanmar. Plus tard il a été introduit dans toute l’Inde, dans presque tous les systèmes fluviaux, les réservoirs et les bassins. Comme l’espèce se reproduit en écosystème fluvial, la grande disponibilité de ses alevins a aidé à en établir l’aquaculture dans ces pays, aux environs du système fluvial. La distribution naturelle de catla semble dépendre de la température plutôt que de la latitude et de la longitude. La température minimum tolérée est d’environ 14 °C. L’utilisation de catla comme composante en pisciculture était une pratique traditionnelle dans les Etats d’Inde orientale, qui ne s’est répandue dans tous les autres Etats indiens qu’au cours de la seconde moitié du 20ème siècle. Son taux de croissance plus élevé et sa compatibilité avec d’autres carpes indiennes, son habitude de se nourrir en surface et la préférence des consommateurs ont augmenté sa popularité en systèmes de polyculture de carpes parmi les pisciculteurs en Inde, Bangladesh, Myanmar, Laos, Pakistan et Thailande. La collecte d’alevins fluviaux était la seule source de culture jusque dans les années 50. Le succès en 1957 de la reproduction induite de l’espèce a ensuite assuré la fourniture d’alevins, révolutionnant ainsi cette forme de polyculture en Inde et dans les autres pays du Sud Est asiatique. L’espèce a aussi été introduite dans d’autres pays, notemment Sri Lanka, Israel, Japon et Maurice. A présent, catla fait partie intégrale des espèces composantes, aussi bien dans la polyculture à trois espèces avec rohu (Labeo rohita) et mrigal (Cirrhinus mrigala), que dans celle à six espèces, qui ajoute la carpe commune (Cyprinus carpio), la carpe herbivore (Ctenopharyngodon idellus) et la carpe argentée (Hypophthalmichthys molitrix) au mélange d’espèces.
Principaux pays producteurs

Principaux pays producteurs de Catla catla (FAO Statistiques des pêches, 2006).
* lao = République démocratique populaire lao |
Habitat et biologie
Catla est une espèce eurythermale qui croit le mieux à des températures situées entre 25 et 32 °C.
Les œufs sont d’abord démersaux et deviennent ensuite graduellement flottant. Les jeunes larves restent dans les eaux de surface et sub-surface et sont fortement phototactiques. Les larves commencent à se nourrir trois jours après leur éclosion, alors que leurs membranes vitellines persistent. Pendant qu’elles grandissent, le nombre de branchiospines et de filaments branchiaux augmentent également, ce qui les aide à filtrer les éléments alimentaires ingérés.
Les petits alevins sont planctonophages, se nourrissant principalement de zooplancton tel que des rotifères et des cladocères. Les adultes se nourrissent en surface et en mi-eau; ils sont aussi planctonophages, avec une préférence pour le zooplancton, principalement crustacés, rotifères, insectes et protozoaires, ainsi qu’une grande partie de matériel végétal, algues et plantes.
Catla atteint la maturité dans sa seconde année, accomplissant alors une migration de reproduction au cours de la saison de la mousson vers les biefs supérieurs des rivières où mâles et femelles se rassemblent et se reproduisent dans les zones marginales peu profondes. La saison de reproduction correspond avec la mousson du sud ouest en Inde nord orientale et au Bangladesh, qui dure de mai à août, et dans le nord de l’Inde et au Pakistan de juin à septembre. Sa fécondité varie généralement de 100 000 à 200 000 oeufs/kg, en fonction de la longueur et du poids du poisson. Les alevins qui en résultent sont apportés par le courant vers les zones en aval où ils sont capturés par les collecteurs d’alevins.
Comme un environnement fluvial est nécessaire, la reproduction naturelle ne survient pas en étang, même si l’espèce y atteint la maturité: l’induction hormonale est donc nécessaire. Des trois carpes indiennes, catla est la plus difficile à reproduire parce qu’elle nécessite des conditions environnementales précises pour se reproduire. En conditions normales, catla atteint 1 à 1,2 kg la première année, comparé respectivement à 700-800 g et 600-700 g pour rohu et mrigal, Elle atteint la maturité sexuelle en deux ans.
Les œufs sont d’abord démersaux et deviennent ensuite graduellement flottant. Les jeunes larves restent dans les eaux de surface et sub-surface et sont fortement phototactiques. Les larves commencent à se nourrir trois jours après leur éclosion, alors que leurs membranes vitellines persistent. Pendant qu’elles grandissent, le nombre de branchiospines et de filaments branchiaux augmentent également, ce qui les aide à filtrer les éléments alimentaires ingérés.
Les petits alevins sont planctonophages, se nourrissant principalement de zooplancton tel que des rotifères et des cladocères. Les adultes se nourrissent en surface et en mi-eau; ils sont aussi planctonophages, avec une préférence pour le zooplancton, principalement crustacés, rotifères, insectes et protozoaires, ainsi qu’une grande partie de matériel végétal, algues et plantes.
Catla atteint la maturité dans sa seconde année, accomplissant alors une migration de reproduction au cours de la saison de la mousson vers les biefs supérieurs des rivières où mâles et femelles se rassemblent et se reproduisent dans les zones marginales peu profondes. La saison de reproduction correspond avec la mousson du sud ouest en Inde nord orientale et au Bangladesh, qui dure de mai à août, et dans le nord de l’Inde et au Pakistan de juin à septembre. Sa fécondité varie généralement de 100 000 à 200 000 oeufs/kg, en fonction de la longueur et du poids du poisson. Les alevins qui en résultent sont apportés par le courant vers les zones en aval où ils sont capturés par les collecteurs d’alevins.
Comme un environnement fluvial est nécessaire, la reproduction naturelle ne survient pas en étang, même si l’espèce y atteint la maturité: l’induction hormonale est donc nécessaire. Des trois carpes indiennes, catla est la plus difficile à reproduire parce qu’elle nécessite des conditions environnementales précises pour se reproduire. En conditions normales, catla atteint 1 à 1,2 kg la première année, comparé respectivement à 700-800 g et 600-700 g pour rohu et mrigal, Elle atteint la maturité sexuelle en deux ans.
PRODUCTION
Ciclo de producci�n
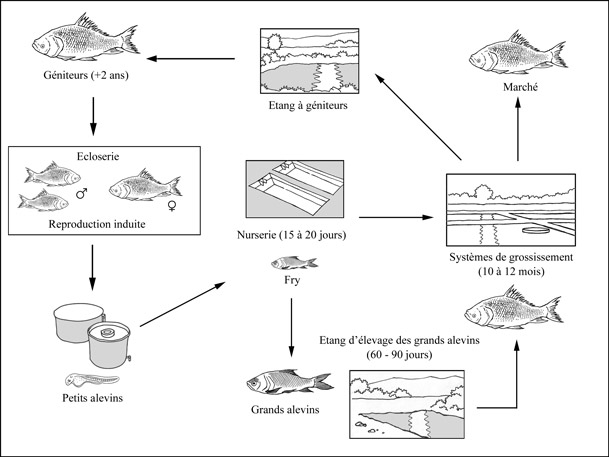 |
Cycle de production de Catla catla |
Systèmes de production
Catla, l’espèce la plus importante après rohu (mrigal est troisième), est utilisé comme composante de nourrissage en surface dans les systèmes de polyculture de carpes indiennes. Dans le système composé de six espèces avec rohu, mrigal, carpe commune, carpe herbivore et carpe argentée, catla partage la niche alimentaire supérieure de l’étang avec la carpe argentée. En Inde dans le système à trois espèces, la proportion de catla est généralement maintenue à 30-35 pour cent, tandis que dans le système à six espèces, il forme 15-20 pour cent. Dans un système commercial de production de carpes à deux espèces pratiqué dans la région du lac Koleru, en Andhra Pradesh, la principale région de production de carpes en Inde, catla constitue 20-30 pour cent du stock total, le reste étant du rohu. Au Bangladesh, bien que les trois carpes indiennes soient les composantes principales dans les systèmes de polyculture, l’on stocke également carpe argentée, carpe herbivore, carpe commune, labeo (Labeo calbasu), tilapia (Oreochromis mossambicus et O. niloticus) et plusieurs carpes mineures. Une autre carpe chinoise, la carpe à grosse tête (Hypophthalmichthys nobilis), est une espèce composante de la polyculture de carpes au Myanmar et au Népal.
Approvisionnement en juvéniles
La reproduction induite de catla a répondu à quasi tous les besoins en alevins de tous les pays où il est cultivé, bien que dans certaines régions, la collecte en rivière soit encore utilisée comme source d’alevins. La stimulation hormonale pour la reproduction induite donne souvent de pauvres résultats pour catla, comparativement aux autres carpes indiennes. Ceci, couplé à une saison de reproduction relativement courte, résulte en une production inadéquate d’alevins d’écloserie, ce qui souvent ne permet pas de répondre entièrement aux besoins des fermiers dans plusieurs régions. Bien que l’extrait pituitaire de carpe ait été l’agent inducteur communément utilisé depuis le développement de la technologie de la reproduction par induction, plusieurs formulations commerciales synthétiques de gonadotropine purifiée de saumon et d’antagonistes de dopamine comme Ovaprim, Ovatide et Wova-FH ont aussi été utilisées avec succès ces récentes années. Lorsque l’extrait pituitaire est utilisé, les femelles sont injectées avec une dose stimulante de 2-3 mg/kg suivie d’une seconde dose de 5 à 8 mg/kg six heures plus tard; les males reçoivent une seule dose de 2-3 mg/kg au moment de la seconde injection de la femelle. Lorsque des formulations synthétiques sont utilisées, une seule dose de 0,4-0,5 ml/kg (femelles) ou 0,2-0,3 ml/kg (males) est administrée.
Bien que différents types de systèmes d’écloserie aient été essayés au cours des années, l’écloserie circulaire chinoise s’est révélée la plus efficiente pour la production à grande échelle d’alevins. Les géniteurs, stockés à 3-5 kg/m3 et dans le rapport poids femelle:male de 1:1 (1:2 en nombre) sont injectés avec l’agent inducteur choisis et relâchés dans le bassin de reproduction dans une profondeur d’eau d’environ 1,5 m. Les œufs fertilisés, collectés 8-12 heures plus tard, sont transférés vers le bassin d’éclosion où ils sont maintenus 64-72 heures pour incubation et éclosion. Le nombre et la grandeur des bassins d’éclosion dans ce type d’écloserie varient, selon les besoins de production et la taille du bassin de reproduction. En général, l’on recouvre 0,10-0,12 million oeufs/kg de géniteur femelle. L’élevage des alevins se fait normalement par un système en deux phases, i.e. une phase de 15-20 jours de nurserie pour élever les petits alevins, suivie par une phase de 2-3 mois pour la production de grands alevins.
Bien que différents types de systèmes d’écloserie aient été essayés au cours des années, l’écloserie circulaire chinoise s’est révélée la plus efficiente pour la production à grande échelle d’alevins. Les géniteurs, stockés à 3-5 kg/m3 et dans le rapport poids femelle:male de 1:1 (1:2 en nombre) sont injectés avec l’agent inducteur choisis et relâchés dans le bassin de reproduction dans une profondeur d’eau d’environ 1,5 m. Les œufs fertilisés, collectés 8-12 heures plus tard, sont transférés vers le bassin d’éclosion où ils sont maintenus 64-72 heures pour incubation et éclosion. Le nombre et la grandeur des bassins d’éclosion dans ce type d’écloserie varient, selon les besoins de production et la taille du bassin de reproduction. En général, l’on recouvre 0,10-0,12 million oeufs/kg de géniteur femelle. L’élevage des alevins se fait normalement par un système en deux phases, i.e. une phase de 15-20 jours de nurserie pour élever les petits alevins, suivie par une phase de 2-3 mois pour la production de grands alevins.
Nurserie
Les larves agées de trois jours, mesurant environ 6 mm, sont élevées pour 15-20 jours dans de petits étangs de nurserie en terre de 0,02-0,1 ha, pour atteindre la taille de 20-25 mm. Dans certaines régions, des bassins en briques ou en ciment sont aussi utilisés comme nurseries. Là où seul catla est stocké, les étangs de terresont stockés à la densité de 3-10 millions/ha et les bassins en ciment à la densité de 10-20 millions/ha. Dans beaucoup de cas cependant, les fermiers stockent plusieurs espèces de carpes, n’ayant pas assez d’étangs pour les stocker séparemment. La préparation d’un étang de nurserie avant son empoissonnement comprend l’enlèvement des plantes aquatiques et des poissons prédateurs, suivi d’un chaulage et d’une fertilisation avec de la fumure organique et des engrais inorganiques. L’application d’une émulsion savon-huile ou la filtration répétée de l’eau avec un filet est utilisée pour éradiquer les insectes aquatiques avant de stocker. Un mélange poudreux de son de riz et de tourteaux est l’aliment supplémentaire communément distribué. Les taux de survie varient normalement entre 30 et 40 pour cent; cependant, cette survie reste souvent faible dû à une mauvaise gestion. En l’absence d’aliments commerciaux, les fermiers sont obligés de recourir au mélange traditionnel son-tourteau ce qui limite la croissance et la survie des alevins. La survie de catla en étangs de nurserie est normalement plus faible que celle de rohu et de mrigal.
Elevage de fingerlings
Les alevins de 20-25 mm produits en nurserie sont encore élevés pour 2-3 mois jusqu’à la taille de 80-100 mm (6-10 g) grands alevins en étangs de terre de 0,05-0,2 ha. Les alevins de catla sont élevés ensembles avec rohu and mrigal en égales proportions, à la densité combinée de 0,2-0,3 million alevins/ha. La fertilisation de l’étang avec des engrais organiques et inorganiques, et l’alimentation supplémentaire avec le mélange conventionnel de son de riz et de tourteau sont la norme ; cependant, dosage et forme d’application varient selon l’intensité de l’élevage et la productivité inhérente de l’étang. Dans ces systèmes d’élevage de grands alevins, la survie varie de 60 à 70 pour cent.
Techniques de grossissement
Etant un poisson qui se nourrit en surface et qui est fortement préféré des consommateurs, catla est une composante intégrale des systèmes de polyculture de carpes dans tous les pays où il est cultivé, y compris Inde, Bangladesh, Pakistan, Népal, Laos et Myanmar. Des trois carpes indiennes, c’est l’espèce qui croit la plus rapidement. Pour le grossissement dans le système de polyculture de carpes, les pratiques standardisées incluent: le contrôle des poissons prédateurs et des poissons sans valeur par l’application de produits chimiques ou d’extraits de plantes; l’empoissonnement de grands alevins à la densité combinée de 4 000-10 000 ind/ha; la fertilisation de l’étang avec des fumures organiques telles que fumier de bétail ou fientes de volaille et des engrais inorganiques; alimentation supplémentaire avec un mélange de son de riz/blé et de tourteau; et le monitoring de la santé des poissons et la gestion de l’eau. Le niveau d’adoption de ces pratiques varie de pays à pays, en fonction principalement de la disponibilité de ressources et de la situation économique des pisciculteurs. Normalement, la période de grossissemnt est de un an, au cours duquel il grandit jusqu’à environ 1 kg. Dans la région du Lac Koleru de l’Andhra Pradesh, le centre de la pisciculture commerciale en Inde avec plus de 100 000 ha d’eau en production, la période de grossissement s’étend jusqu’à 18 mois. Dans cette région, ce sont des alevins «stunted» (i.e. de grands alevins élevés sous de fortes densités pour un an et pesant 150-300 g) qui sont mis en charge et le poids moyen des catla récoltés est de 1,5-2,0 kg. Les niveaux de production réalisés dans les systèmes de polyculture de carpes restent en général à 3-5 tonnes/ha/an, avec catla contribuant environ 20-30 pour cent de la biomase.
Les alevins fournis par la plupart des écloseries/nurseries de carpes pour le grossissement consistent en un mélange d’espèces, souvent avec une très faible proportion de catla; ceci est dû à la faible réponse à la reproduction et à la comparativement mauvaise survie en nurserie de catla. Une mauvaise ou non disponibilité de suffisamment grands alevins est un autre facteur limitant important qui oblige les fermiers à stocker de petits alevins, ce qui résulte souvent en une faible survie. Le coût élevé d’aliments commerciaux et des ingrédients alimentaires empêchent parfois les fermiers de nourrir convenablement, ce qui limite aussi la production.
Catla est aussi une composante importante du système de carpiculture en eaux usées qui se pratique sur plus de 4 000 ha en Bengal occidental, Inde. Dans cette forme de pisciculture, qui se caractérise par de multiples empoissonnements et de multiples récoltes de poissons de 300 g, des eaux usées de premier traitement sont déversées dans les étangs comme intrant principal. Même sans l’apport d’aliments suppplémentaires, ce système produit 2-3 tonnes/ha/an; avec l’apport d’aliments, ceci peut être augmenté jusqu’à 4-5 tonnes/ha/an.
Les alevins fournis par la plupart des écloseries/nurseries de carpes pour le grossissement consistent en un mélange d’espèces, souvent avec une très faible proportion de catla; ceci est dû à la faible réponse à la reproduction et à la comparativement mauvaise survie en nurserie de catla. Une mauvaise ou non disponibilité de suffisamment grands alevins est un autre facteur limitant important qui oblige les fermiers à stocker de petits alevins, ce qui résulte souvent en une faible survie. Le coût élevé d’aliments commerciaux et des ingrédients alimentaires empêchent parfois les fermiers de nourrir convenablement, ce qui limite aussi la production.
Catla est aussi une composante importante du système de carpiculture en eaux usées qui se pratique sur plus de 4 000 ha en Bengal occidental, Inde. Dans cette forme de pisciculture, qui se caractérise par de multiples empoissonnements et de multiples récoltes de poissons de 300 g, des eaux usées de premier traitement sont déversées dans les étangs comme intrant principal. Même sans l’apport d’aliments suppplémentaires, ce système produit 2-3 tonnes/ha/an; avec l’apport d’aliments, ceci peut être augmenté jusqu’à 4-5 tonnes/ha/an.
Techniques de récolte
Les consommateurs préfèrent généralement que catla soit grand 1-2 kg. Les fermiers ne récoltent donc cette espèce qu’à la fin de la période d’élevage plutôt qu’au moment des récoltes intermédiaires. Dans les plans d’eau où l’on pratique de multiples empoissonnements et de multiples récoltes, la récolte de plus grands individus (plus de 500 g) est généralement initié après 6-7 mois de culture, tandis les individus trop petits sont remis dans l’étang pour y continuer à grandir. Des filets traînants opérés à la main sont l’engin de pêche le plus utilisé pour récolter les carpes. Les poissons ayant atteint la taille commerciale sont généralement récoltés par multiple opération du filet. L’épervier est un autre engin de pêche fréquemment utilisé pour la récolte partielle de poissons dans les petits étangs et dans les étangs d’arrière cour.
Manipulation et traitement
Catla est commercialisé surtout sur les marchés locaux, où il est vendu frais. La commercialisation de cette espèce dépend principalement des marchés domestiques, où elle est vendue à l’état frais. Dans les grandes fermes commerciales où la récolte est considérable, les poissons, après être bien nettoyés dans de l’eau, sont emballés avec de la glace pilée (proportion 1:1) dans des caisses rectangulaires en plastique (généralement 60 cm x 40 cm x 23 cm). Le transport sur de longues distances de ces poissons sous glace en camionnettes calorifugées se fait couramment dans des pays comme l’Inde où catla est même transportée sur plus de 3 000 km par route vers des régions manquant de poisson. La transformation après récolte et l’ajoute de valeur pour cette espèce sont quasi inexistentes à présent dans les pays producteurs.
Coûts de production
En général, la carpe est une espèce de faible valeur se vendant sur le marché pour moins de 1 USD/kg au niveau du producteur; l’utilisation de gros intrants comme alevins, engrais et aliment supplémentaire, en plus de la main d’œuvre, est donc maintenue au minimum. L’alimentation supplémentaire constitue plus de 50 pour cent du coût total des intrants en polyculture de carpes; une bonne gestion de l’alimentation est donc particulièrement importante pour augmenter les bénéfices. En systèmes extensifs, avec une production de 2-3 tonnes/ha, le coût de production est d’environ 0,30 USD/kg, tandis que les coûts augmentent à 0,5-0,6 USD/kg en élevage semi intensif, où l’on s’attend à une production de 4-8 tonnes/ha.
Maladies et mesures de contrôle
Dans certains cas, des antibiotiques et d’autres produits pharmaceutiques ont été utilisés pour traitement mais leur inclusion dans cette table ne signifie pas une recommandation de la FAO.
Fournisseurs d’expertise en pathologie
L'assistance peut être fournie par les sources suivantes:
| MALADIE | AGENT | TYPE | SYNDROME | MEASURES |
| Maladie des yeux | Aeromonas liquefaciens | Bactérie | Yeux, nerfs optiques et cerveau affectés; cornée de l’oeil vascularisée & devient opaque; ensuite globe de l’œil se putréfie conduisant à la mort | Traiter étangs affectés avec 0,1 ppm KMnO4, suivi de 300 ppm chaux vive |
| Ulcère | Aeromonas spp.; Pseudomonas spp. | Bactéries | Ulcérations; exophthalmie; distension abdominale | Détruire poissons fort affectés; désinfecter étangs affectés avec 0,5 ppm solution de KMnO4; ajouter sulphadiazine (100 mg/kg) ou terramycine (75-80 mg/kg) à la nourriture pendant 10-12 jours |
| Columnariose | Flavobacterium columnaris | Bactérie | Plaques blanches surélevées, souvent avec zone périphérique rougeâtre devenant des tâches hémorragiques sur le corps | Traitement par bain dans solution 500 ppm KMnO4 |
| Œdème | Aeromonas sp. | Bactérie | Ecailles du corps se tendent comme sur cône de pin; inflammation; ulcération; exophtalmie; distension abdominale | Désinfecter étangs affectés avec 1 ppm KMnO4; bains dans 5 ppm KMnO4 pour 2 minutes |
| Saprolégniose | Saprolegnia parasitica | Champignon | Des moisissures se développent sur le corps comme du coton, pénétrant dans le muscle; pourriture morbide du muscle | Bain dans 3-4% NaCl; bain dans KMnO4 160 mg/litre pour 5 jours; bain dans vert de malachite 1-2 mg/litre pendant 30 minutes à 1 heure; ajouter du formol pour atteindre 20 ml/litre dans étangs affectés |
| Branchiomycose (pourriture des branchies) | Branchiomyces demigrans | Champignon | Champignon se développe dans vaisseaux sanguins des branchies et cause nécrose des tissus environnant; décoloration brun-jaunâtre et désintégration des tissus branchiaux | Addition de chaux vive (50-100 kg/ha) aux étangs affectés; si faibles infections, bain dans 3-5% NaCl pour 5-10 minutes, ou dans 5 ppm KMnO4 pour 5-10 minutes |
| Ichtyophthiriase | Ichthyophthirius multifilis | Parasite (protozoaire) | Peau, rayons des nageoires & opercules couverts de spores blanches; poissons malades se frottent à des substrats durs | Bain dans solution 1:5 000 formol pendant 1 heure pour 7-10 jours ou dans 2% NaCl pour 7-10 jours; désinfecter étangs affectés avec chaux vive à 200 kg/ha |
| Trichodiniase | Trichodina reticulata; T. negre | Parasite (protozoaire) | Invasion de parasites dans la peau et dans la région des branchies | Bain dans 2-3 % NaCl pour 5-10 minutes ou dans 4 ppm KMnO4 pour 5-10 minutes; traiter étangs affectés avec 25 ppm formol |
| Points blancs des branchies | Thenohanellus catlae; Myxobolus bengalensis; M. catlae; M. hosadurgensis | Parasite (protozoaire) | Faiblesse; amaigrissement; soulèvement des écailles le long bords postérieurs; perte d’écailles; perforation des écailles; perte de chromatophores | Réduire densité d’empoissonnement; ajouter levure à la nourriture (1 g/kg); bain dans 2-3 % NaCl |
| Dactylogyrose et gyrodactylose | Dactylogyrus spp.; Gyrodactylus spp. | Parasites (trématodes monogénéens) | Branchies, nageoires et peau affectées; sécrétion excessive de mucus | Bain dans 3-5 % NaCl pour 5-10 minutes; bain dans 100 ppm formol; traiter étangs affectés avec 25 ppm formol ou 4 ppm KMnO4 |
| Points noirs ou diplostomiase | Diplostomum pigmentata | Parasites (trématodes digénéens) | Nodules noirs de cystes avec métacercaires dans le corps; infecte aussi les yeux et cause la cécité | Eliminer la population de mollusques présente dans l’étang |
| Argulose | Argulus sp. | Parasite (crustacé) | Parasites visibles à l’œil nu, attachés à la tête & aux nageoires; tâches hémorragiques présentes dans cas chroniques | Si infection sévère, drainer et assécher les étangs; court bain dans 5 ppm KMnO4; traiter au 'Butox' trois fois à 35 ml/ha-m à une semaine intervalle |
| Syndrome ulcératif épizootique | Aeromonas hydrophila; A. sorbia; Aphanomyces invadans | Bactéries et champignons | Grands ulcères rouges ou gris, peu profonds avec zones nécrotiques sur la peau; champignon s’étend profondément sous la peau dans la musculature; lésions de dermatite aigue et ulcères | 200 kg/ha de chaux vive ou 0,1 ppm CIFAX (formulation CIFA, Inde) |
Fournisseurs d’expertise en pathologie
L'assistance peut être fournie par les sources suivantes:
- Central Institute of Freshwater Aquaculture (CIFA), Inde.
- Central Institute of Fisheries Education, Mumbai, Inde.
- College of Fisheries, Mangalore, Inde.
STATISTIQUES
Statistiques de production
Production globale d’aquaculture de Catla catla
(FAO Statistiques des pêches) 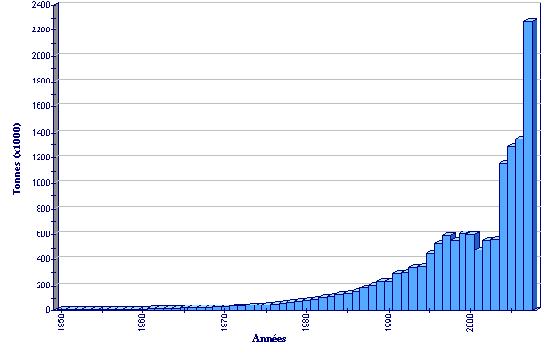 |
Marché et commercialisation
Catla se vend surtout dans les marchés locaux où il est généralement vendu à l’état frais. Il est aussi souvent transporté sous glace vers de proches marchés urbains. Les poissons sont aussi transportés mélangés à de la glace par camionettes calorifugées vers des régions privées de poisson, distantes parfois jusqu’à 2 000-3 000 km du lieu de production. L’on préfère les poissons de petite taille de 1-2 kg parce que le goût diminue quand ils deviennent plus grands. Catla et rohu se vendent à des prix similaires, qui sont généralement 10-20 pour cent plus élevés que pour mrigal. Des poissons frais produits localement se vendent à un prix environ une et demi fois plus élevé que le poisson sous glace. Le prix du poisson vivant est deux fois celui du poisson glacé. Il n’y a pratiquement pas de réglementation ni de contrôle du gouvernement sur les marchés domestiques pour ces produits aquacoles; le prix est donc influencé avant tout par l’offre et la demande. Excepté pour la congélation par glace pour le transport, la transformation après récolte est pratiquement inexistente.
SITUATION ET TENDANCES
Plusieurs facteurs ont amélioré le statut de l’élevage des carpes indiennes:
D’autres facteurs ont causé des problèmes. L’adoption de pratiques intensives d’élevage, l’utilisation non contrôlée d’intrants et le manque de connaissances scientifiques chez les fermiers ont résulté en une augmentation de l’incidence des maladies. Cependant, une confiance continue en la gestion sanitaire a permis le développement de thérapies et aidé le secteur à se remettre de telles situations.
L’Inde a déjà établi un plan stratégique pour doubler la production de l’aquaculture d’eau douce par des augmentations de productivité et de surface. Comme catla est une composante importante du système de polyculture de carpes, il faut s’attendre à ce qu’il y aura une forte augmentation de sa production en Inde d’ici 2015. L’on s’attend également à ce que le Bangladesh augmente aussi sa production de catla aquacoles. Le grand potentiel de croissance des carpes indiennes a attiré l’attention de plusieurs pays tropicaux du Sud Est asiatique et du Moyen Orient.
L’on s’attend à ce que d’autres facteurs influencent la croissance de l’aquaculture des carpes indiennes, y compris:
- Améliorations dans la reproduction induite et la production d’alevins qui ont enlevé la dépendance de la capture d’alevins sauvages en rivières.
- Amélioration de la technologie de grossissement.
- Améliorations dans l’alimentation et la gestion sanitaire.
D’autres facteurs ont causé des problèmes. L’adoption de pratiques intensives d’élevage, l’utilisation non contrôlée d’intrants et le manque de connaissances scientifiques chez les fermiers ont résulté en une augmentation de l’incidence des maladies. Cependant, une confiance continue en la gestion sanitaire a permis le développement de thérapies et aidé le secteur à se remettre de telles situations.
L’Inde a déjà établi un plan stratégique pour doubler la production de l’aquaculture d’eau douce par des augmentations de productivité et de surface. Comme catla est une composante importante du système de polyculture de carpes, il faut s’attendre à ce qu’il y aura une forte augmentation de sa production en Inde d’ici 2015. L’on s’attend également à ce que le Bangladesh augmente aussi sa production de catla aquacoles. Le grand potentiel de croissance des carpes indiennes a attiré l’attention de plusieurs pays tropicaux du Sud Est asiatique et du Moyen Orient.
L’on s’attend à ce que d’autres facteurs influencent la croissance de l’aquaculture des carpes indiennes, y compris:
- La reproduction sélective.
- La pisciculture organique.
- L’exportation vers les pays du Sud Est asiatique et du Moyen Orient.
- Le développement de produits de transformation et à valeur ajoutée.
PROBLÈMES ET CONTRAINTES MAJEURS
Les carpes sont généralement élevées en un système fermé qui comprend des espèces herbivores, dans lequel des matériaux organiques sont utilisés comme sources principales d’intrants, ce qui en fait une pratique généralement considérée comme amie de l’environnement. De plus, la compatibilité de catla en systèmes de polyculture avec la préférence de l’habitat et les habitudes alimentaires est bonne. Cependant, la tendance des fermiers d’augmenter leur revenus par unité de surface a résulté en une utilisation excessive d’engrais, d’aliments protéinés et de produits chimiques qui peuvent être nuisibles à l’environnement. La compatibilité de catla en systèmes de polyculture avec les autres carpes a déjà été établie. Cependant, une faible reproduction de catla a été observée dans plusieurs régions; ceci, combiné à la faible survie de cette espèce au cours des stades de nurserie comparé à rohu et à mrigal, a parfois résulté en des manques d’alevins.
Pratiques pour une aquaculture responsable
Etant un système basé sur peu d’intrants, la carpiculture n’a, en général, pas été considérée comme présentant un danger pour l’environnement. Cependant, l’importance accrue donnée ces dernières années à l’intensification afin d’augmenter la production a résulté en une utilisation accrue d’engrais chimiques, d’aliments, de produits thérapeutiques, de médicaments, de produits chimiques, etc., ce qui devient inqiétant. Il est donc nécessaire que les pays concernés formulent des directives et imposent de strictes mesures en vue de l’utilisation judicieuse de ces intrants critiques. L’application des principes de l’Article 9 du Code de Conduite pour des Pêches Responsables de la FAO serait approprié.
RÉFÉRENCES
Bibliographie
| Ayyappan, S. & Jena, J.N. 2001. Sustainable freshwater aquaculture in India.In: T. J. Pandian (ed.), Sustainable Indian Fisheries, pp. 83-133. National Academy of Agricultural Sciences, New Delhi, India. |
| Ayyappan, S. & Jena, J.K. 2003. Grow-out production of carps in India. Journal of Applied Aquaculture, 13:251-282. |
| Basavaraju, Y. & Varghese, T.J. 1980. A comparative study of growth rate of rohu - mrigal and mrigal - rohu hybrids and their parental species. Mysore Journal of Agricultural Sciences, 14(3):388-395. |
| Choudhury, S.N. 1995. Shrimp and carp aquaculture and the environment.In: Bangladesh Study Report. Regional Study and Workshop on Aquaculture Sustainability and the Environment. Manila, Asian Development Bank & Bangkok, Network of Aquaculture Centres in Asia-Pacific. [Draft report] |
| CIFA. 2004. Annual Report Central Institute of Freshwater Aquaculture. Bhubaneswar.CIFA. 99 pp. |
| Gopakumar, K., Ayyappan, S., Jena, J.K., Sahoo, S.K., Sarkar, S.K., Satapathy, B.B. & Nayak, P.K. 1999. National Freshwater Aquaculture Development Plan.CIFA, Bhubaneswar, India, 75 pp. |
| Gupta, S.D., Rath, S.C., Dasgupta, S.D. & Tripathi, S.D. 1995. A first report on quadruple spawning of Catla catla (Ham.). Veterinarski Arhiv, 65(5):143-148. |
| Hayat, M. 1995. Shrimp and carp aquaculture and the environment. Pakistan Study Report. In: Regional Study and Workshop on Aquaculture Sustainability and the Environment. Manila, Asian Development Bank and Bangkok, Network of Aquaculture Centres in Asia-Pacific. [Draft report] |
| Jayaram, K.C. 1981. The Freshwater Fishes of India, Pakistan, Bangladesh, Burma and Sri Lanka. Handbook of Zoological Survey of India, Volume 2. Calcutta, India. 475 pp. |
| Jena, J.K., Aravindakshan, P.K., Chandra, S., Muduli, H.K. & Ayyappan, S. 1998a. Comparative evaluation of growth and survival of Indian major carps and exotic carps in raising fingerlings. Journal of Aquaculture in the Tropics, 13:143-150. |
| Jena, J.K., Aravindakshan, P.K. & Singh, W.J. 1998b. Nursery rearing of Indian major carp fry under different stocking densities. Indian Journal of Fisheries, 45(2): 163-168. |
| Jhingran, V.G. 1968. Synopsis of Biological Data on Rohu, Cirrhinus mrigala (Hamilton, 1822). FAO Fisheries Synopsis No. 32, FAO, Rome, Italy. |
| Jhingran, V.G. 1991. Fish and Fisheries of India. Hindustan Publishing Corporation (India), Delhi, India. 727 pp. |
| Khoke, U.C. 1995. Shrimp and carp aquaculture and the environment. Myanmar Study Report. In: Regional Study and Workshop on Aquaculture sustainability and the Environment. Manila, Asian Development Bank & Bangkok, Network of Aquaculture Centres in Asia-Pacific. [Draft report] |
| Pathak, S.C. & Palanisamy, K. 1995. Shrimp and carp aquaculture and the environment. India Study Report. In: Regional Study and Workshop on Aquaculture sustainability and the Environment. Manila, Asian Development Bank & Bangkok, Network of Aquaculture Centres in Asia-Pacific. [Draft report] |
| Singh, D.M. 1995. Shrimp and carp aquaculture and the environment. Nepal Study Report. In: Regional Study and Workshop on Aquaculture sustainability and the Environment. Manila, Asian Development Bank & Bangkok, Network of Aquaculture Centres in Asia-Pacific. [Draft report] |
| Somalingam, J., Maheshwari, U.K. & Langer, R.K. 1990. Mass production of intergeneric hybrid catla (Catla catla x Labeo rohita) and its growth in ponds, small and large reservoirs of Madhya Pradesh. In: P. Keshavanath & K.V. Radhakrishnan (eds.), Proceedings of the workshop on carp seed production technology, pp. 49-52. Asian Fishery Society Indian Branch, Mangalore, India. |
| Talwar, P.K. & Jhingran, A.G. 1991. Inland Fishes of India and Adjacent Countries. Volume 1. Oxford and IBH Publishing Co. Pvt. Ltd., New Delhi, India. 541 pp. |

