As biotoxinas marinhas são responsáveis por um número substancial de doenças relacionadas com o pescado. As toxinas conhecidas estão indicadas no Quadro 3.7.
As toxinas e as doenças que elas podem provocar têm sido descritas em vários artigos de revisão da autoria de Taylor (1988), Hall (1991), WHO (1984a, 1989) e Todd (1993) os quais podem ser consultados para uma informação mais pormenorizada. Alguns dos aspectos mais importantes vão ser discutidos a seguir.
Contrariamente a todas as outras biotoxinas que se acumulam no peixe vivo ou marisco, a tetrodotoxina não é produzida por algas. O mecanismo preciso envolvido na produção desta tão potente toxina não está claro, mas, aparentemente e com frequência, estão envolvidas bactérias simbióticas (Noguchi et al., 1987; Matsui et al., 1989).
A tetrodotoxina encontra-se, principalmente, no figado, ovas e intestinos de várias espécies de baiacu, pertencendo os membros mais tóxicos à família Tetraodontidae, mas nem todas as espécies desta família contêm a toxina. O tecido muscular do peixe tóxico não tem, normalmente, esta toxina, mas há excepções. O envenenmento por baiacu causa sintomas neurológicos 10–45 minutos após a ingestão. Os sintomas são a sensação de formigueiro na face e extremidades, paralisia, sintomas respiratórios e colapso cardiovascular. Em casos fatais, a morte ocorre em 6 horas.
| Toxina | Quando e onde é produzida | Animal(ais)/órgão envolvido |
|---|---|---|
| Tetrodotoxina | no peixe ante mortem | Baiacu (Tetraodontidae) principalmente nas ovas, figado e intestinos |
| Ciguatera | Algas marinhas | >400 espécies de peixes tropicais e subtropicais |
| Toxinas paralisantes (PSP) | Algas marinhas | Bivalves filtradores, principalmente na glândula digestiva e nas gónadas |
| Toxinas diarreicas (DSP) | Algas marinhas | Bivalves filtradores |
| Neurotoxinas(NSP) | Algas marinhas | Bivalves filtradores |
| Toxinas amnésicas (ASP) | Algas marinhas | Bivalves filtradores (mexilhões) |
O envenenamento com ciguatera resulta da ingestão de peixe que ficou tóxico devido à ingestão de dinoflagelados tóxicos que são algas marinhas planctónicas microscópicas. A fonte principal é o dinoflagelado bentónico Gambierdiscus toxicus, que vive junto dos recifes corais estreitamente ligado a macroalgas. Observa-se um aumento da produção de dinoflagelados tóxicos quando os recifes são perturbados (furacões, destruiçãa ou quentes, têm etc.). Mais de 400 espécies de peixes; todos provenientes de águas tropicais ou quentes, têm sido referidas como tendo causado ciguatera, tal como representado na figura 3.3 (Halstead, 1978). A toxina acumula-se nos peixes que se alimentam de algas tóxicas ou em peixes carnívoros de maiores dimensões que se alimentam destes herbívoros. A toxina pode ser detectada no intestino, no figado ou no tecido muscular através de ensaios com ratos e por cromatografia. Alguns peixes podem ser capazes de eliminar a toxina acumulada (Taylor, 1988).
Embora a incidência referida para o envenenamento com ciguatera seja baixa (Taylor, 1988), tem sido estimado que a incidência a nível mundial pode ser da ordem de 50 000 casos por ano (Ragelis, 1984). O quadro clínico varia, mas o tempo de aparecimento dos sintomas é apenas de algumas horas após a ingestão da toxina. Os sistemas gastrointestinal e neurológico são afectados (vómitos, diarreia, sensação de formigueiro, ataxia, fraqueza). A duração da doença pode ser de dois a três dias, mas pode persistir durante semanas ou mesmo anos em casos críticos. A morte resulta de colapso circulatório. Halsted (1978) indicou uma taxa de casos fatais de cerca de 12%.
A intoxicação após o consumo de bivalves é um síndroma que é conhecido há séculos, sendo o mais comum designado por intoxicação por toxinas paralisantes de bivalves (PSP). Este é causado por um grupo de toxinas (saxitoxinas e derivados) produzidas por dinoflagelados do género Alexandrium, Gymnodinium e Pyrodinium.
Historicamente, a PSP tem sido associada ao afloramento de dinoflagelados (>106 células/litro), que podem causar uma colorção avermelhada ou amarelada da água. Contudo, a coloração da água pode ser causada pela proliferação de muitos tipos de espécies planctónicas que nem sempre são tóxicas e nem todos os afloramentos de algas tóxicas apresentam cor.
O afloramento de dinoflagelados depende da temperatura da água, da luz, da salinidade, da presença de nutrientes e de outras condições ambientais. Todavia, a natureza precisa dos factores que provocam o aparecimento de um clone tóxico édesconhecida. A temperatura da água deve ser superior a 5 – 8°C para que ocorram os afloramentos. Se as temperaturas forem inferiores a 4°C, os dinoflagelados podem sobreviver sob a forma de cistos enterrados nas camadas superiores dos sedimentos. A ocorrência mundial de PSP está representada na figura 3.3.

Figura 3.3. Distribuição mundial de surtos de intoxicações por toxinas paralisantes de bivalves (pontos pretos) e de ciguatera (zona sombreada). Dados da WHO (1984a), Halstead e Schantz (1984) e Lupin (1992).
Os mexilhões, as amêijoas, os berbigões e as vieiras que se alimentaram de dinoflagelados tóxicos retêm a toxina durante períodos variáveis que dependem da espécie. Alguns eliminam a toxina muito rapidamente e são tóxicos apenas durante o afloramento, enquanto que outros retêm a toxina durante um longo período, mesmo durante anos (Schantz, 1984).
A PSP provoca uma desordem neurológica cujos sintomas incluem formigueiro, sensação de calor e dormência dos lábios e da ponta dos dedos, ataxia, sonolência e discurso incoerente. Em casos críticos ocorre a morte devido a paralisia respiratória. Os sintomas desenvolvem-se entre 0,5 a 2 horas após uma refeição e, em geral, as ví timas que sobrevivem mais de 12 horas recuperam.
Milhares de casos de desordens gastrointestinais causadas por intoxicações por toxinas diarreicas de bivalves (DSP) têm sido registados na Europa, no Japão e no Chile (WHO, 1984a). Os dinoflagelados envolvidos que produzem as toxinas pertencem ao géero Dinophysis e Aurocentrum. Estes dinoflagelados encontram-se largamente espalhados o que significa que esta doença pode também ocorrer noutras partes do mundo. Foram identificadas pelo menos 7 toxinas, incluindo o ácido okadaico. O aparecimento da doença ocorre desde meia hora até algumas horas após o consumo do bivalve que se tenha alimentado com as algas tóxicas. Os sintomas são desordens gastrointestinais (diarreia, vómitos, dores abdominais) e as vítimas recuperam após 3 – 4 dias. Nunca foram registados casos fatais.
As intoxicações por neurotoxinas de bivalves (NSP) têm sido descritas em pessoas que consumiram bivalves expostos a “marés vermelhas” de dinoflagelados (Ptychodiscus breve). A doença tem estado limitada ao Golfo do México e às áreas da costa da Florida. As brevetoxinas são altamente letais para o peixe e as marés vermelhas deste dinoflagelado estão também associadas à morte massiva de peixes.
Os sintomas de NSP assemelham-se aos da PSP excepto no facto de não ocorrer a paralisia. A NSP é raramente fatal.
A intoxicação por toxinas amnésicas de bivalves (ASP) sófoi identificada recentemente (Todd, 1990; Addison e Stewart, 1989). A intoxicação é devida ao ácido domóico, um aminoácido produzido pela diatomácea Nitzschia pungens. A primeira incidência verificada de ASP ocorreu durante o Inverno de 1987/88 na parte leste do Canadá onde mais de 150 pessoas foram afectadas e ocorreram 4 mortes após o consumo de mexilhões de cultura.
Os sintomas de ASP variam grandemente desde uma náusea ligeira, vómitos, até à perda de equilíbrio e deficiências no sistema nervoso central que incluem confusão e perda de memória. As breves ausências de memória parecem ser permanentes nas vítimas sobreviventes, sendo esta a origem da designação de intoxicação por toxinas amnésicas.
O controlo das biotoxinas marinhas é dificil e a doença não pode ser inteiramente prevenida. As toxinas são todas de natureza não proteica e extremamente estáveis (Gill et al., 1985). Assim, a cozedura, a fumagem, a secagem e a salga não as destroi e não se pode dizer, com base no aspecto do peixe ou da carne do marisco, se este é ou não tóxico.
A principal medida de prevenção é a inspecção e a amostragem das áreas de pesca e dos bancos de bivalves para análise das toxinas. O bioensaio com ratos é usado muitas vezes com este objectivo e a confirmação por HPLC é efectuada se ocorrer a morte após 15 min. A apanha é interditada se forem encontrados elevados níveis de toxinas. Parece improvável que seja sempre possível controlar a composição do fitoplâncton nas áreas de crescimento por eliminação das espécies toxinogénicas, não havendo um método de confiança para prever quando uma espécie particular de fitoplâncton se desenvolve e, por conseguinte, não há maneira de prever um afloramento de espécies toxinogénicas (Hall, 1991).
A eliminação da toxina por técnicas de depuração pode apresentar algumas potencialidades, mas o processo é muito lento e caro. Há também o risco de um pequeno número de indivíduos não abrir as valvas e não filtrar a água limpa através do sistema e de reter, por conseguinte, o seu nível original de toxicidade (Hall, 1991).
A vigilância, para ser eficiente, exige planos de amostragem de confiança e meios eficientes de detecção das toxinas. Os métodos químicos de confiança para a detecção de todas as toxinas estão actualmente disponíveis e devem ser aplicados. O plano de amostragem deve ter em consideração que a toxicidade dos bivalves pode aumentar desde níveis desprezáveis até níveis letais em menos de uma semana ou até em menos de 24 horas no caso de mexilhões. A toxicidade pode variar também com o local de crescimento dos bivalves de acordo com a geografia, as correntes e a actividade das marés.
A situação actual, no que diz respeito a tolerâncias e métodos de análise a serem utilizados num programa de vigilância, está apresentada no Quadro 3.8.
| Toxina | Tolerância | Método de análise |
|---|---|---|
| Ciguatera | Controlo não possível | Não há método de confiança |
| PSP | 80 μg/100g | Bioensaio com ratos, HPLC |
| DSP | 0–60 μg/100g | Bioensaio com ratos, HPLC |
| NSP | Qualquer nível detectado/100g é perigoso | Bioensaio com ratos. Não há nenhum método químico |
| ASP | 20 μg de ácido domoico/g | HPLC |
O envenenamento por histamina é uma intoxicação química resultante da ingestão de produtos alimentares que contenham níveis elevados de histamina. Este envenenamento foi designado, historicamente, por envenenamento por escombroides devido à sua frequente associação com peixes, principalmente, o atum e a cavala.
O envenenamento por histamina é um problema a nível mundial e ocorre em países onde se consome peixe, contendo altos níveis de histamina. É uma doença de carácter benigno; o período de incubação é muito curto (desde alguns minutos até algumas horas) e a duração da doença é curta (algumas horas). Os sintomas mais comuns são cutâneos tais como ruborização facial, urticária, edema, mas o tracto gastrointestinal pode ser também afectado (náuseas, vómitos, diarreia) bem como a nível neurológico (dores de cabeça, formigueiro, sensação de queimadura na boca).
A histamina é formada no peixe post mortem através da descarboxilação bacteriana do aminoácido histidina como se representa na figura 3.4. As espécies mais frequentemente envolvidas são aquelas que apresentam elevados teores de histidina livre tal como as pertencentes à família Scombridae, mas podem estar também envolvidas espécies não escombroides como as pertencentes à família Clupeidae e o mahi-mahi no envenenamento por histamina.
As bactérias que produzem a histamina são algumas Enterobacteriaceae, Vibrio sp., Clostridium e Lactobacillus sp. Os produtores mais potentes de histamina sã a Morganella morganii, Klebsiella pneumoniae e Hafnia alvei (Stratten e Taylor, 1991). Estas bactérias podem ser encotradas na maior parte das espécies de peixes, provavelmente, como resultado de uma contaminação após a captura. Desenvolvem-se bem a 10°C, mas a 5°C a sua proliferação é grandemente retardada e quando a temperatura é mantida sempre abaixo de 5°C nunca há produção de histamina pela M. morganni (Klausen e Huss, 1987). Contudo, formavam-se grandes quantidades de histamina pela M. morganii a temperaturas baixas (0– 5°C) a seguir a uma armazenagem, até 24 horas, a temperaturas mais altas (10–25°C), ainda que a proliferação bactriana não tivesse ocorrido a 5°C ou abaixo desta temperatura.
Muitos estudos são unânimes em afirmar que as bactérias produtoras de histamina são mesófilas. No entanto, Ababouch et al. (1991) detectaram uma produção considerável de histamina em sardinha armazenada a temperaturas <5°C e van Spreekens (1987) referiu uma produção de histamina por Photobacterium sp. que se podem desenvolver a temperaturas <5°C.
A M. morganii, a principal bactéria produtora de histamina, desenvolve-se melhor a pH neutro, mas o seu desenvolvimento pode também ocorrer na gama de pH de 4, 7–8, 1. O organismo não é muito resistente ao NaCl, mas para condições óptimas diferentes, o desenvolvimento pode ocorrer até a níveis de 5% de NaCl. Assim, a produção de histamina por este organismo constitui apenas um problema em produtos de pescado ligeiramente salgados.
Deve salientar-se que se houver produção de histamina no peixe, o risco de provocar doença é muito elevado. Esta amina biogénica é muito resistente ao calor pelo que, mesmo que o peixe seja cozinhado, enlatado ou tratado a quente de qualquer outra maneira, antes de ser consumido, a histamina não é destruída.
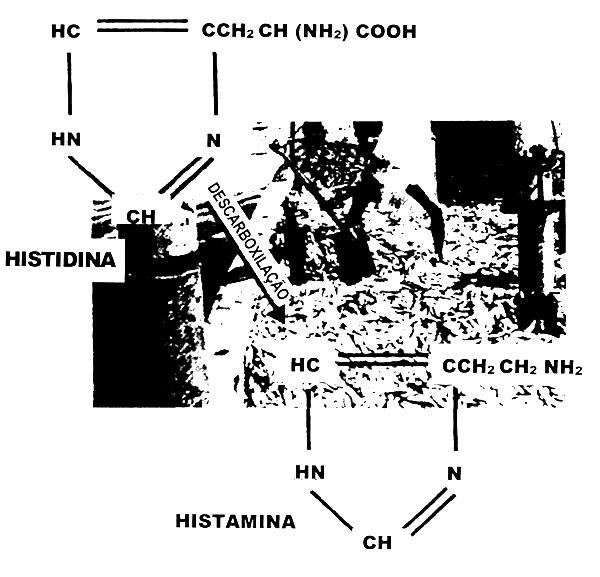
Figura 3.4. Estrutura química da histamina (fotografia de Pan e James, 1985).
A prova de que a histamina é a causadora da doença é a maior parte das vezes circunstancial. Altos níveis de histamina têm sido encontrados em amostras implicadas em surtos e os sintomas observados indicam que a histamina é o agente causador. Todavia, a ingestão de um nível elevado de histamina nem sempre provoca a doença mesmo quando é ultrapassado o “nível de risco” (50 mg/100g de atum).
O corpo humano pode tolerar uma determinada quantidade de histamina sem que haja reacção. A histamina ingerida será eliminada no tracto intestinal por, pelo menos, duas enzimas. Estas sào diamina oxidase (DAO) e a histamina N-metiltransferase (HMT) (Taylor, 1986). Este mecanismo de protecção pode ser eliminado se a ingestão de histamina e/ou outras aminas biogénicas for muito elevada ou ainda se as enzimas forem bloqueadas por outros compostos como está representado na figura 3.5.
Outras aminas biogénicas tais como a cadaverina e a putrescina, cuja ocorrência no peixe deteriorado é bem conhecida, podem actuar, consequentemente, como potenciadores de toxicidade histamínica. A inibição do catabolismo da histamina a nível intestinal pode resultar, presumivelmente, num maior transporte de histamina através das membranas celulares e entrar na circulação sanguínea.
A manutenção do peixe a baixa temperatura durante toda a armazenagem constitui a medida mais eficiente. Todos os estudos parecem concordar que a armazenagem a O°C ou muito próximo desta temperatura limita a formação de histamina no peixe a níveis desprezáveis.
Vários países têm adoptado regulamentações, determinando os níveis máximos permissíveis de histamina no peixe. No Quadro 3.9 apresentam-se alguns exemplos.

Figura 3.5. O conceito de doença de histaminose induzida por alimentos (segundo Sattler e Lorenz, 1990)
| Nível de intervenção (em caso de perigo) mg/100g | Nível de intervenção (em caso de perigo) mg/100g | Limite méximo permitido mg/100g | |
|---|---|---|---|
| USA (FDA) | 50 | 10–20 | - |
| UE | - | 10 | 20 |
A presença de parasitas no peixe é muito frequente, mas a maior parte deles são pouco preocupantes no que respeita à economia ou à saúde pública. Healey e Juranek (1979), Higashi (1985) e Olson (1987) publicaram vários artigos sobre este tema.
No entanto, são conhecidas mais de 50 espécies de parasitas helmintas do peixe e marisco que provocam doenças no homem. Muitas são raras e envolvem apenas danos ligeiros a moderados, mas algumas colocam riscos potenciais de saúde. Os mais importantes encontramse no Quadro 3.10.
Todos os parasitas helmintas têm ciclos de vida complexos. Não se transmitem directamente de peixe para peixe, mas durante o seu desenvolvimento têm de passar por um certo número de hospedeiros intermediários. Muito frequentemente os caracóis do mar ou os crustáceos estão envolvidos como primeiros hospedeiros intermediários e peixes marinhos como os segundos hospedeiros intermediários enquanto que o parasita sexualmente maduro se encontra em mamíferos como hospedeiros definitivos.
Entre estes hospedeiros, pode ocorrer um ou mais estádios de vida livre. A infecção do homem pode fazer parte deste ciclo de vida ou constituir uma via paralela, causando rotura no ciclo de vida como se mostra na figura 3.6.

Figura 3.6. Ciclo de vida do Anisakis simplex.
Os vermes redondos ou nemátodos encontram-se frequentemente nos peixes marinhos de todo o mundo. Os nemátodos anisakis A. simplex e P. dicipiens, normalmente conhecidos por verme do arenque e por verme do bacalhau, respectivamente, têm sido muito estudados. São vermes redondos típicos, com 1 a 6 cm de comprimento que, se forem ingeridos vivos, podem penetrar nas paredes do tracto gastrointestinal do Homem e causar uma inflamação aguda (“doença provocada por vermes do arenque”, uma anisakiase). O ciclo de vida completo do Anisakis sp. encontra-se representado na figura 3.6.
| Parasita | Distribuição geográfica conhecida | Peixe e marisco |
|---|---|---|
| Nemátodos ou vermes redondos | ||
| Anisakis simplex | Atlântico Norte | arenque |
| Psudoterranova dicipiens | Atlântico Norte | bacalhau |
| Gnathostoma sp. | Ásia | peixe de água doce, rãs |
| Capillaria sp. | Ásia | peixe de água doce |
| Angiostrongylus sp. | Ásia, América do Sul, África | gambas de água doce, caracóis, peixes |
| Céstodos ou ténias | ||
| Diphyllobothrium latum | Hemisfério Norte | peixe de água doce |
| D. pacificum | Perú, Chile, Japão | peixe de água salgada |
| Tremátodos ou fascíolas | ||
| Clonorchis sp. | Ásia | peixe de água doce, caracóis |
| Opisthorchis sp. | Ásia | peixe de água doce |
| Metagonimus yokagawai | Extremo Oriente | |
| Heterophyes sp. | Médio Oriente, Extremo Oriente | caracóis, peixe de água doce e salobra |
| Paragonimus sp. | Ásia, América, África | caracóis, crustáceos, peixes |
| Echinostoma sp. | Ásia | amêijoas, peixe de água doce, caracóis |
Um certo número de outros nemátodos encontra-se em peixes de águas doces. Os Gnathostoma sp. são as espécies mais importantes que se encotram na Á sia. Os hospedeiros definitivos são os gatos e os cães, mas o Homem pode ser também infectado. Após a ingestão, as larvas migram do estômago para várias regiões, mais frequentemente para zonas subcutâneas no tórax, braços, cabeça e pescoço onde os vermes induzem uma sensação de comichão e edema.
Um outro nemátodo com importância para a saúde pública é a Capillaria sp. (p. ex., Capillaria philippinensis). Os vermes adultos são parasitas do tubo digestivo de aves que se alimentam de peixes e os hospedeiros intermediários são pequenos peixes de água doce. A infecção no Homem causa diarreias graves e morte provável devido à perda de água nas fezes. Um nemátodo bem conhecido e frequente na Ásia éo Angiostrongylus sp. (por exemplo, Angiostrongylus cantonensis). O verme adulto encontra-se nos pulmões dos ratos e os hospedeiros intermediários são caracóis, gambas de água doce e caranguejos de terra. Tem-se verificado que o parasita causa meningite no Homem (Figura 3.7).
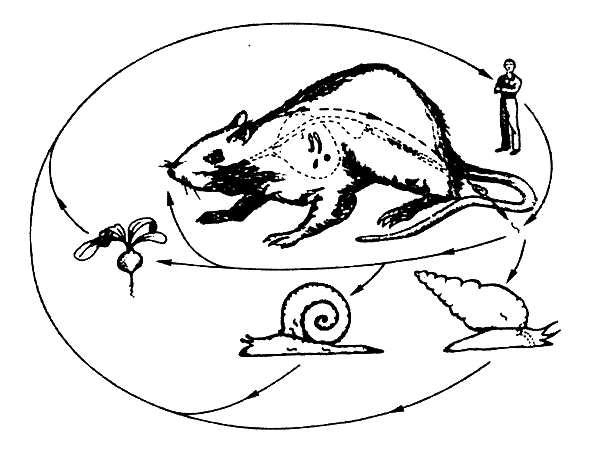
Figure 3.7. Ciclo de vida dos angiostronglidos (Angiostrongylus sp.). Os nemátodos sexualmente dióicos acasalam e produzem ovos que saem com as fezes ou eclodem no intestino. O A. cantonensis atinge a maturidade nos pulmões e o A. costaricensis atinge a maturidade nos intestinos. As larvas migram para locais húmidos e podem invadir invertebrados como os gastrópodes. Os mamíferos podem ingerir as larvas através do consumo de invertebrados infectados crus ou de vegetais. Nos mamíferos, as larvas penetram no intestino e migram para outras vísceras. O A. cantonensis migra através do espaço subaracnoide e desenvolve-se, antes de migrar para os pulmões. No Homem, as larvas não migram além do cérebro. Nos ratos, o A. cantonensis migra nas vísceras, músculos e pele antes de regressar ao intestino. No Homem continua a migrar até que morre. O ciclo de vida dos gnatostomatídeos é semelhante; parecem infectar e migrar em quase todos os hospedeiros intermediários, mas apenas atingem a maturidade naquele que lhes proporciona o sinal fisiológico adequado (segundo Brier, 1992).
Apenas alguns céstodos ou ténias presentes no Homem são transmitidos pelos peixes. No entanto, a grande ténia do peixe, o Diphyllobothrium latum, é um parasita frequente no Homem onde atinge, no tracto intestinal, até 10m ou mais de comprimento. Este parasita tem como primeiro hospedeiro intermediário um microcrustáceo e um peixe de água doce como segundo intermediário (Fig 3.8). A espécie afim, D. pacificum, é transmitida por peixes de água salgada e ocorre frequentemente em águas consteiras do Perú, Chile e Japão onde é usual o consumo de produtos crus de pescado (“ceviche”, sushi e outros).
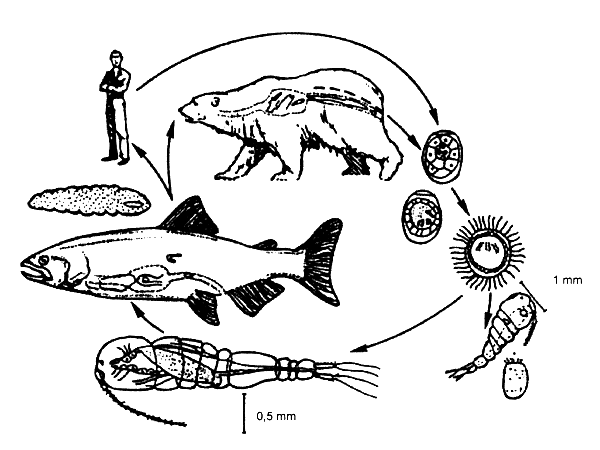
Figura 3.8. Ciclo de vida genérico duma ténia. O Diphyllohotrium sp. atinge a maturidade sexual no tracto digestivo dos mamíferos. Os ovos podem ser expelidos com as fezes, eclodirem na água e desenvolverem-se em larvas que nadam livremente. As larvas, se forem consumidas por um copépode ou outro crustáceo adequado, podem-se tornar infecciosas para um peixe que tenha consumido os crustáceo adequado, infectados. Estas larvas desenvolvem-se então em formas que podem infectar outros peixes, onde já não vêm a desenvolver-se, ou em mamíferos onde podem atingir a maturidade sexual sexual (segundo Brier, 1992).
Alguns Tremátodos ou fascíolas são extremamente frequentes, em particular, na Ásia. Assim, estima-se que o Clonorchis sinensis (a fascíola do figado) infecta mais de 20 milhões de pessoas na Ásia. No sul da China a taxa de clonorquíase no Homem pode ultrapassar, nalgumas regiões, 40% dos habitantes (Rim, 1982). Os hospedeiros intermediários são caracóis e peixes de água doce enquanto que os cães, gatos, animais selvagens e o Homem são os hospedeiros definitivos onde as fascíolas vivem e se desenvolvem nos canais biliares do figado. O problema dominante na transmissão é a contaminação das águas infestadas por caracóis pelas fezes de origem humana que transportam os ovos (por exemplo, uso do líquido das nitreiras como fertilizantes).

Figura 3.9. Ciclo de vida da fascíola do figado. Estes tremátodos atingem a maturidade sexual no figado do Homem e noutros mamíferos. Os ovos entram no intestino através da bílis, são incorporados nas fezes do hospedeiro e, se forem ingeridos por um molusco, podem eclodir. As larvas penetram nos tecidos através de estádios morfológicos distintos os quais, por reprodução assexuada, produzem larvas nadadoras livres. As larvas do Clonorchis sinensis podem infectar apenas algumas espécies de peixes enquanto que as do Opisthorchis sinensis podem infectar tanto peixes como moluscos hospedeiros. As larvas nestes hospedeiros tornam-se infecciosas para os mamíferos que consumam os hospedeiros intermediários infectados, crus ou mal cozinhados (segundo Brier, 1992).
Duas fasciolas muito pequenas (1–2 mm), a Metagonimus yokagawai e a Heterophyes heterophies diferem do Clonorchis por viverem nos intestinos do hospedeiro definitivo, causando inflamação, sintomas de diarreia e dores abdominais. Os hospedeiros intermediários são caracóis e peixes de água doce (Figura 3.10).

Figura 3.10. Ciclo de vida de um heterofideo. As pequenas fascíolas do intestino atingem a maturidade sexual no intestino delgado do Homem e de outros mamíferos. A maturação tem lugar no interior dos folículos do intestino, onde alguns ovos podem entrar no sistema circulatório e causar perturbações cardíacas. Os ovos que saiem com as fezes podem-se transformar em larvas as quais, se forem consumidas por um hospedeiro gastrópode compatível, eclodem e penetram nos tecidos do caracol onde se desenvolvem através de duas gerações morfologicamente distintas. A larva resultante que apresenta capacidade para se mover deixa o caracol hospedeiro e pode penetrar nos tecidos de um peixe hospedeiro para formar o estádio infeccioso dos mamíferos. O ciclo de vida pode-se completar se o Homem ou outros mamíferos consumirem os peixes hospedeiros infectados, crus ou mal cozinhados (segundo Brier, 1992).
A fasciola oriental do pulmão no estado adulto, a Paragonimus sp, tem 8 a 12 mm de comprimento, encontrando-se encapsulada viva sob a forma de cistos nos pulmões do Homem, gatos. cães. porcos e muitos outros animais selvagens carnívoros. Os caracóis e os crustáceos (caranguejo de água doce) são os hospedeiros intermediários (Figura 3.11).

Figura 3.11. Ciclo de vida de uma fascíola do pulmão. As Paragonimus sp. atingem a maturidade sexual nos pulmões do Homem e de outros mamíferos e encontrase, habitualmente, aos pares nos alvéolos pulmonares. Os ovos são expelidos na saliva ao tossir e'são também excretados nas fezes. As larvas com vida livre saiem e eclodem em condições de humidade adequada. Se estas larvas encontram um hospedeiro gastrópode podem entrar e desenvolver-se assexuadamente através de duas formas morfológicas distintas, dando origem a larvas com vida livre. Estas penetram depois nos tecidos macios de um caranguejo ou de um lagostim de água doce e são encapsuladas num estádio infeccioso para os mamíferos. As larvas que são consumidas por um mamífero atravessam de seguida a parede intestinal e migram através dos tecidos. Nalguns hospedeiros a migração continua sem desenvolvimento posterior; todavia, estas larvas continuam a ser infecciosas para os mamíferos que consomem os hospedeiros crus. As larvas, nos hospedeiros que possuem o sinal fisiológico apropriado, migram para os pulmões e atingem a maturidade (segundo Brier, 1992).
Todos os parasitas que constituem perigo são transmitidos ao Homem através do consumo de pescado cru ou mal cozido. As medidas de controlo para reduzir os problemas para a saúde pública relacionados com a presença de parasitas incluem legislação e vigilância. Em princípio, e segundo a WHO (1989), o problema pode ser atacado a três níveis, como se enumera a seguir para o caso do nemátodos:
Evitar a captura de peixe infectado por nemátodos através da selecção de áreas de pesca, de espécies especificas ou de grupos de idade específios.
Escolher e eliminar peixes infectados por nemátodos ou remoção dos nemátodos do peixe, por exemplo, à mão, colocando o peixe sobre uma mesa iluminada.
Aplicar técnicas para matar os nemátodos presentes na carne do peixe.
Apenas os pontos 2) e 3) são aplicados na pesca comercial.
As medidas de controlo são particularmente importantes para o pescado que irá ser consumido cru ou parcialmente cozinhado (arenque fermentado típico da Holanda, peixe marinado, peixe ligeiramente salgado e peixe fumado a frio, “ceviche”, ‘sashimi’, ‘sushi’. etc.). Assim, a maior parte das regulamentações de saúde de cada país, por exemplo, o decreto alemão sobre exigências de saúde em relação ao peixe e ao marisco (Decreto Alemão sobre o Pescado, 1988) contém regras específicas para o manuseamento e o processamento deste tipo de peixe com o objectivo de se assegurar que todos os nemátodos sejam mortos (processamento de segurança). Com base numa investigação coordenada entre a Holanda, Alemanha e Dinamarca (Huss et al., 1992), foram estabelecidos os seguintes critérios tendo em vista um processamento seguro:
Peixe marinado:
O processamento de segurança baseia-se, principalmente, no nível de NaCl na fase aquosa do tecido. Quando é usada a quantidade mínima de ácido acético (2,5% a 3% no fluido do tecido), foram registados os seguintes períodos máximos de sobrevivência dos nemátodos a vários níveis de NaCl:
| % de NaCl no fluido do tecido | Período máximo de sobrevivência dos nemátodas |
|---|---|
| 4–5 | >17 semanas |
| 6–7 | 10 a 12 semanas |
| 8–9 | 5 a 6 semanas |
Os períodos máximos de sobrevivência dos nemátodos devem ser, por conseguinte, também os períodos mínimos de armazenagem do produto final antes de ser vendido.
Peixe tratado a quente:
Todos os nemáodos são eliminados quando aquecidos à temperatura de 55°C durante 1 minuto. Isto significa que o pescado fumado a quente, pasteurizado, cozinhado a vácuo bem como outros tipos de produtos de pescado tratados ligeiramente a quente são seguros. Contudo, algumas tradições culinárias caseiras usuais podem não cumprir as regras de segurança.
Peixe congelado:
A congelação a -20°C e a manutenção do pescado a esta temperatura durante pelo menos 24 horas leva à morte de todos os nemátodos.
Os resultados apresentados anteriormente mostram que alguns produtos derivados do pescado não são seguros. Isto aplica-se ao pescado pouco salgado < 5–6% de NaCI na fase aquosa) tal como arenque fermentado típico da Holanda, peixe “gravad”, peixe fumado a frio, caviar pouco salgado, ceviche e muitos outros produtos tradicionais locais. Um curto período de congelação quer de peixe cru quer de produtos finais deve ser, portanto, incluído no processamento como um meio de controlar os parasitas.
A contaminação com produtos químicos como causa de doenças provocadas pelo consumo de pescado figura muito pouco nas estatísticas oficiais (ver Quadro 2.2).
Os contaminantes químicos com algum potencial tóxico parecem ser (Ahmed, 1991):
Compostos inorgânicos: antimónio, arsénico, chumbo, mercúrio, selénio, sulfitos (usados no processamento de camaraão).
Compostos orgânicos: bifenilos policlorados, dioxinas, insecticidas (hidrocarbonetos clorados).
Compostos relacionados com o processamento: nitrosaminas e contaminantes relacionados com a aquacultura (antibióticos, hormonas).
Nos ambientes aquáticos limpos encontra-se sempre uma pequena concentração de contaminantes. Alguns metais como o cobre, selénio, ferro e zinco são nutrientes essenciais para o peixe e marisco. A contaminação ocorre quando há um aumento, estatisticamente significativo, dos níveis médios em organismos comparáveis.
Os problemas relacionados com a contaminação química do ambiente são quase todos provocados pelo Homem. As descargas nos oceanos de centenas de milhões de toneladas de desperdícios do processamento industrial, de lamas provenientes das instalações de tratamento de esgotos, a drenagem para o mar dos produtos químicos utilizados na agricultura e de esgotos não tratados, de grandes populações urbanas e de indústrias, são todos eles responsáveis pela contaminação dos ambientes marinhos costeiros ou de água doce. Éa partir daqui que estes produtos químicos têm acesso ao pescado e a outros organismos aquáticos. Têm-se vindo a registar quantidades crescentes de produtos químicos em espécies predadoras como resultado da bioamplificação que é a concentração de productos químicos nos níveis mais altos da cadeia alimentar. Podem também resultar de bioacumulção, quando concentrações crescentes de produtos químicos se acumulam nos tecidos ao longo da vida de um indivíduo. Neste caso, um peixe grande (isto é, um peixe mais velho) terá um teor mais elevado de determinado produto químico do que um peixe mais pequeno (mais novo) da mesma espécie. A presença de contaminantes químicos no pescado está, portanto, muito dependente da localização geográfica, da espécie e do tamanho do peixe, dos padrões alimentares, da solubilidade dos produtos químicos e da sua persistência no ambiente.
Price(1992), num estudo recente sobre a presença de resíduos químicos no pescado, concluiu que o risco de contaminantes químicos em peixe ou marisco capturados comercialmente é pequeno, não constituindo um problema. O risco resultante da presença de resíduos químicos (mercúrio, selénio, dioxinas, PCB, ‘kepone’, ‘clordano’, dieldrina e DDT) constituem um perigo no peixe e marisco capturados pela pesca desportiva, ou nos capturados em águas costeiras e (possivelmente) em águas muito poluídas.
No entanto, uma grande parte de um relatório de um comité sobre a Segurança do Pescado nos Estados Unidos (Ahmed, 1991) foi dedicada à ocorrência de contaminação química e aos riscos para a saúde com ela relacionada. Algumas das conclusões gerais e recomendções deste relatório são as seguintes:
Apenas uma pequena proporção do pescado está contaminada com concentrações apreciáveis de produtos químicos inorgânicos ou orgânicos potencialmente perigosos provenientes de fontes humanas ou naturais. Alguns dos riscos que podem ser considerados significativos incluem efeitos na reprodução provocados pelos PCB e metilmercúrio e carcinogénicos devidos aos congéeres dos PCB, às dioxinas e a alguns pesticidas de hidrocarbonetos clorados.
O consumo de alguns tipos de pescado contaminado representa um risco tal que exige um aumento dos esforços, tendo em vista a sua avaliação, a educação e o controlo daquele risco.
Os actuais processos de avaliação quantitativa do risco que são usados por organismos governamentais podem e devem ser melhorados e alargados a efeitos não cencerígenos.
O controlo constante e os programas de vigilância proporcionam uma representação inadequada da presença de contaminantes nas partes edíveis de pescado importado ou nacional de que resultam dificuldades sérias na avaliação tanto dos riscos como das oportunidades específicas de controlo.
A irregularidade da contaminação das espécies e das áreas geográficas torna exequível dirigir esforços de controlo específicos e ainda atingir reduções significativas em espécies que estejam expostas.
A base de dados para avaliar a segurança de alguns produtos químicos que se encontram no pescado, provenientes da aquacultura e do processamento, é insuficiente para permitir concluir que estes produtos estão a ser controlados efectivamente.
As principais recomendações do comité são as seguintes:
As actuais regulamentações para minimizar a contaminação biológica e qumica do ambiente aquático devem ser fortalecidas e reforçadas.
As actuais regulamentações da FDA e estatais devem ser fortalecidas e reforçadas no sentido de reduzir o consumo de organismos aquáticos que tenham níveis de contaminação relativamente elevados (por exemplo, algumas espécies dos Grandes Lagos com elevados ní de PCB, o espadarte e outras espécies com níveis elevados de metilmercúrio).
As agências federais devem apoiar activamente mais investigações para determinar os riscos actuais resultantes do consumo de contaminantes associados ao pescado e para desenvolver abordagens específicas para eliminar estes riscos.
O aumento da vigilância do meio ambiente deve ser iniciado a nível estatal, constituindo parte de um vasto programa federal de gestão dos níveis de exposição.
Os diversos países devem continuar a ser responsáveis pela interdição de locais e pela publicação de normas sobre a contaminação e a saúde que correspondam a hábitos de consumo específicos, de reprodução ou quaisquer outros riscos específicos, bem como de fontes de informação para grupos específicos de consumidores.
Deve haver um amplo programa de educação pública sobre os perigos de contaminantes químicos específicos, dinamizado por organismos governamentais e por profissionais da saúde.
Alguns exemplos de teores residuais máximos de contaminantes químicos no peixe para consumo são apresentados no Quadro 3.11.
| Produto químico | Limite máximo de resíduo (mg/kg) | Paí |
|---|---|---|
| DDT + DDE + DDD | 2 | Dinamarca |
| Dieldrina | 0,1 | Suécia |
| PCB | 2 | Suécia |
| Chumbo | 2 | Dinamarca |
| Mercúrio | 0,5 | CEE |
O elevado teor em proteínas e em azoto não proteico (por exemplo, aminoácidos, óxido de trimetilamina, OTMA, creatinina) é uma das características do tecide muscular do peixe. Apresenta, todavia, um baixo teor em hidratos de carbono de que resulta um valor de pH alto (>6,0). Além disso, os peixes gordos, pelágicos, têm um elevado teor em lípidos, constituídos, principalmente, por triglicéridos com ácidos gordos de cadeia comprida que são, também, muito insaturados. Os fosfolípidos são igualmente muito insaturados o que tem importantes consequências nos processos de deterioração nas condições de armazenagem em aerobiose.
O estado designado por “deteriorado” não está claramente definido em termos objectivos. Podem-se indicar os seguintes sinais evidentes de deterioração:
detecção de cheiros e sabores desagradáveis
formação de muco
produção de gás
coloração anormal
alterações na textura.
O desenvolvimento destes sinais de deterioração do peixe e dos produtos da pesca é devido a um conjunto de fenómenos microbiológicos, químicos e autolíticos.
A perda da qualidade inicial nas espécies magras ou não gordas (não conservadas), arrefecidas ou não, é provocada por alterações autolíticas enquanto que a deterioração é devida, principalmente, à acção das bactérias (ver figura 3.12).
A flora inicial do peixe é muito diversa, embora as bactérias psicrotróficas Gram-negativas sejam, muitas vezes, dominantes. O peixe capturado em áreas tropicais pode transportar uma carga ligeiramente mais elevada de organismos Gram-positivos e bactérias entérias entéricas. Durante a armazenagem, desenvolve-se uma flora característica mas apenas parte dela contribui para a deterioração (ver Quadro 3.12). Os organismos específicos de deterioração (OED) produzem metabolitos responsáveis pelo desenvolvimento dos cheiros e sabores desagradáveis associados à deterioração.
A Shewanella putrefaciens é uma bactéria típica da deterioração de muitas espécies de peixes de águas temperadas, conservadas em refrigerado e em condições aeróbias e produz trimetilamina (TMA), sulfureto de hidrogénio (H2S) e outros sulfuretos voláteis, responsáveis pelos cheiros e sabores a peixe e pelos que lembram couve estragada. Metabolitos semelhantes são produzidos por bactérias Vibrionaceae e Enterobacteriaceae durante a deterioração a temperaturas altas. Durante a armazenagem em atmosferas modificadas (contendo CO2), uma espécie de Photobacterium psicrófilo, que produz grandes quantidades de TMA, é uma das principais bactérias responsáveis pela deterioração. Alguns peixes de água doce e muitas espécies de águas tropicais, durante a armazenagem em gelo e em condições aeróbias, são caracterizados por apresentarem uma deterioração do tipo Pseudomonas que é descrita como sendo frutada, a sulfidrilo e enjoativa. As Pseudomonas produzem vários sulfuretos voláteis (por exemplo, metilmercaptano CH3SH) e sulfureto de dimetilo ((CH3)2S), cetonas, ésteres e aldeídos, mas não sulfureto de hidrogénio. Para o peixe fresco, não conservado, os OED que têm sido identificados, apresentam-se no Quadro 3.12. A putrefacção ou deterioração ocorre muito rapidamente desde que a carga de OED exceda, aproximadamente, 107 UFC/g.
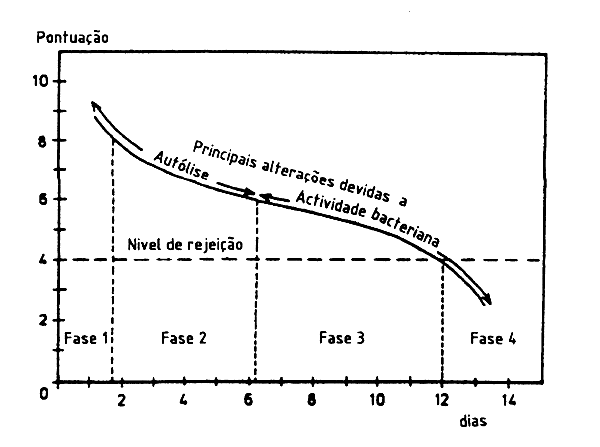
Figura 3.12. Alterações na qualidade sensorial do bacalhau conservado em gelo (0°C) (segundo Huss, 1988).
A actividade microbiana é também a causa da deterioração de muitos produtos detivados do pescado conservados e armazenados a temperaturas acima de 0°C. Todavia, na maioria dos casos, as bactérias específicas de deterioração não são conhecidas. A adição de pequenas quantidades de sal e ácido, tal como acontece nos produtos de derivados do pescado ligeiramente conservados, altera a microflora dominante, principalmente, para estirpes de bactérias Gram-positivas (bactérias lácticas, Brochotrix) e algumas destas podem actuar como OED em certas condições como se mostra no Quadro 3.13. No entanto, também algumas Enterobacteriaceae e Vibrionaceae podem actuar como OED destes produtos. Além disso, nos produtos com baixos níveis de conservação, a Shewanella putrefaciens pode ter também um papel importante.
També os produtos derivados do pescado com um maior grau de conservação tais como os produtos salgados ou fermentados se alteram devido à acção de alguns microrganismos. A flora dominante nestes produtos é Gram-positiva, halófila ou micrococos halotolerantes, leveduras, esporos, bactérias lácticas e bolores. Um certo número de OED tais como bastonetes Gram-negativos, extremamente halófilos, e leveduras halófilas foi identificado por Køchel e Huss (1984) como organismos específicos de deterioração ao provocarem no arenque salgado o desenvolvimento de cheiros e sabores desagradáveis (a sulfidrico, frutados). Uma bactéria de deterioração, extremamente halófila, provoca o aparecimento do “rouge”.
| Temperatura de armazenagem | Atmosfera da embalagem | Microflora dominante | Organismos específicos de deterioração (OED) | Referências |
|---|---|---|---|---|
| 0°C | Aeróbica | Psicrotrófica Gram-negativa, bastonetes não fermentativos (Pseudomonas sp., S. putrefaciens, Moraxella, Acinetobacter) | S. putrefaciens Pseudomonas3 | 2,3,4,9 |
| Vácuo | Bastonetes Gram-negativos, psicrotróficos ou com carácter psicrófilo (S. putrefaciens, Photobacterium) | S. putrefaciens P. phosphoreum | 1,9 | |
| EAM1 | Bastonetes fermentativos Gram-negativos com carácter psicrófilo (Photobacterium) Bastonetes psicrotróficos não fermentativos Gram-negativos (1-10% da flora; Pseudomonas, S. putrefaciens) Bastonetes Gram-positivos (BL2) | P. phosphoreum | 1,7 | |
| 5°C | Aeróbica | Bastonetes psicrotróficos Gram-negativos (Vibrionaceae, S. putrefaciens) | Aeromonas sp. S. putrefaciens | |
| Vácuo | Bastonetes psicrotróficos Gram-negativos (Vibrionaceae, S. putrefaciens) | Aeromonas sp. S. putrefaciens | ||
| EAM | Bastonetes psicrotróficos Gram-negativos (Vibrionaceae) | Aeromonas sp. | 6 | |
| 20–30°C | Aeróbica | Bastonetes fermentativos mesófilos Gram-negativos (Vibrionaceae, Enterobacteriaceae) | Aeromonas sp. móvel (A. hydrophila) | 2,4,5,8 |
1) Embalagem em Atmosfera Modificada (contendo CO2)
2) BL: Bactérias lácticas
3) A deterioração do peixe capturado em águas tropicais ou em água doce é, em geral, dominada por Pseudomonas sp.
Referências: 1) Dalgaard et al. (1993), 2) Gram et al. (1987), 3) Lima dos Santos (1978), 4) Gram et al. (1990), 5) Gorezyca e Pek Poh Len(1985), 6) Donald e Gibson (1992), 7) van Spreekens (1977), 8) Barile et al. (1985), 9) Jørgensen e Huss (1989).
| Produto | Atmosfera da embalagem | Outros conservantes além do NaCl | Sinais de deterioração | Microflora dominante | Organismos específicos de deterioração (OED)1 |
|---|---|---|---|---|---|
| Peixe fumado a frio | Vácuo | - | Cheiro e sabor desagradáveis (pútrido, enjoativo, a enxofre) | Bastonetes Gram-negativos (Enterobacteriaceae, Vibrionaceae) ocasionalmente BL2 | ??? |
| Sabor desagradável (azedo, acre) | BL | ??? | |||
| Perda de cheiro | BL | - | |||
| Camarões | Em salmoura | Ácido benzóico e/ou | Muco | BL | Leuconostoc sp |
| ácido sórbico; ácido cítrico; pH 5,5-5,8 | Produção de gás
Ocasionalmente fermentado Cheiro e sabor desagradáveis | BL | BL heterofermentativas, ocasionalmente leveduras | ||
| Diacetilo | BL | BL | |||
| - | Cheiro e sabor desagradáveis | BL, Brochothrix | ??? | ||
| Peixe com açúcar e sal (“gravad”) | Vácuo | - | Cheiro e sabor desagradáveis | BL, Brochothrix, ocasionalmente bactérias Gram-negativas | ??? |
| * Cavala: rançoso | (Enterbacteriaceae, | ||||
| * Salão: azedo e acre | Vibrionaceae, S. | ||||
| * Alabote da Groenlândia: pútrido | putrefaciens) | ||||
| EAM | - | Cheiro e sabor desagradáveis | Bactérias Gram-positivas | ??? | |
| (azedo) | (BL) |
1) Isto é, organismos espcíficos de deterioração que têm vindo a ser relaciondos com a detrioração do produto
2) BL = Bactérias lácticas.
Estas bactérias (Halococcus e Halobacterium) provocam o aparecimento de colorações vermelhas no sal, salmouras e no peixe salgado bem como o desenvolvimento de cheiros e sabores desagradáveis, associados normalmente à deterioração (sulfureto de hidrogénio e indol).
Alguns bolores halófilos (Sporendonema, Oospora) são também classificados como organismos responsáveis pela deterioração. Não produzem cheiros desagradáveis, mas a sua presença diminui o valor do produto em virtude do aspecto desagradável que lhe conferem.
Os processos de deterioração química mais importantes são as alterações que ocorrem na fracção lipidica do peixe. Os processos de oxidação, a autoxidação, envolvem apenas o oxigénio e os lipidos insaturados. O primeiro passo leva à formação de hidroperóxidos que não conferem nenhum sabor, mas podem levar ao aparecimento de colorações castanhas ou amarelas no tecido do peixe. A degradação dos hidroperóxidos dá origem à formação de aldeídos e cetonas como está representado na Figura 3.13. Estes compostos têm um sabor forte a ranço. A oxidação pode ser iniciada e acelerada pelo calor, luz (especialmente luz ultravioleta) e várias substâncias orgânicas e inorgânicas (por exemplo, Cu e Fe). São também conhecidos alguns antioxidantes que apresentam o efeito oposto (alfa-tocoferol, ácido ascórbico, ácido cítrico, carotenoides).

Figura 3.13. Processos básicos envolvidos na oxidação dos ácidos gordos polinsaturados que se encontram no tecido do peixe (segundo Ackman e Ratnayake, 1992).
A deterioração ou as alterações autoliticas são responsáveis pela perda inicial da qualidade do peixe fresco, mas contribuem muito pouco para a deterioração do peixe refrigerado e de outros produtos da pesca. Porém, o rápido desenvolvimento de cheiros desagradáveis e o aparecimento de manchas devido à acção das enzimas digestivas nalguns peixes não eviscerados constituem excepções. No entanto, no peixe congelado as alterações autoliticas são de grande importância. Um exemplo é a redução do óxido de trimetilamina (OTMA),que no peixe refrigerado é um processo bacteriano que leva à formaçào de trimetilamina (TMA) No peixe congelado, porém, a actividade bacteriana é o OTMA é convertido em dimetilamína (DMA) e formaldeído (FA) por enzimas autolíticas:
(CH3)3N:O → (CH3)2 NH + HCHO
O efeito do FA formado no peixe congelado é provocar um aumento na desnaturação do músculo do peixe, alterar a textura e diminuir a capacidade de retenção de água. Amite-se também que outras reacções enzimáticas tais como a formação de ãcidos gordos livres tenham uma grande influência na qualidade sensorial do peixe congelado. As enzimas autolíticas são activas a -20°C e mesmo abaixo desta temperatura, mas actuam muito mais rapidamente a temperaturas mais altas, próximo de zero.
As causas dos vários tipos de deterioração do pescado estão resumidas no Quadro 3.14.
| Sinais de deterioração | Causas da deterioração do peixe | |||
|---|---|---|---|---|
| Microbiológicas | Químicas (Oxidação) | Autolíticas | Físicas | |
| Cheiros e sabores desagradáveis | + | + | + | - |
| Formação de muco | + | - | - | - |
| Formação de gases | - | - | - | - |
| Coloração | (+) | + | + | + |
| Alterações de textura | (+) | - | + | + |
Todos os produtos alimentares proteicos degradam-se mais cedo ou mais tarde, mas podem ser tomadas algumas medidas para reduzir a taxa de deteriorção. O maior efeito pode ser obtido por controlo da temperatura de armazenagem. Tal como foi referido, a principal causa da deterioração é de origem bacteriana e na gama de temperaturas de refrigeração o padrão de proliferação dos organismos psicrotróficos de deterioração pode ser descrito, rigorosamente, pela relação da raiz quadrada conforme referido por Bremner et al. (1987). Assim, quando é usada a temperatura de 0°C como referência, a razão entre a proliferação bacteriana (r) a uma determinada temperatura t e a 0°C é dada pela expressão:
√r = 1 + 0.1 × t em que t é a temperatura em °C.
Isto significa que, se a temperatura de armazenagem for 10°C, o desenvolvimento das bactérias de deterioração é 4 vezes mais rápido do que a 0°C (√r=1+0.1x10,r=4) e o tempo de conservação é reduzido de igual modo.
A deterioração química ou desenvolvimento do cheiro a ranço pode ser impedido por um rápido manuseamento do pescado a bordo e armazenagem dos produtos em condições de anóxia (embalagem a vácuo ou em atmosfera modificada). A utilização de antioxidantes pode ser também considerada.
O efeito da temperatura de armazenagem na qualidade do peixe congelado é também pronunciado e a velocidade de deterioração é consideravelmente reduzida a temperaturas abaixo de -20°C.
O efeito da higiene no controlo da deterioração varia e depende do tipo de contaminação que pode ocorrer. Um grande esforço para reduzir a contaminação geral durante o manuseamento do pescado a bordo não leva a nenhum atraso significativo na deterioração (Huss et al., 1974) porque apenas uma fracção muito pequena desta contaminação geral é provocada por bactérias específicas de deterioração. Em contrapartida, as medidas de higiene para controlar a contaminação do peixe e dos produtos da pesca por bactérias especficas de deterioração influencia grandemente a velocidade de deterioração e o tempo de conservação (Jørgensen et al., 1988).