


Depuis très longtemps, les insectes comestibles contribuent au régime alimentaire de différentes populations dans le monde. La première partie de ce document traite des chenilles à partir des analyses provenant détudes de cas réalisées par des experts locaux dans quatre pays dAfrique centrale.
Ce document fournit des informations sur les ressources naturelles de base, lidentification taxonomique des insectes et de différentes espèces de plantes hôtes, mais aussi sur les chenilles dans leur habitat naturel; et enfin, il aborde lexploitation des ressources. Les techniques de récolte des chenilles dont la récolte manuelle et labattage des arbres comme les activités postrécolte de conservation et de préparation alimentaire sont détaillées.
Labondance saisonnière des insectes varie selon les différentes régions. La majorité des familles interrogées lors de la réalisation des études de cas consomme des chenilles. Celles-ci possèdent une forte valeur nutritionnelle et constituent une source importante de protéines dans les régimes alimentaires des populations dAfrique centrale. Différents modes de consommation sont présentés selon les habitudes culturelles ainsi que les autres ressources en protéines disponibles (viande de brousse, etc.). Le commerce des insectes, même saisonnier, peut offrir des revenus complémentaires aux populations rurales mais aussi aux populations urbaines, particulièrement aux femmes. Le document présente les filières commerciales et les types de revenus possibles ainsi que certaines données chiffrées au sujet de lexportation des chenilles.
Les relations entre les populations dinsectes et les forêts qui constituent leur habitat naturel, sont présentées, lexploitation forestière, les feux de brousse et les autres formes de dégradation de la forêt ayant un impact important sur les populations dinsectes. Enfin, les déficits de la recherche ont été identifiés et des recommandations ont été élaborées sur la manière dont les insectes comestibles pourraient contribuer à améliorer les conditions de vie locales et sur les moyens dintégrer la production de chenilles aux plans de gestion des ressources naturelles et de conservation des forêts.
Dans cette étude qui a pour thème principal les chenilles, une différence est faite entre les chenilles et les larves. Le Tableau 1 donne une définition des abréviations utilisées.
Tableau 1: Terminologie: chenilles, larves
Terme |
Définition |
Chenilles |
Les chenilles sont des larves de lépidoptères comme les papillons et les mites. Elles se nourrissent principalement de feuilles et des autres parties des arbres, arbustes et autres plantes. |
Larves |
Les larves sont des larves de coléoptères comme les charançons. Elles se développent sous lécorce des arbres, dans les troncs des palmiers, ou dans le sol. |

Commerçante semi-grossiste de chenilles
comestibles
au marché de Bangui (République centrafricaine) (NGasse)
Etudes de cas
Les quatre études de cas présentées dans la seconde partie du document ont été réalisées par des experts en 2002 et 2003:
NGasse, Georges (2003): Contribution des chenilles/larves comestibles à la réduction de linsécurité alimentaire en République centrafricaine.
Balinga, Michel Philippe (2003): Les chenilles et larves comestibles dans la zone forestière du Cameroun.
Moussa, Jean-Baptiste (2002): Les chenilles comestibles du Congo: Intérêt alimentaire et circuits de commercialisation: Cas de Brazzaville.
Monzambe Mapunzu, Paul (2002): Contribution de lexploitation des chenilles et autres larves comestibles dans la lutte contre linsécurité alimentaire et la pauvreté en République démocratique du Congo.
Pour la collecte des données, les chercheurs ont préparé des questionnaires dau moins deux types selon les groupes cibles de consommateurs, les différentes catégories de vendeurs, etc. Balinga (2003) a aussi analysé dautres études sur le sujet; NGasse (2003) a réalisé des interviews de différentes personnes clés pour obtenir des informations générales. Le Tableau suivant présente, sous forme globale, les zones détude et le nombre de personnes interrogées en tant quéchantillon des groupes cibles correspondants.
Synthèse des connaissances
La synthèse résume principalement linformation clé récoltée dans les quatre études de cas. Seules les données nationales ou régionales spécifiques ou exceptionnelles sont citées avec des références aux pays et/ou auteurs concernés.
Tableau 2: Etudes de cas: zones étudiées et nombre de personnes ayant répondu
NGasse (2003) |
Balinga (2003) |
Moussa (2002) |
Monzambe Mapunzu (2002) | |
Nombre de foyers |
100 dans la forêt de Ngotto |
180 dans la province du Centre, 20 dans celle de lEst, 130 de lOuest, 90 celle du Nord-Ouest, 174 Sud-Ouest et 96 dans la province du Littoral |
251 au total dans des établissements scolaires, lieux de vente alimentaire et sur les marchés de Brazzaville |
600 à Kinshasa |
Nombre de vendeurs |
100 à Bangui et 12 dans 11 autres villes autour de Bangui (dans un rayon de 400 km) |
9 à Yaoundé |
45 grossistes et 300 revendeurs de Kinshasa |
Dautres études sont citées lorsquelles contiennent des aspects spécifiques ou se réfèrent à dautres expériences dans des régions différentes, lorsque cette information nest pas disponible dans les études de cas. Cependant, ces études ont été revues partiellement, le thème essentiel de cette synthèse étant les études de cas.
Durant lanalyse des études de cas, des questions sont apparues qui ont dû être clarifiées ou expliquées avec plus de détails. Les auteurs ont donc été contactés afin de compléter certaines informations proposées dans la synthèse. Dautre part, des discussions avec plusieurs spécialistes entomologistes et experts en terme de consommation de viande de brousse en Afrique centrale, ont contribué à une meilleure compréhension et ont fourni des informations importantes. Un article a été préparé sur le sujet a été publié dans la série sur les politiques sur lenvironnement: Wildlife Policy Briefing nº 3 de lODI1 (Vantomme et al., 2004); les commentaires émis par rapport à cet article ont aussi enrichi cette synthèse.
Dans les études de cas, les données monétaires ont souvent été présentées en monnaie régionale: le Franc de la communauté française africaine (FCFA). Pour permettre la comparaison, des chiffres en dollar EU, basés sur les taux de change suivants, sont donnés (FAO, 2003): 1 FCFA = 0,0017 dollar EU ou 1 dollar EU = 604,792 FCFA.
Identification taxonomique des différentes espèces dinsectes
Selon de Foliart (2002), en Afrique de lEst et Afrique centrale, lidentification taxonomique exacte des insectes comestibles est connue pour 128 espèces. Autrement, 21 insectes comestibles sont seulement identifiés selon leur genre, 12 selon leur famille et un selon lordre. Une liste des chenilles identifiées au niveau taxonomique et des espèces de larves2 citées dans les études de cas, comprenant autant que possible les plantes hôtes, est présentée en annexe. Les Annexes fournissent des informations spécifiques sur les ressources naturelles de base de certains pays (avec les noms vernaculaires ajoutés aux noms scientifiques). La liste la plus complète est fournie par Monzabe Mapunzu (2002). Les données seulement composées de noms vernaculaires de larves ou de plantes hôtes ne sont pas présentées en annexe, mais dans les études de cas, dans la Partie B de ce document.
Les populations locales connaissent bien les chenilles et les larves mais elles ont parfois des difficultés à distinguer les différentes espèces. Lidentification taxonomique de nombreux insectes fait encore défaut. Malgré tout, plusieurs recherches ont été réalisées dans ce domaine.

Chenille Imbrasia epimethea (Internet, 2003) et papillon

Imbrasia dione, parmi les plus importants dAfrique centrale (Internet, 2003)
Abondance des insectes
Selon leur habitat, constitué par les plantes hôtes, les larves sont présentes dans différents types de forêt ainsi que dans les savanes arborées et les arbustes. NGasse (2003) a fait une recherche sur labondance de Nudaurelia oyemensis sur les plantes hôtes Entandrophragma angolense (sapelli) sur une période de 7 ans (1995 à 2001). Il a découvert quen moyenne, un arbre hôte était occupé par un poids correspondant à 3,3 kg (matière sèche) en chenilles. Il cite aussi une enquête de Serge Bahuchet3 (recherches réalisées de 1960 à 1970) établissant une présence de 2 kg/ha (matière sèche) de chenilles comestibles dans la Réserve de biosphère de Basse Lobaye. Dautres recherches indiquent des valeurs plus élevées. Par exemple, Latham (2002) analyse une présence de 5 kg/ha (matière sèche) pour Cirina forda dans la province du Bas-Congo (RDC). Munthali et Mughogho (1992) indiquent même 14,63 kg/ha (matière sèche) de chenilles comestibles au Malawi.
Techniques de récolte
La présence de chenilles se détecte de différentes manières. Par les déjections, tout dabord, qui saccumulent à la base des troncs dues aux proliférations des insectes et à lodeur évidente qui les identifie mais aussi du fait des rassemblements de chenilles à la base du tronc (cf. photo suivante) et par les feuilles mangées. La présence de larves dans les troncs de palmiers (comme Augosoma centaurus et Rhynchophorus phoenicis) peut aussi être perçue par les bruits caractéristiques de crépitement.

Colonie dImbrasia ertli dans le tronc de Funtumia sp. (Latham)
Dans la région dAfrique centrale, deux techniques différentes de récolte peuvent être distinguées. La première consiste à ramasser les chenilles manuellement sur le sol, les troncs, les branches et les feuilles. Ce sont principalement les femmes et les enfants, durant leurs vacances, qui sont chargés de cette activité. La récolte est facilitée lorsque les chenilles descendent des troncs à leur maturité. A cette période, les populations coupent aussi des branches entières pour améliorer la récolte ou pour mieux conserver les chenilles et ensuite les vendre vivante. Une attention spéciale doit être accordée aux espèces formant des processions (telle quImbrasia ertli). Dans ce cas, des cuvettes sont posées sur les troncs à une hauteur relativement basse afin quelles se remplissent en cinq ou six jours.
Afin de faire tomber les chenilles des parties hautes des arbres de taille moyenne, les récolteurs donnent parfois des coups de marteaux contre les troncs. Une longue tige en bambou est aussi utilisée pour atteindre le sommet des grands arbres et faire tomber les chenilles. Les pygmées de la RCA grimpent souvent dans les arbres pour récolter différents fruits et ramasser des chenilles (Bahuchet, 1990).
Une autre technique de récolte est labattage des arbres hôtes des chenilles. Dans le cas de larves qui se sont développées dans les troncs des palmiers, le palmier est coupé et fendu en deux. Les larves sont extraites vivantes ou après avoir été séchées au soleil avec le tronc durant une courte durée. Les palmiers à huile coupés pour la production de vin de palme fournissent des larves comme sous-produit. Contrairement à la collecte dinsectes, les coupes darbres et de palmiers sont principalement pratiquées par les hommes.
Dans létude de cas sur le Cameroun, les ménages interrogés pratiquent seulement la récolte dinsectes. En RDC, 65 pour cent des personnes interrogées coupent les arbres pour récolter les trois espèces de chenilles les plus nombreuses. Selon NGasse (2003), en RCA, les familles se déplacent pour se rapprocher de la forêt durant la période de récolte qui dure deux à trois mois. Elles y construisent des huttes temporaires et de petites grilles en bois pour le fumage des insectes. Contrairement à ce que Latham (2002) a observé dans le Bas-Congo (RDC), ces collecteurs déplacent fréquemment les jeunes chenilles des plantes hôtes venant de la forêt dans des arbres qui sont proches de leur village.
Périodes de récolte
La récolte des chenilles est une activité saisonnière alors que la récolte des larves sétend sur toute lannée. La période de collecte a souvent lieu durant la saison des pluies (Malaisse, 1997). La disponibilité des chenilles peut extrêmement varier entre les différentes régions dun pays en raison des conditions climatiques différentes (Tableau 3). Les pluies entravent les activités de récolte et encore plus la conservation des chenilles; le poisson et le gibier sont eux-mêmes souvent plus difficiles à attraper à la saison des pluies.
Tableau 3: Abondance des chenilles dans les pays dAfrique centrale
Pays |
Province |
Jan. |
Fév. |
Mar. |
Av. |
Mai |
Juin |
Juillet |
Aout |
Sept. |
Oct. |
Nov. |
Déc. |
RCA |
|||||||||||||
Cameroun |
|||||||||||||
RDC |
Kasaï oriental |
||||||||||||
Kasaï occidental |
|||||||||||||
Bandundu |
|||||||||||||
Kinshasa |
|||||||||||||
Rep. du Congo |
Sangha |
||||||||||||
Likoula |
|||||||||||||
Brazzaville |
|||||||||||||
Pool |
|||||||||||||
Plateaux |
La disponibilité saisonnière des chenilles affecte principalement la récolte des ménages ruraux alors que les zones urbaines sont souvent approvisionnées par différentes provinces. Ainsi, les chenilles sont vendues sur une plus longue période sur les marchés urbains que sur les marchés ruraux. Par exemple, Kinshasa est approvisionnée au moins sept mois par an.
Gestion
Dans les études de cas, on parle peu de la gestion des chenilles et de la production de larves et, si cette gestion est intégrée et de quelle manière, à la gestion de la forêt et des autres ressources naturelles.
Balinga (2003) précise que la taille des larves qui se développent dans le tronc des palmiers à huile est plus petite, cest pourquoi ces espèces sont seulement récoltées à des fins de subsistance. Au contraire, les espèces qui se développent dans les troncs de palmiers de Mayotte sont de meilleure qualité et prolifèrent énormément, aussi sont-elles davantage récoltées pour la commercialisation. Pour soutenir la reproduction des larves qui se nourrissent de matières mortes organiques (comme Rhynchophorus phoenicis), les palmiers sont parfois coupés pour favoriser le processus de décomposition. Après deux ou trois semaines, lextraction des larves est possible.

Sapelli, arbre hôte de Pseudanthera discrepans
défeuillé après le passage
des chenilles (NGasse)
En RCA, les règlements des concessions forestières requièrent actuellement de laisser au moins une graine dEntandrophragma angolense (sapelli) pour 10 hectares, pour la production de bois et pour permettre la régénération naturelle des espèces. Mais, aucune mention nest faite du besoin des populations locales de récolter des chenilles comestibles sur les feuilles de sapelli (comme Nudaurelia oyemensis). Même si cette injonction était respectée, laisser une seule graine darbre pour 10 hectares réduirait significativement la production de chenilles. De plus, dans la forêt de Lobaye, en RCA, NGasse (2003) a trouvé que les abattages darbres hôtes pour la récolte des chenilles ont considérablement réduit la population de jeunes sapelli.
Monzambe Mapunzu (2002) décrit différentes expériences de domestication de chenilles et de plantes hôtes. Dans la province du Bas-Congo (RDC), les expériences de domestication ont montré des résultats encourageants et ont en même temps souligné les déficits de la recherche. Dautres études ont été réalisées dans le domaine de la reproduction végétale. Les espèces suivantes de plantes hôtes ont été identifiées comme ayant de bonnes perspectives: Acacia auriculiformis, Antidesma membranaceum, Bridelia ripicola, Bridelia micrantha, Hymenocardia ulmoides et Chlorophora excelsa. Les efforts de domestication darbres hôtes doivent tenir compte du besoin daugmenter les systèmes agroforestiers en général. Les cultures comme les plantations agroforestières doivent répondre à la demande de marchés ciblés. Les plantations proches des villages faciliteront les récoltes familiales en raccourcissant les trajets.
Latham (1999) et Chidumayo (1997) ont fait des recherches sur la disponibilité des chenilles sur les terres forestières en jachère. Latham pense que les systèmes traditionnels de cultures itinérantes comprennent des périodes de jachère de 7 à 14 ans. Cette période de régénération permet à une grande quantité de plantes de se régénérer, en particulier les espèces forestières, offrant en même temps un nouvel habitat à divers espèces de chenilles. Cette situation change actuellement en raison de laugmentation de la population, la terre étant souvent cultivée de nouveau après deux ou trois années, et les rendements peu élevés avec une perte progressive de la biodiversité. Latham recommande dassister les agriculteurs afin de rétablir un usage multiple des jachères forestières.
Chidumayo (1997) a trouvé que les chenilles Gynanisa maja et Gonimbrasia zambesina sont majoritaires et sont les plus abondantes dans les jeunes repousses de forêt de miombo sur les cultures itinérantes de jachère par rapport aux peuplements anciens dune réserve forestière. Il conclut que les recrutements sur les terres en jachère fournissent davantage dhabitats favorables à ces deux espèces de chenilles, ce qui peut peut-être sexpliquer par la densité plus élevée darbres hôtes Julbernardia paniculata dans les repousses. Dans les anciennes repousses de forêt de miombo ayant subi une coupe sélective durant la récolte des chenilles Julbernardia paniculata, la mortalité est élevée (Chidumayo, Mbata, 2002) et la régénération par recrutement des jeunes plants semble être étouffée par lombre des arbres. Sur la base de ces résultats, Chidumayo et Mbata (2002) suggèrent que ces zones de réserve forestière pourraient comprendre certaines zones dédiées à la production de chenilles. Ce genre dapproche pourrait assurer que les populations locales tirent davantage de bénéfices des réserves forestières et cela pourrait aussi réduire les activités illégales pratiquées dans ces zones. Cette étude montre que des connaissances détaillées sur les processus naturels dans différents écosystèmes sont nécessaires pour mettre en place un système dexploitation des forêts.

Chenilles Imbrasia oyemensis sur
des feuilles de sapelli, son arbre hôte (NGasse)
Les études de cas fournissent peu dinformations sur les systèmes juridiques des systèmes fonciers et du cadre législatif. Selon Latham (2002), au Zimbabwe, les populations locales et les exploitants étrangers entrent en conflit à ce sujet. La CE et la FAO (2001) parlent de conflits similaires en Namibie. Le gouvernement namibien a entamé des actions pour transférer les droits des usagers aux communautés locales (CAMPFIRE: Communal areas management programme for indigenous resources). Une des conditions de départ pour le faire est leur organisation en associations locales.
Conservation des larves fraîches
Les chenilles vivantes peuvent seulement être conservées sur une durée très courte. Si on les empacte ou emballe dans des feuilles ou si elles sont lavées régulièrement, elle peuvent survivre deux ou trois jours. Au Cameroun, les feuilles de Xanthosoma sagittifolium (du macabo) sont en général utilisées pour la conservation des chenilles.
Balinga (2003) présente aussi un mode de conservation naturel des chenilles fraîches pratiqué au Cameroun. Le fait de rassembler une grande quantité de chenilles fait quelles développent une sorte de carapace protectrice leur permettant de survivre quelques mois. Aucune information détaillée sur les espèces concernées et les procédés à suivre nest donnée.
Conservation par séchage au soleil et fumage
Plusieurs méthodes de conservation ont été améliorées pour conserver les chenilles. Deux types dapproche peuvent être distingués: séchage au soleil et fumage. La larve séchée peut alors être stockée et transportée dans des grands seaux ou des sacs.
Pour faire sécher les larves au soleil (sur des grilles en bois, des tôles ondulées ou des claies) une longue période densoleillement est nécessaire ce qui fait que la procédure demande un certain temps. La méthode de séchage au soleil, moins pratiquée que le fumage, ne permet pas une longue conservation. Avant le séchage au soleil, les chenilles doivent être nettoyées. Souvent, les chenilles sont cuites avant, afin de les vider et de leur retirer leurs poils. Il est aussi essentiel de vider labdomen des chenilles qui se nourrissent de plantes toxiques (comme Lobobunaea phaedusa).
Les processus de fumage qui permettent de les conserver au moins trois mois, diffèrent légèrement selon les régions. Les chenilles sont fréquemment fumées après avoir été cuites durant 30 à 45 mn dans une eau salée ou nature, après les avoir exposées au soleil un ou deux jours. Autrement, les chenilles doivent être séchées dans un four avant dêtre fumées. Le fumage consiste à étaler les insectes sur une grille en bois ou un autre type de grille posée juste au-dessus du feu. Pour durcir les larves, le fumage ne doit pas dépasser un ou deux jours. Un autre moyen, surtout pratiqué avec des espèces à longs poils épais telles que Cirina forda, est de déposer la larve directement sur les braises du charbon de bois. La chaleur facilitera la dépilation et lélimination des déjections. Le séchage au soleil deux ou trois jours doit suivre la cuisson. Dans dautres régions encore, après leur avoir vidé labdomen, les chenilles sont perforées avec une tige de métal ou en bambou pour les cuire directement sur le feu. Cette méthode permet seulement de les conserver sur une durée limitée de deux semaines au maximum. La larve fumée prend une couleur brune et son goût change du fait de lacide pyroligneux qui est dégagé lors de la combustion du bois (Laurent, 1981). Selon NGasse (2003), le fumage réduit aussi les valeurs nutritionnelles. Un des problèmes les plus importants du fumage est que lon pense quil peut être cancérigène.
Préparation des insectes
En général, les insectes sont consommés à tous les stades de leur cycle de développement (uf, larve, adulte, etc.). Près de 80 pour cent des insectes sont mangés à un stade jeune, avant leur complète maturité (Ramos-Elorduy, 1996).
Les chenilles représentent un ingrédient courant dans la préparation locale des plats. Elles sont principalement mangées comme aliment de complément ou parfois comme encas. Pour préparer les larves fraîches, il faut les vider, les laver puis les cuire, les frire ou les griller de différentes manières. Une des possibilités peut être de préparer les chenilles dans de leau ou de lhuile (lhuile de palme de préférence), ou en y ajoutant différentes associations dépices (sel, piment, etc.) ou dautres ingrédients comme la pâte darachide. Souvent, elles sont mélangées avec de la sauce, du poisson, de la viande et/ou des légumineuses comme le manioc, des champignons, des feuilles (Gnetum africanum, Gnetum buchholzianum, etc.). Les espèces peu poilues perdent normalement leurs poils durant la cuisson, à la différence des espèces poilues comme Anaphe sp. dont la préparation requiert de les cuire dans les braises du charbon de bois. La préparation des larves séchées/fumées est analogue à celles qui sont fraîches, mais elles doivent être vidées et dépilées.
Valeurs nutritionnelles
Malaisse (1997) donne un bon aperçu des valeurs nutritionnelles des chenilles et confirme les connaissances empiriques des populations locales dune manière scientifique. Pour donner une idée de leur valeur nutritionnelle, la proportion moyenne de protéines et de graisses ainsi que leur valeur énergétique moyenne, 24 espèces de chenilles fraîches ont été analysées (Tableau 4, chiffres en matière sèche).
Tableau 4: Valeurs nutritionnelles des chenilles
Valeurs | |
Protéines |
63,5 ± 9,0 pour cent |
Graisses |
15,7 ± 6,3 pour cent |
Valeur énergétique |
457 ± 32 kcal/100 g |
Comparés au buf ou au poisson, les insectes possèdent une part élevée de protéines, de graisses et sont donc extrêmement énergétiques. Les protéines des insectes tendent à être peu élevées en acides aminés particuliers, comme la méthionine et la cystéine, et contiennent beaucoup dautres types, particulièrement en lysine et thréonine (de Foliart, 1992). De plus, la chitine nétant pas digérable, les insectes sont une source en protéines de mauvaise qualité par rapport aux aliments provenant des animaux vertébrés (Dreyer, Wehmeyer, 1982).
Selon les espèces, les chenilles sont riches en différents minéraux (K, Ca, Mg, Zn, P, Fe) et/ou vitamines (thiamine/B1, riboflavine/B2, pyridoxine/B6, acide pantothénique, niacine). Des études montrent que 100 g dinsectes cuits fournissent plus de 100 pour cent des besoins en vitamines et minéraux (de Foliart, 1992). Malaisse (1997) révèle que la consommation quotidienne de 50 g de chenilles séchées répond aux besoins humains en riboflavine et acide pantothénique ainsi que pour 30 pour cent des besoins en niacine.
Table 5: Comparaison des valeurs nutritionnelles pour 100 g daliment
Aliments |
Eau |
Protéines |
Matières grasses |
Carbohydrates [g] |
Valeur énergétique [kcal] |
Chenilles fraîches |
81,1 |
10,6 |
2,7 |
4,2 |
86 |
Chenilles sèches |
9,1 |
52,9 |
15,4 |
16,9 |
430 |
Chenilles frites |
20,4 |
62,3 |
4,6 |
6,5 |
333 |
Buf frais semi-gras |
63,1 |
18,2 |
17,7 |
0 |
273 |
Buf séché, salé |
29,4 |
55,4 |
1,5 |
0 |
250 |
Buf cuit |
68,5 |
22,6 |
8,0 |
0 |
172 |
Poisson frais |
73,7 |
18,8 |
2,5 |
0 |
103 |
Poisson séché, salé |
13,8 |
47,3 |
7,4 |
0 |
269 |
Poisson cuit |
82,1 |
16,6 |
0,3 |
0 |
74 |
Sources: Wu Leung et al., 1970.
En raison de leur forte valeur nutritionnelle, dans certaines régions, les chenilles sont mélangées à la farine afin de préparer une bouillie pour lutter contre la malnutrition des enfants. Les espèces qui sont particulièrement riches en protéines (Imbrasia epimethea, Imbrasia dione, Antheua insignata), calcium (Tagoropsis flavinata) ou en fer (Cinabra hyperbius) sont données aux personnes anémiques et aux femmes enceintes à leur petit-déjeuner. Plusieurs autres espèces jouent un rôle important dans les médecines traditionnelles, comme dans la culture chinoise (Chen, Feng, 2002). Cependant, certains insectes peuvent secréter des substances toxiques provenant de plantes dont ils se nourrissent ou quils produisent eux-mêmes (Duffey, 1980). Souvent, ces espèces ont des couleurs qui indiquent ou attirent lattention dune autre manière et elles ne sont pas ramassées.
Selon NGasse (2003), près de 85 pour cent des populations de RCA consomment des chenilles, le taux dans les zones rurales étant légèrement plus élevé que celui des zones urbaines. On trouve ce même chiffre dans dautres pays. Les recherches de Monzambe Mapunzu (2002) en RDC montrent que 70 pour cent des personnes interrogées mangent des chenilles. Zitzmann (1999) le confirme avec le Botswana où 91 pour cent des ménages étudiés récoltent Imbrasia belina dans les forêts de mopane.
En général, les chenilles ne sont pas considérées comme une nourriture de secours mais elles contribuent au régime alimentaire durant certaines saisons. Les données sur la consommation moyenne de chenilles diffèrent selon les régions. NGasse (2003) cite une enquête anonyme sur la forêt de Ngotto qui a établi une consommation denviron 137 g (insectes frais) par personne par jour, entre la mi-juin et la fin septembre; comparé à une consommation de 83 g (insectes séchés) par personne/jour une ou deux fois par semaine durant la saison. Paulin (1963) cite 40 g (insectes fumés) par personne/jour, de novembre à janvier, à Brazzaville. Monzambe Mapunzu (2002) donne le chiffre de 6,12 g (insectes frais) par personne/jour, pour la période de juin à mars, à Kinshasa. Face au total des quantités fournies par les provinces, il estime que la consommation annuelle de chenilles à Kinshasa est de 9 600 tonnes. Ajoutons un fait important qui est que les enfants complètent leur régime alimentaire en récoltant spontanément les jeunes larves alors quils font autre chose en même temps.
Limportance saisonnière des chenilles dans les régimes alimentaires des pays dAfrique centrale est illustrée dans la Figure 1 avec Bangui.
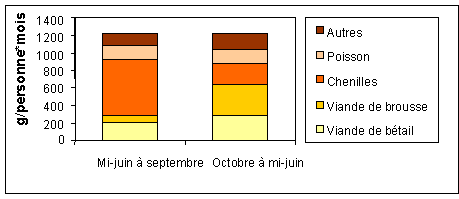
Figure 1: Comparaison des compositions de protéines animales par personne et par mois,
à différentes périodes à Bangui (RCA) (NGasse, 2003)
La Figure 4 montre quà Bangui/RCA, entre mi-juin et fin septembre, les chenilles constituent une proportion importante dapport en protéines animales. Mais, même si on peut imaginer que les chenilles peuvent se substituer à la viande de brousse durant une saison, les insectes ne sont pas considérés comme un produit de substitution à la viande. Les chenilles sont consommées comme un met délicat ou sont un complément au régime alimentaire quotidien selon leur disponibilité saisonnière et les prix du marché. Les prix des chenilles enregistrent de fortes fluctuations sur les marchés locaux et ne sont pas forcément moins élevés que les prix de la viande ou du poisson. Cependant, quand lapprovisionnement en viande de brousse et en poisson diminue lors de la saison des pluies et que les prix du marché augmentent, les populations comptent davantage sur les chenilles et les autres insectes disponibles. Dans certaines régions aussi, il est évident que le gibier est terriblement plus difficile à se procurer du fait de la surexploitation et du braconnage. Limportance des insectes dans lalimentation se fait alors plus forte. Vu la complexité du sujet, il nest pas facile de conclure si et combien de chenilles doivent/peuvent remplacer la viande de brousse. Cependant, certaines populations comme les Yukpa du Venezuela et de la Colombie préfèrent certaines espèces dinsectes à la viande (Ruddle, 1973), ainsi que les Pedi dAmérique du Sud (Quin, 1959).
Selon NGasse (2003), à Bangui, 29 pour cent de la consommation annuelle totale de protéines animales par personne et par an (14,6 kg) est fourni par les chenilles (cf. Figure 4, colonne de gauche). Des chiffres équivalents sont donnés par Gomez et al. (1961) qui estime que les insectes fournissent 10 pour cent des protéines animales annuelles en RC. En regardant au niveau du district, on peut voir que pour quatre des 25 districts congolais, la proportion est de plus de 20 pour cent.
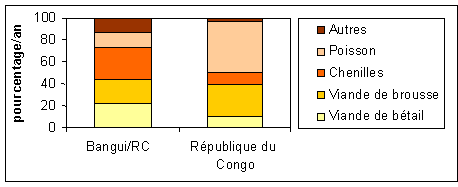
Figure 2:
Comparaison des compositions en protéines animales par an à Bangui/RCA
(NGasse, 2003) et pour la République du Congo (Gomez et al., 1961)
Aspects culturels
Limportance de la consommation des chenilles et les préférences entre espèces dépendent des habitudes alimentaires. En RCA, les populations qui vivent près des forêts préfèrent Imbrasia truncata, Nudaurelia oyemensis et Imbrasia obscura. A Brazzaville, la majorité des vendeurs provient des groupes ethniques Téké, Lari et Mbochi.
Dans certaines cultures, des restrictions traditionnelles existent par rapport à certains modes de consommation. Certains groupes du Cameroun réservent les chenilles pour les dignitaires et les classes sociales les plus élevées. En Chine, des espèces particulières étaient souvent envoyées à lempereur et aux dignitaires des clans, il y a fort longtemps (Chen, Feng, 2002). En RDC, la consommation de chenilles est taboue pour le groupe ethnique Yombe, certaines personnes ayant même peur de les toucher (province du Bas-Congo). Dautres ethnies du pays ne consomment pas certaines espèces de chenilles car elles ont peur des conséquences nocives. Les Luba, par exemple, croient que lespèce Nudaurelia oyemensis transmet des maladies. Chez les Rega, les femmes enceintes ne sont pas autorisées à manger les espèces Misaba; dans la province de lEquateur, les espèces Batikatike et Mpofumi sont taboues pour les femmes et les enfants4. Alors que peu de groupes ethniques du Congo, en général, repoussent les insectes en raison de leur physionomie ou de leur aspect spécifique, les femmes dautres groupes tendent à manger moins de larves que les hommes.
Filière de commercialisation
Il est facile de trouver des insectes à acheter sur les marchés des villages alors que les espèces préférées sont vendues sur les marchés des villes et les restaurants (de Foliart, 1992; Tabuna, 2000). Selon Zitzmann (1999), au Botswana, le commerce dImbrasia belina est présumé comme lactivité commerciale la plus importante au regard des produits du velt5. Dans chacune des études de cas aussi, la commercialisation des chenilles est définie comme une activité saisonnière générant des revenus importants pour les zones rurales et urbaines, notablement pour les femmes.
Seules les chenilles arrivées au stade adulte sont récoltées pour être vendues car elles sont de meilleure qualité. La commercialisation des larves vivantes ou séchées est directe mais se pratique plus fréquemment à travers les grossistes et les revendeurs (Figure 3). Lors de la commercialisation directe, le produit est offert sur le marché local ou dans les rues proches de la zone de récolte. Mais, en général, un ou plusieurs intermédiaires interviennent entre les producteurs (collecteurs) et le consommateur, augmentant nettement les prix. Normalement, les grossistes vont dans les villages pour acheter les larves et les revendre en ville. Certains grossistes les conservent eux-mêmes dans des dépôts en ville afin dêtre approvisionnés plus régulièrement et daugmenter les prix en période de manque.
La commercialisation directe et indirecte est pratiquée de manière très traditionnelle et informelle ce qui facilite les procédures mais comporte des risques dapprovisionnement irréguliers.
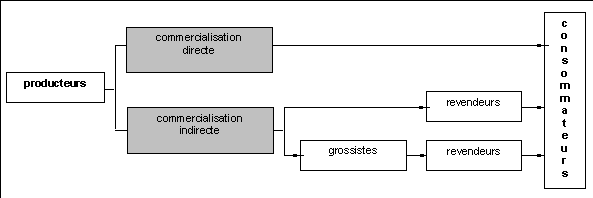
Figure 3: Circuits possibles de commercialisation des chenilles en Afrique centrale
Sur les marchés, les vendeurs sont principalement des femmes et des enfants alors que dans certaines régions seulement, ce sont les hommes qui pratiquent la vente en gros. Pour la majorité des vendeurs de chenilles, ce nest pas la principale activité mais plutôt un supplément qui sajoute aux autres aliments vendus: poisson, noix, manioc ou autres légumes. Cest seulement durant la saison que les vendeurs proposent exclusivement des chenilles au marché. Pour disposer dun stand sur un marché, les communes réclament normalement une taxe. En RCA, cette taxe est de 50 FCFA (0,085 $EU) par jour. Alors que normalement les femmes restent sur leur étal, les enfants se déplacent souvent autour pour vendre et se rendent même dans les autres quartiers.
Les vendeurs sorganisent eux-mêmes parfois en association formelle pour faciliter les activités logistiques comme la location de voitures pour livrer les insectes sur les marchés. Au Zimbabwe, il y a déjà un système de vente formelle bien établi pour la commercialisation dImbrasia belina (Zitzmann, 1999). Souvent, la mauvaise qualité des routes entrave les activités commerciales. Pour fournir en larves des capitales comme Kinshasa et Brazzaville, et dautres petites villes, les voitures (taxi brousse) et le transport par train, bateau et avion sont aussi utilisés.

Taxi brousse transportant des passagers et
des PFNL dont les chenilles
dans
des sacs de toile (NGasse)
Fixation des prix et revenus
Si la plupart des chenilles sont vendues pour de largent comptant, dans certaines régions, elles sont troquées pour de la nourriture, des vêtements, des ustensiles pour le foyer, des cigarettes, de lalcool ou des machettes. Zitzmann (1999) reporte quau Botswana et en RCA, les pygmées pratiquent encore le troc. Habituellement, les pygmées les troquent dans des lieux de commerce informel près de la forêt, dans la soirée. Les acheteurs apporteront les larves en ville puis les commercialiseront.
La fixation des prix dépend des espèces et de la qualité des produits. Pour les chenilles fraîches, le prix peut varier dun jour à lautre selon les procédés employés pour le séchage. Les facteurs qui influencent les prix sont:
les habitudes alimentaires et les espèces préférées par les communautés locales;
la période (exemple: quand les prix augmentent en début et fin de saison);
la distance entre le producteur et le consommateur (transport, stockage, etc.);
le nombre dintermédiaires;
la quantité de chenilles fournie sur le marché;
le site de commercialisation (comme les différents quartiers dune ville).
Un autre fait important est lunité de vente, le prix par kg augmentant lorsque la quantité diminue. La plus petite unité commune est le verre, le bol et la poignée; les plus grosses sont les paniers et les sacs. Voici un exemple pour la RCA:
Tableau 6: Comparaison de prix par kg pour des chenilles séchées selon les unités de vente en cours à Bangui
|
Fournisseur |
Prix pour une vente en petite quantité |
Prix pour la vente en sac de 12 kg | ||
|
[FCFA/kg] |
[$EU/kg] |
[FCFA/kg] |
[$EU/kg] | |
|
Producteur |
1 000 |
1,7 |
1 000 |
1,7 |
|
Grossiste |
1 500 |
2,55 |
1 333 |
2,27 |
|
Revendeur |
1 800 |
3,06 |
1 583 |
2,69 |
Source: NGasse, 2003.
Dans plusieurs publications commerciales sur les chenilles, cette activité est présentée comme générant dimportants revenus (Latham, 1999; de Foliart, 1992; Merle, 1958). NGasse (2003) analyse le revenu dun grossiste durant la bonne saison (cf. Tableau 7). Ce grossiste achète et vend 24 kg de chenilles par jour durant 3 mois par an (tous les 26 jours).
Tableau 7: Bénéfices dun grossiste commercialisant des chenilles en RCA
|
FCFA |
$EU | ||
|
Prix dachat par kg |
1 000 |
1,7 | |
|
Prix dachat par jour (24 kg par jour) |
24 000 |
40,8 | |
|
Dépenses additionnelles (transport, taxes, etc.) par jour |
2 500 |
4,25 | |
|
Dépenses totales par jour |
27 500 |
46,75 | |
|
Prix de vente par kg |
1 333 |
2,27 | |
|
Revenus par jour (24 kg par jour) |
32 000 |
54,4 | |
|
Bénéfices |
Par jour |
4 500 |
7,65 |
|
Par mois (26 jours par mois) |
117 000 |
198,9 | |
|
Par an (3 mois par an) |
351 000 |
596,7 | |
Source: NGasse, 2003.
Pour une évaluation de la contribution du commerce des chenilles pour lensemble des revenus des foyers durant une saison ou sur une année, des études comparées plus fouillées sont nécessaires sur dautres insectes (comme les termites) et sur dautres activités générant des revenus. De plus, des études sur la façon dont les bénéfices de la commercialisation des insectes sont redistribués auprès des producteurs, grossistes et revendeurs sont nécessaires. Il semble que les filières commerciales existantes avantagent nettement les grossistes.

Commerçantes proposant différents types de chenilles en même temps que des fruits (NGasse)
Zitzmann (1999) a réalisé une étude détaillée des stratégies de survie au Botswana qui permet lestimation suivante pour les ménages étudiés: les revenus de la vente dImbrasia belina représentent 13 pour cent du total des revenus en nature des ménages sur une année6. Les heures de travail pour cette activité représentent seulement 5,7 pour cent de toutes les activités générant un revenu. Zitzmann compare finalement les marges brutes par heure de travail: la vente dImbrasia belina est en troisième position après la vente de pieux en bois et du bétail et cela avec une importance primordiale pour les conditions dexistence des familles. Un exemple, en Zambie, indique que le revenu annuel tiré de la commercialisation des chenilles est comparable ou est même plus important que la vente des récoltes (Chidumayo, Mbata, 2002).
Exportation
Il existe aussi un important commerce transfrontalier des insectes comestibles dans tous les pays dAfrique centrale7, avec le Soudan et le Nigéria et à petite échelle, ils sont aussi exportés vers la France et la Belgique. Dans les aéroports ou les villes frontalières, les pays exportateurs peuvent collecter des taxes. En RCA, le Service phytosanitaire collecte 2 000 FCFA (3,4 $EU) par lot expédié dun poids de 20 kg (NGasse, 2003). Peu de chiffres précis sur lexportation sont disponibles. Selon une enquête réalisée par Tabuna (2000), la France et la Belgique importent annuellement, respectivement, environ 5 tonnes et 3 tonnes dImbrasia sp. sèches de la RDC. Dans le cas de la Belgique, la quantité importée est évaluée à 41 500 $EU, correspondant à un prix moyen de 13,83 $EU par kg.
Impact de la défoliation sur les plantes hôtes
Plusieurs chenilles sont connues pour défolier les arbres lorsquelles se développent au début de la saison des pluies en se nourrissant de feuilles fraîches. Les forestiers considèrent donc souvent les chenilles comme des ravageurs, alors que les populations locales voient certaines dentre elles comme de la nourriture. La défoliation ralentit la croissance temporairement mais les arbres y répondent habituellement en produisant une autre série de feuilles (Reeler et al., 1991). Malgré tout, après plusieurs attaques, les arbres peuvent perdre leur vitalité et ne plus se régénérer. NGasse (2003) observe que les attaques dinsectes, si elles sont irrégulières, génèrent des affaiblissements qui endommagent seulement les plantes hôtes des zones de forêt dense humide; et que ces invasions de chenilles qui dévorent les feuilles nont pas été observées fréquemment ou sur une zone importante. Lutilisation de produits chimiques pour contrôler les pullulations de chenilles dans ces forêts nexiste pas, les récoltes dinsectes de la forêt ne comportent donc aucun risque dimpact chimique. Mais les chenilles ont-elles un impact négatif quand elles se nourrissent des cultures? Dans la région, le contrôle des chenilles en tant que ravageur est habituellement pratiqué en répandant de grandes quantités de pesticides, tuant les insectes et les rendant impropres à la consommation.
Dounias (1999) montre les effets positifs de la récolte des parasites. Un exemple caractéristique est labondance dAugosoma centaurus et de Rhynchophorus phoenicis sur Raphia sese et Elaeis guineensis. Même si ces plantes sont souvent fortement endommagées, les récoltes extensives de larves contribuent à maintenir la reproduction naturelle. La question est souvent posée de savoir comment une récolte plus importante dinsectes comestibles pourrait constituer une forme de contrôle biologique des ravageurs. Cette pratique pouvant aussi entraîner la diminution de lutilisation des pesticides ainsi que la création de nouvelles opportunités économiques pour les populations locales (de Foliart, 1990).
Impacts des récoltes sur les ressources forestières
La récolte des chenilles est souvent pratiquée dune manière non destructive avec le ramassage manuel. Cependant, dans certains cas, labattage des arbres hôtes est largement répandu. En Zambie, 2 ha de forêt ont été défrichés les années où les chenilles étaient abondantes (Lees, 1962). La pratique de couper les grosses branches est un grave problème qui conduit à la destruction des arbres lors des abattages qui suivent. De cette manière, la récolte des chenilles peut contribuer à la dégradation de la forêt ou à la déforestation. En Zambie, du fait des dommages causés par les collecteurs de chenilles qui coupent les branches et abattent les arbres, les forestiers considèrent les chenilles comme un parasite qui provoque des ravages sur la forêt (Holden, 1991).
Impacts de la déforestation sur les populations de chenilles
Dans les études de cas, il est montré que les récoltes prolongées de chenilles ne semblent pas affecter négativement leur capacité de reproduction. Pourtant, on peut penser que la disparition des arbres hôtes peut sur le long terme être suivie dune diminution progressive de la présence de ces insectes, particulièrement ceux qui proviennent de plantes hôtes spécifiques. Trois espèces darbre sont menacées par les techniques de récoltes dinsectes destructrices ou les exploitations sélectives. Tel est le cas des espèces forestières à forte valeur comme le sapelli (Entandrophragma angolense). Selon les recherches de Chidumayo et Mbata (2002), les exploitations sélectives sont particulièrement destructives pour des écosystèmes vulnérables spécifiques comme les espèces darbres qui ne se régénèrent pas avec le recrutement de jeunes plants.
Les activités qui dégradent la forêt en général mettent en danger lexistence des populations dinsectes. Le problème des feux de brousse doit être pris en compte très sérieusement du fait de ses conséquences à la fois sur les habitats et les populations dinsectes. Dans la région, les feux sont pratiqués pour diverses raisons mais, le plus souvent, pour étendre les cultures permanentes et sur les cultures itinérantes. La pratique des feux pour chasser le gibier et plus fréquemment, pour attraper les petits rats de brousse communs a un impact négatif notable sur lhabitat forestier. Cela peut avoir pour résultat la réduction des possibilités de survie des chenilles comestibles les plus appréciées, alors quen même temps, dautres populations dinsectes peuvent proliférer (par exemple, les coléoptères non comestibles). Comme les insectes constituent un des maillons de la chaîne alimentaire de plusieurs oiseaux et dautres petits animaux chassés pour la viande de brousse, une disponibilité moindre dinsectes peut finalement affecter aussi les stocks de leurs prédateurs. La perte de biodiversité consécutive affecte loffre alimentaire et les conditions dexistence des populations locales mais aussi la fructification potentielle des plantes par diminution de leur pollinisateur.
Un aspect très intéressant de la récolte des chenilles est son impact positif sur la fréquence des feux de brousse quHolden (1991) a suivi en Zambie. Il note quil y a encore très peu de temps8, les feux dans les régions où les villageois récoltaient des chenilles, permettaient de protéger les insectes. Il propose donc une recherche sur les chenilles, pas seulement parce quelles sont importantes au niveau alimentaire, mais aussi pour leur impact positif sur la gestion des forêts. Leleup et Daems (1969) qui ont aussi étudié les périodes de feux de brousse en relation à la présence saisonnière des différents stades de vie (uf, larve, etc.) de trois espèces de chenilles comestibles de la RDC, font plusieurs recommandations sur les durées optimales pour prescrire les feux de forêt.
Indirectement, la déforestation peut, sur le court terme, altérer les microclimats locaux et sur le long terme, contribuer aux changements climatiques, interrompant le cycle de vie des insectes. Par exemple, Holden (1991) mentionne les sécheresses comme un premier symptôme parmi les autres impacts négatifs tels que la disparition des plantes hôtes et des espèces comestibles correspondantes, et/ou associées à une invasion et une prolifération dautres espèces (non comestibles).
1.1.8. Recommandations1. Même si la sensibilisation a augmenté, des recherches devraient être réalisées sur le potentiel biologique des insectes comestibles de la forêt dune façon pluridisciplinaire et pratique en incluant la conservation, lexploitation des forêts, lagriculture, la nutrition et les aspects de transformation. Ainsi: a. De nombreuses espèces ne sont pas encore identifiées au niveau taxonomique et les connaissances sur les cycles de vie, les plantes hôtes, leur abondance selon les différents habitats, etc., sont fragmentaires. Un inventaire détaillé des ressources naturelles de base et des relations entre les chenilles et les plantes hôtes devrait être un des domaines prioritaires de recherche. Les populations locales devraient être associées afin de pouvoir y contribuer grâce à leurs connaissances traditionnelles. b. Un autre point primordial dans le domaine de la nutrition est lanalyse des risques cancérigènes que comporte la consommation de chenilles fumées et par suite, lamélioration des techniques de conservation. c. La recherche au niveau de la transformation et la conservation des chenilles est primordiale. La valeur ajoutée devrait pouvoir offrir de nouvelles opportunités pour lexportation. Les expériences du Botswana et du Zimbabwe (Imbrasia belina) pourraient servir de base de réflexion. 2. Les insectes comestibles et leur commercialisation contribuent de manière significative aux moyens dexistence des populations pauvres et des groupes les plus désavantagés de la région. La recherche et les actions de soutien doivent inclure: a. Une analyse socioéconomique détaillée au niveau des familles pour évaluer la contribution des insectes à la sécurité alimentaire, incluant la notion de subsistance ainsi que la génération de revenus. Lanalyse doit être intégrée à différentes catégories de ménages impliquées dans la commercialisation des insectes: les producteurs, les grossistes et les revendeurs. b. Pour améliorer les revenus provenant de la commercialisation des insectes ainsi que les moyens dexistence des plus pauvres, les filières commerciales et la redistribution des bénéfices doivent être analysées. Limpact sur les femmes est important du fait quelles sont les principales actrices qui gèrent la transformation et la commercialisation des chenilles; les associations féminines de productrices et de commercialisation doivent être soutenues pour améliorer leur accès au marché et leurs profits. 3. Même si davantage dinformations détaillées et valides sur les ressources naturelles de base, les marchés et les parties prenantes sont disponibles, il faut surtout évaluer comment une meilleure production dinsectes peut être intégrée à des plans de gestion des ressources naturelles et de conservation des forêts. a. Comment intégrer la production et la récolte de chenilles dans un plan de gestion des forêts, de lagroforesterie et de lutilisation des terres, comme par exemple optimiser les rendements et assurer des niveaux de récoltes et de techniques durables, avec des risques peu élevés pour les cultures avoisinantes. Un très bel exemple deffort pour améliorer la production de larves au sein dun système foncier intégré est la recherche de Chidumayo (1997) et de Holden (1991) qui pensent que la récolte des chenilles a un impact positif sur la réduction des feux de brousse. b. Un domaine très important de la recherche est la domestication des espèces dinsectes forestiers et des plantes hôtes qui doivent être pris en compte dans une gestion intégrée de lutilisation des terres, devant même soutenir les efforts de reforestation. Il faut identifier les systèmes agroforestiers et les types dexploitation adaptés; sélectionner de manière appropriée les insectes et plantes hôtes, les méthodes de multiplication végétale et les conditions permettant daugmenter les rendements de production avec peu de risques pour les cultures. c. Le développement de ce système de gestion forestière se basera aussi sur une analyse des systèmes fonciers et de laccès aux forêts avec leurs cadres institutionnels correspondants et les réglementations concernant la gestion des conflits entre les différents groupes dutilisateurs dune concession forestière, comme les populations locales, les chenilles garde-buf et les exploitants de bois. d. Les utilisateurs de la forêt doivent être sensibilisés afin de mieux comprendre les processus écologiques et les liens entre la récolte des insectes et lécosystème forestier au moyen de programmes déducation et de vulgarisation. Une meilleure reconnaissance des impacts négatifs de la déforestation et des feux de brousse sur lapprovisionnement en chenilles et particulièrement de labattage des arbres pratiqué pour récolter les chenilles, devrait mobiliser les populations afin quelles adoptent dautres techniques pour la collecte des insectes. |
Edible insects are a deliberate part of the diet in different cultures. This synthesis focuses on caterpillars and it analyses examples from four Central African countries based on four case studies by local experts.
The paper provides some information on the natural resource base (such as the taxonomical identification of insect and host plant species), the abundance of caterpillars in their habitats and management of the resource. More detailed information is provided in terms of harvesting techniques, including gathering caterpillars by hands and collection through tree-cutting; post-harvest handling, including storage and preservation methods; and food preparation. The seasonal availability of the insects, which varies in different regions, is outlined.
The majority of households covered by the case studies consume caterpillars. The insects have a high nutritional value and are a main source of protein in the local diets of Central Africa. Examples of consumption patterns are given, referencing both alternate sources of protein such as bushmeat and culturally-driven habits.
Trade in insects, although seasonal, does provide additional income for rural as well as urban people and particularly benefits women. The paper provides an overview of market chains and relevant income-generating activities while providing some export figures.
In addition, linkages between insect populations and forests (as their natural habitat) are outlined. These include the significant impact of forest logging, bushfires and other forms of forest degradation on insect populations.
Finally, research gaps are identified and recommendations given as to how best edible insects can contribute to improving local livelihoods and how to best incorporate caterpillar production in natural resource management and forest conservation.
The study distinguishes between caterpillars and grubs (as defined in Table 1):
Table 1: Terminology: caterpillars and grubs
|
Term |
Definition |
|
Caterpillars |
Caterpillars are the larvae of Lepidoptera, i.e. of butterflies and moths. They mainly feed on leaves and other parts of trees, shrubs or other plants. |
|
Grubs |
Grubs are the larvae of Coleoptera, i.e. beetles. These larvae develop under tree bark, in palm trunks or in soil. |
The four country case studies were carried out by local experts between October 2002 and March 2003:
NGasse, Georges (2003): Contribution des chenilles/larves comestibles à la réduction de linsécurité alimentaire en République Centrafricaine;
Balinga, Michel Philippe (2003): Les chenilles et larves comestibles dans la zone forestière du Cameroun;
Moussa, Jean-Baptiste (2002): Les chenilles comestibles du Congo: Intérêt alimentaire et circuits de commercialization: Cas de Brazzaville;
Monzambe Mapunzu, Paul (2002): Contribution de lexploitation des chenilles et autres larves comestibles dans la lutte contre linsécurité alimentaire et la pauvreté en République démocratique du Congo.
For data collection, the researchers prepared several questionnaires appropriate for consumers, various merchants and other target groups. Balinga (2003) also analysed secondary literature while NGasse (2003) conducted informational interviews with key persons. Table 2 provides an overview of the study areas and the number of participants within the appropriate target groups.
Table 2: Case studies: Study areas and numbers of respondents
|
NGasse (2003) |
Balinga (2003) |
Moussa (2002) |
Monzambe Mapunzu (2002) | |
|
Number of households |
100 in the Ngotto forest |
180 in the Central Province, 20 in the East, 130 in the West, 90 in the Northwest, 174 in the Southwest and 96 in the Littoral Province |
251 total in school establishments, goods stations and markets in Brazzaville |
600 in Kinshasa |
|
Number of merchants |
100 in Bangui and 12 each in 11 other cities in a 400 km circumference of Bangui |
9 in Yaoundé |
45 wholesalers and 300 retailers in Kinshasa |
Synthesis
The synthesis consolidates key information gathered from the four case studies. Country- and/or regionally-specific data or phenomena are cited with reference to the appropriate country and author. In addition, references are made to secondary documentation to highlight pertinent information relating to other regions or to refer to previous experiences gained.
During the analysis of the case studies, some questions were raised that need to be further clarified. The authors were contacted and any complementing information provided by them has been included in the synthesis. Additionally, discussions with several entomologists and experts (specifically in reference to bushmeat consumption in CAR) contributed to better understanding and provided valuable information for this paper. Furthermore, an article was published on the subject in the ODI9 Wildlife Policy Briefing Series nº 3 (Vantomme, et al., 2004).
In the case studies, monetary data was cited in the regional currency, i.e. Franc de la Communauté Française-Africaine (FCFA). For clarity and comparability, the synthesis also indicates figures in US Dollars (US$) based on the following exchange rate (FAO 2003): 1 FCFA = US$0.0017 or US$1 = 604.792 FCFA.
Taxonomic identification of insect species
According to De Foliart (2002), the precise taxonomic identification of the variety of edible insects is known for 128 species in Central and East Africa. Another 21 edible insects are identified up to the genus, 12 up to the family and one up to the order. A list of taxonomically-identified caterpillar and grub species10 mentioned in the case studies (including host plants) is enclosed in Annex. Annexes provide broader country-specific information on the natural resource base, including vernacular names. The most extensive listing is provided by Monzabe Mapunzu (2002). Further research is needed because numerous caterpillar and grub species are not yet taxonomically identified (and are only recognized by local populations).
Corresponding to the habitats of host plants, larvae occur in different types of forests as well as in tree and shrub savannahs. NGasse (2003) investigated the abundance of Nudaurelia oyemensis on its host plant Entandrophragma angolense (Sapelli) over a seven years period: from 1995 to 2001. He determined that on average one host tree was occupied by 3.3 kg (dry matter) caterpillars. He also cited a survey of Serge Bahuchet11 (who investigated from 1960 to 1970) determining an abundance of 2 kg (dry matter) edible caterpillars per hectare (ha) in the biosphere reserve, Basse Lobaye. Other investigations indicated higher levels; for example, Latham (2002) analysed an abundance of 5 kg (dry matter) Cirina forda per ha in the Bas-Congo province (DRC) and Munthali, Mughogho (1992) indicated 14.63 kg (dry matter) of edible caterpillars per ha in Malawi.
The presence of caterpillars is detected in different ways. The smell of accumulating frass, the deformation of leaves and the aggregation of caterpillars themselves are all noticeable. The existence of grubs developing in palm trunks (e.g. Augosoma centaurus, Rhynchophorus phoenicis) might also be perceived by characteristic noises.
In the Central African region, there are two principle harvesting techniques. One technique is to pick caterpillars by hand from the ground, trunks, branches and leaves. Mainly women and children (when not attending school) are involved in the activity. Their collection is facilitated as caterpillars, once mature, descend from trees. In fact, some species form processions (e.g. Imbrasia ertli) and in these cases, buckets are fixed at the base of the tree trunks to collect the insects within five or six days.
Another harvesting technique is to chop down the trees occupied by caterpillars or cut entire branches off trees. This is done either to be efficient or to keep the larvae in good condition in order to sell them alive. Gatherers also strike tree trunks with heavy objects (such as hammers) to shake caterpillars from higher parts of medium-sized trees. A long piece of bamboo, is also used to reach the canopy of tall trees. The Pygmies of CAR are very accustomed to climbing trees to harvest several forest products, including caterpillars (Bahuchet, 1990).
In the case of grubs developing in palms trunks, the palms are cut and split. The grubs are extracted either alive or after having sun-dried together with the palm trunk for a short period. Also, palms cut for wine production supply grubs as a by-product. Unlike gathering, tree- and palm-cutting is a male-dominated activity.
In the case study from CMF, the interviewed households only practised gathering. In DRC, 65 percent of respondents who were questioned about the three most important caterpillar species chopped down trees. According to NGasse (2003), in CAR, some families temporarily move closer to forest areas during the gathering period (for two or three months). They build temporary huts and little wooden grates for smoking the insects. As Latham (2002) observed, collectors in Bas-Congo frequently transfer young caterpillars from original host plants to trees nearer to their village.
Gathering caterpillars is a seasonal activity as opposed to the year-round harvesting of grubs. The collection period takes place during the rainy season, as it related to the natural life cycle of caterpillars (see Malaisse, 1997), Owing to diverse climatic conditions, the availability of caterpillars can vary substantially between different regions within a country (Table 3). Although the rains do hinder harvesting activities (and particularly the storage of caterpillars), fish and game are even more difficult to catch during the rainy season.
Table 3: Availability of caterpillars in Central African countries
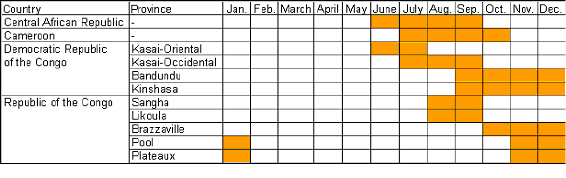
The seasonal availability of caterpillars affects rural gathering households more than urban households because many urban markets are supplied insects from different provinces for most of the year. For example, in Kinshasa caterpillars are available at least seven months of the year.
In the four case studies, little is said of the management of caterpillar and grub production and if or how it is incorporated in the management of forests and other natural resources.
Balinga (2003) mentioned that the size of grubs developing in the trunks of oil palms is rather insignificant. In contrast, species developing in trunks of raphia palms are more prolific and of better quality, and therefore collected for commercial purposes. To support the reproduction of grub species that feed on dead, organic material (e.g. Rhynchophorus phoenicis), palms are frequently cut down to initiate the decomposition process followed by a two to three week period before grub extraction is feasible.
In CAR, present forest concession rules do require at least one seed tree of Entandrophragma angolense (Sapelli) in every ten hectares. This law, driven by silvicultural motives for timber production, was enacted to allow natural regeneration of the species. However, no consideration was given to the fact that local people gather caterpillar species feeding on Sapelli leaves (e.g. Nudaurelia oyemensis) for personal consumption. It is obvious, even if this rule were respected, leaving only one seed tree in every ten hectares would significantly reduce the caterpillar supply. In addition, in the Lobaye forest of CAR, NGasse (2003) found that cutting host trees for caterpillar harvesting considerably reduced the population of young Sapelli trees.
Monzambe Mapunzu (2002) reported on some experiences in terms of the domestication of caterpillar and host plants species. In the Bas-Congo province, domestication experiments provided encouraging results and at the same time have pointed out research gaps. For instance, further research is necessary in the field of vegetal material reproduction. The following host plant species were identified as having good prospects: Acacia auriculiformis, Antidesma membranaceum, Bridelia ripicola, Bridelia micrantha, Hymenocardia ulmoides and Chlorophora excelsa.
Efforts in the domestication of host trees should correspond with efforts to enhance agroforestry systems in general. The cultivation of crops within agroforestry plantings should be driven by demands on target markets. Plantings should be in close proximity to the gatherers villages, to increase efficiency.
Latham (1999) and Chidumayo (1997) investigated the presence of caterpillars on forest fallow land. Latham determined that traditional shifting cultivation systems included fallow periods from seven to fourteen years. This period of regeneration allows a wide range of plants in the area, in particular wooden species, to recover and provide habitats for various caterpillar species simultaneously. As a result of population increase, the land is often re-cultivated after two or three years, resulting in low yields and the gradual loss of biodiversity. Latham recommended assisting farmers to re-establish multiple strategies for optimizing forest fallow.
Chidumayo (1997) determined that the caterpillar species Gynanisa maja and Gonimbrasia zambesina were more widespread (and potentially more plentiful) in young re-growth miombo woodland on shifting cultivation fallow than in old-growth stands of a forest reserve. He concluded that re-growths on fallow land may provide more favourable habitats for the two caterpillar species. One reason for this might be the higher prevalence and density of the caterpillars host tree, Julbernardia paniculata, in re-growths. In old-growth miombo woodland (under selective cutting during caterpillar harvesting), Julbernardia paniculata mortality was higher (Chidumayo, Mbata, 2002) and regeneration through recruitment from stunted saplings seemed to be suppressed by shading from uncut trees.
As a result of these findings, Chidumayo, Mbata (2002) suggested zoning the forest reserve to dedicate certain areas to caterpillar production. Such an approach could ensure that local people benefit from the forest reserve in addition to potentially reducing illegal activities in the proposed zones. Their study shows that detailed knowledge of natural processes in different ecosystems is necessary to establish forest management systems.
The case studies also provide some information on tenure rights and the legislation framework. According to Latham (2002), in Zimbabwe, local people and external developers come into conflict with each other. The European Commission (EC) and FAO (2001) report on similar conflicts in Namibia. The government there supported interventions to transfer user rights to local communities through the Communal Areas Management Programme for Indigenous Resources (CAMPFIRE).
Caterpillars can only be stored alive for a very short time. They can survive for two or three days when wrapped inside leaves and watered occasionally. In CMF, Xanthosoma sagittifolium (Macabo tree) leaves are generally used for storage.
Balinga (2003) describes the natural conservation of fresh caterpillars in Cameroon as follows: a large aggregation of caterpillars will establish a type of carapace allowing them to survive for a few months. Detailed information about which species and their processing is not given.
Preservation by sun-drying and smoking
Sun-drying and smoking caterpillars are the most common methods of preservation; after which the dried larvae are stored and transported in big baskets or sacks.
To sun-dry larvae (on wooden grates, blank sheets or mats) a significant period of sun exposure is required. Cleaning the caterpillars precedes the sun-drying process. Often, caterpillars are cooked in advance to support purging and hair loss. Otherwise, at least the abdomen is removed (which is essential for species that feed on toxic plants such as Lobobunaea phaedusa).
The sun-drying method is practised less frequently than the smoking method because it diminishes the caterpillars durability. Smoking allows for storage of up to three months and methods vary slightly in different regions. Frequently, the caterpillars are smoked after having cooked for 30 to 45 minutes in salted or unsalted water and exposed to one or two days of sunlight. Alternatively, caterpillars can be dried in/on an oven before smoking. The actual smoking is done by spreading the insects on a wooden or other kind of grate that is installed over a fireplace at a low height.
To avoid fragility of the larvae, the smoking process should not exceed one to two days. Another method, particularly practised with thickly-haired species like Cirina forda, is to temporarily deposit the larvae directly into glowing coal. The heat supports depilation and elimination of frass. Sun-drying for two or three days should follow the roasting. In other regions, after having purged the abdomen, caterpillars are perforated with a metal pole or bamboo to roast them directly in fire. This method is only adequate for short-term durability of a maximum of two weeks.
The colour of smoked larvae turns to brown and the taste changes because pyroligneous acid is released during wood combustion (Laurent, 1981). According to NGasse (2003), smoking also decreases nutritional values. More critically, the procedure of fumigation can be carcinogenic.
In general, insects are consumed in all stages of their development (eggs, larvae, adults, etc.). Some 80 percent of insects are eaten in early stages before reaching maturity (Ramos-Elorduy, 1996).
Caterpillars are a standard ingredient in local food preparation. They are primarily eaten as side dishes or sometimes as snacks. To prepare fresh larvae, they are purged, washed and cooked (either fried or grilled in a variety of ways). One might prepare the caterpillars in water or oil (preferably palm oil), while adding different combinations of spices (salt, pimento, etc.) or other ingredients such as groundnut paste. Often they are then mixed with sauce, fish, meat and/or vegetables such as manioc, mushrooms, Gnetum africanum, Gnetum buchholzianum, etc. Lightly-haired species usually lose their hair during cooking. In contrast, preparation of a thickly-coated species (such as Anaphe sp.) requires their deposition into glowing coal beforehand. Preparation of dried/smoked larvae is analogous to that of fresh (previously purged and depilated) larvae.
Malaisse (1997) provided a good overview regarding the nutritional value of various caterpillar species, confirming in scientific terms the empirical knowledge of local people. The average proportion of proteins and fat as well as the average energy value of 24 fresh caterpillar species are listed below (based on dry matter).
Table 4: Proportion of proteins of frech caterpillars
|
Value | |
|
Proteins |
63.5 ± 9.0 % |
|
Fat |
15.7 ± 6.3 % |
|
Energy value |
457 ± 32 kcal/100 g |
In comparison with beef and fish, the insects high proportion of proteins, fat and thus their high energy value is very impressive. Insect proteins tend to be low in specific amino acids such as methionine and cysteine, and very high in others, particularly lysine and threonine (De Foliart, 1992). The indigestibility of chitin makes insects, as a source of protein, of somewhat lower quality than vertebrate animal products (Dreyer, Wehmeyer, 1982) however.
Depending on the species, caterpillars are rich in different minerals (K, Ca, Mg, Zn, P and Fe) and/or vitamins (thiamine/B1, riboflavin/B2, pyridoxine/B6, pantothenic acid and niacin). Research shows that 100 grams of cooked insects provide more than 100 percent of the daily requirements of the respective contained vitamins/minerals (De Foliart, 1992). Malaisse (1997) reveals that the daily consumption of 50 grams dried caterpillars meets the human needs of riboflavin and pantothenic acid as well as 30 percent of the need for niacin.
|
Foods |
Moisture |
Proteins |
Fat |
Crbohydrates [g] |
Energy value [kcal] |
|
Fresh caterpillars |
81.1 |
10.6 |
2.7 |
4.2 |
86 |
|
Dried caterpillars |
9.1 |
52.9 |
15.4 |
16.9 |
430 |
|
Fried caterpillars |
20.4 |
62.3 |
4.6 |
6.5 |
333 |
|
Fresh, semi-boiled beef |
63.1 |
18.2 |
17.7 |
0 |
273 |
|
Dried, salted beef |
29.4 |
55.4 |
1.5 |
0 |
250 |
|
Cooked beef |
68.5 |
22.6 |
8.0 |
0 |
172 |
|
Fresh fish |
73.7 |
18.8 |
2.5 |
0 |
103 |
|
Dried, salted fish |
13.8 |
47.3 |
7.4 |
0 |
269 |
|
Cooked fish |
82.1 |
16.6 |
0.3 |
0 |
74 |
Source: Wu Leung, et al. 1970.
Due to the high nutritional value, in some regions flour made from caterpillars is mixed to prepare pulp given to children to counter malnutrition. Species particularly rich in protein (e.g. Imbrasia epimethea, Imbrasia dione, Antheua insignata), calcium (e.g. Tagoropsis flavinata) or iron (e.g. Cinabra hyperbius) are given to anaemic people or to pregnant and breastfeeding women. Several other species play an important role in traditional medicine, as in Chinese culture (Chen, Feng, 2002). However, some insects do secrete toxic chemicals from food plants or produce toxins themselves (Duffey, 1980). Often these species have alarming colours or attract attention in other ways, in effect warning people not to collect them.
Characteristics of consumption
According to NGasse (2003), approximately 85 percent of the population in CAR consumes caterpillars (with a slightly higher consumption rate in rural areas than urban areas). The investigations of Monzambe Mapunzu (2002) in DRC show 70 percent of respondents ate caterpillars. Zitzmann (1999) determined that in Botswana, 91 percent of the studied households collected Imbrasia belina in mopane woodlands.
In general, caterpillars are not considered an emergency food, but rather, as an intended part of the diet in the appropriate season. Data on the average consumption of caterpillars varies in different regions. NGasse (2003) cited an anonymous survey carried out in the Ngotto forest stating a consumption of approximately 137 g (fresh) per person per day between mid-June and the end of September; compared with a consumption of 83 g (dried) per person per day once or twice a week after the caterpillar season. Paulin (1963) quoted 40 g (smoked) per person per day from November to January in Brazzaville. Monzambe Mapunzu (2002) indicated 6.12 g (dried) per person per day from June to March in Kinshasa. Gathering from the quantities delivered by the provinces, he estimates the total annual consumption of caterpillars in Kinshasa to be some 9 600 tonnes Beyond these figures, it is important to note that children complement their diets by spontaneously gathering (and consuming) small larvae while pursuing other activities.
Figure 4: Seasonal importance of caterpillars to the diet in Central African countries Comparison of the composition of animal proteins consumed per person per month in different periods in Bangui (CAR) (NGasse, 2003)
The figure shows that in Bangui (CAR), in the period from mid-June until the end of September caterpillars represent a substantial protein source. Even though might lead to the assumption that caterpillars substitute bushmeat in the appropriate season, in principle, insects should not be considered such a substitute. Caterpillars are consumed as a delicacy and they are included in the daily diet according to seasonal availability and market prices.
Prices of caterpillars fluctuate significantly at local markets and are not necessarily cheaper then bushmeat or fish. However, when bushmeat and fish supplies decline in the rainy season and their market prices rise, people rely more on caterpillars and other available insects. In some regions there is evidence that game is increasingly more difficult to purchase because of overexploitation and poaching. Therefore, the importance of insects as food may increase.
In view of the complexity of the topic, it is not easy to quantify if and how much do/can caterpillars replace bushmeat. However, some peoples such as the Yukpa of Venezuela and Colombia do prefer certain insect species to meat (Ruddle, 1973), as do the Pedi of South America (Quin, 1959).
According to NGasse (2003), in Bangui, 29 percent of the total annual consumption of animal proteins per person and year (14.6 kg) is provided by caterpillars (Figure 5, left column). A comparative figure was given by Gomez, et al. (1961) who estimated that insects provide ten percent of the annual animal proteins supply in RC and in four of the 25 Congolese districts, the proportion is more than 20 percent.
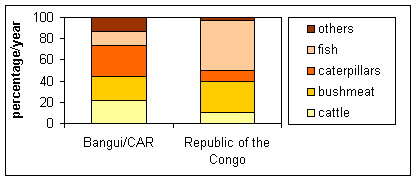
Figure 5: Comparison of the composition of
animal proteins per year in Bangui
(NGasse, 2003) and RC (Gomez, et
al. 1961)
The prevalence of caterpillar consumption and species preferences depend on culinary traditions. In CAR, for example, people living close to forests prefer (amongst others) Imbrasia truncata, Nudaurelia oyemensis and Imbrasia obscura.
In some cultures traditional restrictions on consumption patterns exist. Some Cameroonian tribes withhold caterpillars for dignitaries or wealthier social classes. Historically, in China, specific species were sent to the king and to respectable persons as tributes (Chen, Feng 2002). In DRC, the consumption of caterpillars is taboo for the ethnic group, Yombe, (Bas-Congo). Some individuals of this ethnicity do not dare touch the insects. Other ethnicities within the country do not consume certain caterpillar species. The Luba, for example, believe that the species Nudaurelia oyemensis transfers disease. In the Rega tribe, pregnant women are not allowed to eat the species Misaba and in the Equateur province, the species Batikatike and Mpofumi are taboo for women and children12. While a few Congolian ethnic groups dislike insects because of morphology or specific beliefs, women of other ethnicities tend to eat fewer larvae than men.
Insects are widely available in local village markets, while some of the favourite species do reach urban markets and restaurants (De Foliart, 1992; Tabuna, 2000). According to Zitzmann (1999), in Botswana the commerce of Imbrasia belina is assumed to be the largest commercial activity in regard to velt13 products. Each of the four case studies clearly indicates that the commercialization of caterpillars is a significant seasonal income-generating activity in rural and urban areas, notably for women.
Only full-grown caterpillars are marketed, as they are of better quality. The commercialization of living or dried larvae is most frequently conducted through wholesalers and retailers. When realizing direct commercialization, the product is offered in the local market or along nearby streets. In general, however, one or more intermediaries act between producer (gatherer) and consumer. Customarily, merchants go to rural villages to purchase larvae for resale in cities (where prices are increased significantly). Some wholesalers own storage depots in town to provide more regular supplies and to fulfil demand (at higher prices) in times of shortage.

Transport of edible caterpillars (NGasse)
Direct as well as indirect commercialization is practised in a very traditional, informal and functional way, but one that does not account for the risk of irregular supply.
Sellers at the markets are primarily women and children; only in a few regions do men deal in gross quantity. It should be emphasized that for the majority of merchants, the marketing of caterpillars is not their main activity, but supplements their sale of other foodstuffs such as fish, nuts, manioc or other vegetables. Only during peak seasons might traders exclusively market caterpillars.
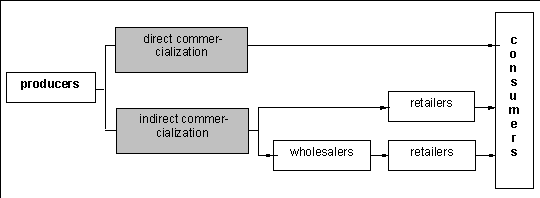
Figure 6: Possible chains of custody for commercialization of caterpillars in Central Africa
To install a stand in the market place, communes normally demand a tax. In CAR, this tax is 50 FCFA (US$0.085) a day. While women normally manage stands, children often walk around to make sales, even visiting neighbourhoods.
Merchants may occasionally organize themselves in formal associations to facilitate logistic activities like renting a motor vehicle for transporting insects to markets. In Zimbabwe, there is already a well-established marketing system for the commercialization of Imbrasia belina (Zitzmann, 1999). Markedly, trade activities are hindered by poor road conditions. To provide Kinshasa and Brazzaville and other big cities with larvae, besides motor vehicles (primarily taxis), transportation by train, ship and plane might also be used.
Although most caterpillars are sold for cash, in some regions they are bartered for food, clothes, household utensils, cigarettes, alcohol or machetes. Zitzmann (1999) reported that among the Pygmies of CAR and in Botswana bartering is the common practice. The Pygmies usually barter at informal trade points close to the forest in the evenings. Merchants will then transport the larvae to cities for sale.
Price formation is dependent on the species and its quality. In the case of fresh caterpillars, the price may decrease within one day because of desiccation. Additional factors that influence price include:
the culinary traditions and/or species preferences of local communities;
the period (e.g. increased prices at the beginning and the end of the season);
the distance between producer and consumer (transportation, storage, etc.);
the number of intermediaries;
the provided quantity of caterpillars on the market;
the market place (e.g. different neighbourhoods in one town).
Caterpillars are sold in units. The most common small units are measured in glasses, bowls or handfuls; larger units are measured in buckets and sacks. An example is given for CAR:
Table 6:
Comparison of prices per kg for dried caterpillars depending on sale units
in Bangui
(NGasse
2003)
|
Supplier |
Price when marketing small units |
Price when marketing 12 kg sacks | ||
|
[FCFA/kg] |
[US$/kg] |
[FCFA/kg] |
[US$/kg] | |
|
Producer |
1 000 |
1.7 |
1 000 |
1.7 |
|
+ |
||||
|
Wholesaler |
1 500 |
2.55 |
1 333 |
2.27 |
|
Retailer |
1 800 |
3.06 |
1 583 |
2.69 |
In several publications, the marketing of caterpillars is mentioned as an important income-generating activity (e.g. Latham, 1999; De Foliart, 1992; Merle, 1958). NGasse (2003) analysed the revenue of a wholesaler in the appropriate season (as reported in Table 7). This wholesaler purchased and sold 24 kg of caterpillars per day, 26 days each month, for three consecutive months.
Table 7: Income of a wholesaler marketing caterpillars in CAR (NGasse, 2003)
|
FCFA |
US$ | ||
|
Price of purchase per kg |
1 000 |
1.7 | |
|
Price of purchase per day (24 kg per day) |
24 000 |
40.8 | |
|
Additional expenses (transport, taxes, etc.) Per day |
2 500 |
4.25 | |
|
Total expenses per day |
27 500 |
46.75 | |
|
Price of marketing per kg |
1 333 |
2.27 | |
|
Income per day (24 kg per day) |
32 000 |
54.4 | |
|
Profit |
per day |
4 500 |
7.65 |
|
per month (26 days per month) |
117 000 |
198.9 | |
|
per year (3 month per year) |
351 000 |
596.7 | |
More in-depth comparative studies are needed (including studies of other insects such as termites, etc.) to best assess the contribution of caterpillar marketing to total household income during the season or within the year. In addition, research on how the benefits from marketing insects are spread among producers, wholesalers and retailers is necessary. It is assumed that the existing market chain is particularly advantageous for wholesalers.
Zitzmann (1999) provided a comprehensive study of livelihood strategies in Botswana that allows the following estimation for the researched household: the income from selling Imbrasia belina represents 13 percent of the total household cash income in one year14. The labour input for that activity required only 5.7 percent of all considered income-generating activities. Zitzmann also compared the gross margins per working hour: the sale of Imbrasia belina is ranked third after the sale of poultry and livestock, and thus plays a leading role in household livelihood. An example from Zambia indicates that annual income from caterpillar marketing is comparable to, or even greater than that of selling agricultural crops (Chidumayo, Mbata, 2002).
There is not only a significant trans-border trade in edible insects among all countries within the Central African region15, but also with Sudan and Nigeria and on a smaller scale with exportation to France and Belgium. Some exporting countries collect taxes at airports and/or border towns. In CAR, the Phytosanitary Service collects 2 000 FCFA (US$3.4) per shipped parcel of 20 kg weight (NGasse, 2003). Precise export figures are rarely recorded.
According to an inquiry made by Tabuna (2000), France and Belgium annually import, about 5 tonnes and 3 tonnes of dried Imbrasia sp. from DRC, respectively. In Belgium, the exported quantity is valued at US$41.500 (corresponding to an average price of US$13.83 per kg.)
Defoliation impact of caterpillars on host plants
Several caterpillar species that nourish on fresh leaves as they develop at the beginning of the rainy season are known to defoliate trees. Foresters often consider these caterpillars as pests. The defoliation causes a temporarily confined growth, but the trees usually respond by producing a second growth of leaves (Reeler, et al., 1991). However, after several attacks trees might loose vitality and the potential for a second growth. NGasse (2003) observed that the insects attack, if it is not an irregular outbreak, generates relatively insignificant permanent damage to host plants in the dense moist forest zone, and that such outbreaks have not been observed frequently or over large areas. The application of chemicals in these forests to control caterpillar outbreaks is therefore non-existent and thus, there are no risks on forest-gathered insects.
When feeding on farm crops, however, caterpillars negatively impact forest resources. In the region where the insects commonly feed on farm crops, pest control involves applying enormous amounts of chemicals to kill the insects (thus making them unsuitable for human consumption).
In their support, Dounias (1999) pointed out the positive effect of harvesting the pests. A characteristic example is the plentiful occurrence of Augosoma centaurus and Rhynchophorus phoenicis on Raphia sese and Elaeis guineensis. Even if there are often heavy damages to plants, the extensive harvest of the grubs contributes to maintain natural reproduction. The question is often raised whether an increased harvest of insects as food might serve as a form of biological pest control. Such a practice might result in the reduction of pesticides as well as in the creation of new economic opportunities for local people (De Foliart, 1990).
Harvesting impacts on forest resources
Harvesting caterpillars by hand is the most common method employed and the least harmful to forest resources. In some places, however, chopping down host trees for gathering the caterpillars is widespread. In Zambia, clearings of up to 2 ha were made in the woodland in years when caterpillars were abundant (Lees, 1962). In addition, the cutting of large branches is critical, as it predestines trees for felling afterwards. In this way, harvesting caterpillars can contribute to forest degradation and deforestation. Because of the damage caused by people cutting off branches and chopping down trees to collect caterpillars, foresters in Zambia consider caterpillars as pests (Holden, 1991).
Impacts of deforestation on caterpillar populations
From the case studies it appears that extensive collection of caterpillars does not negatively-affect their reproductive capacity. It can be assumed that the disappearance of given host tree species may in the long run be followed by a gradual decreasing supply of the given insect species, particularly those specific to certain host plants. Tree species disappear because of destructive insect-harvesting techniques or selective logging of high-value timber species like Sapelli (Entandrophragma angolense). According to investigations by Chidumayo, Mbata (2002), selective logging is particularly destructive in specific vulnerable ecosystems such as those where tree species do not regenerate through recruitment of saplings.
In general, forest degradation activities endanger the existence of insect populations. The problem of bushfires must be seriously considered as it disturbs both the natural habitat and insect populations. There are many reasons behind the burning of forests in the region, but the most common is to expand permanent agricultural land. The extensive use of fire for hunting game and more frequently to catch smaller bush rats also has a significant, negative impact on the forest habitat. It may result in the reduced survival for the most popular edible caterpillars, while at the same time, other, more resilient insect populations may increase (e.g. non-edible beetles).
As insects are part of the food chain of several birds and other small animals hunted for bushmeat, the reduced availability of insects ultimately affects the numbers of their predators. The resulting loss of biodiversity directly affects the food supply and livelihoods of local people as well as the fructification potential of given plant species by reducing their pollinator.
Interestingly, the research by Holden (1991) linked caterpillar harvesting and the frequency of bushfires in Zambia. He noticed that there were very few late16 bushfires set in those areas where people harvest caterpillars, as the villagers wanted to protect the insects. Thus, he proposed research on caterpillars not only because they are important as food but also for their favourable impact on forest/woodland management. Similarly, Leleup, Daems (1969) investigated bush-burning dates in relation to the seasonal occurrence of different life stages (eggs, larvae, etc.) of three edible caterpillar species in DRC and provided several recommendations on the least destructive periods for premeditated bushfires.
Indirectly, deforestation may alter local micro-climates in the short run and contribute to climate changes in the long run, which disrupts insect lifecycles. Holden (1991) mentioned drought as a forthcoming problem, causing among other negative impacts the disappearance of host plants and corresponding edible insect species and/or the invasion and proliferation of other (non-edible) species.
1.2.8. Recommendations1. Although awareness has already increased, more attention should be paid by the research community to further investigate the biological potential of edible forest insects in a multidisciplinary and practical way; to include conservation, forest management, agriculture, nutrition and processing aspects. More specifically: a. Most species are taxonomically identified, but knowledge on life cycles, host plants, abundance in different habitats, etc. is fragmentary. A detailed inventory of the natural resource base and linkages between caterpillars and host plants should be a priority field of research. In addition, local people should be involved in this research, so that they can contribute with their traditional knowledge. b. Another priority in the field of nutrition is the analysis of cancer risks through the consumption of smoked caterpillars (and subsequently the improvement of preservation techniques). c. Further research in caterpillar processing and storage is needed. Adding value might also open new opportunities for exportation and marketing. Experiences from countries such as Botswana and Zimbabwe in reference to the Imbrasia belina industry should be duplicated if possible. 2. Edible insects and their trade make a significant contribution to livelihoods of the poorest and most disadvantaged groups in the region. Research and development actions may include: a. A comprehensive socio-economic analysis at the household level to assess the contribution of insects to food security, including subsistence as well as income generation. The analysis should distinguish the different types of households involved in insect commercialization: producers, wholesalers and retailers. b. To improve household revenues through marketing insects, market chains and benefit-sharing must be analysed. As mainly women manage caterpillar processing and commercialization, producer-trade associations among women should be supported to improve their market share and profits. 3. Once more detailed and reliable information on the natural resource base, the markets and individual stakeholders is available, emphasis should go to investigating how best the production of insects can be incorporated in natural resource management and forest conservation plans: a. How to integrate the production and harvesting of caterpillars in forest, agroforest and land use management plans in general (e.g. to optimize yields and to ensure sustainable harvest levels and techniques with low risks to neighbouring farmed crops). The research of Holden (1991) and Chidumayo (1997) who documented positive impacts of caterpillar harvests on the reduction of bushfires is a very good example of potential ways to improve larvae production within an integrated land use system. b. Another critical field of research is the domestication of forest-based insect species and host plants, which should be considered in integrated land use management practices as it may support reforestation efforts. The focus is to identify suitable agroforestry systems and their management, appropriate selection of insect species and host plants, methods on how to reproduce vegetal material and conditions enabling increased yields of production (but with low risks for farmed crops). c. The development of such forest management systems includes analysis of tenure and access to forests, with their corresponding institutional frameworks and regulations regarding conflict management between different user groups in a forest concession; for example: the local people, caterpillar gatherers and timber producers. d. By means of education and extension programmes, forest users should be sensitized to understand the ecological processes and links between insect gathering and the forest ecosystem. An increased recognition of the negative impacts of deforestation and bushfires on caterpillar numbers and particularly the practice of tree-cutting for harvesting caterpillars should motivate people to adopt alternate techniques. |
Bahuchet, S. 1990. The Aka Pygmies: Hunting and gathering in the Lobaye forest. In: Hladik et al. 1990.
Balinga, M.P. 2003. Les chenilles et larves comestibles dans la zone forestière du Cameroun. Rapport de Consultation. FAO. Rome.
CE-FAO. 2001. Data collection and analysis for sustainable forest management in ACP Countries. Linking national and international efforts. Pilot studies: Zimbabwe. Programme de partenariat CE-FAO (1998-2001). FAO. Rome.
Chen, X., Feng, Y. 2002. Review on nutritive value of edible insects. Chinese Forestry Science and Technology 1) 2: 54-59.
Chidumayo, E.N. 1997. Miombo ecology and management: An introduction. Intermediate Technology Publications. Londres.
Chidumayo, E.N., Mbata, K.J. 2002. Shifting cultivation, edible chenilles and livelihoods in the Kopa area of northern Zambia. Forests, Trees and Livelihoods 12 (3): 175-193.
De Foliart, G.R. 1992. Insects as human food. Crop Protection (11) 5: 395-399.
De Foliart, G.R. 1990. Hypothesizing about palm weevil and palm rhinoceros beetle larvae as traditional cuisine, tropical waste recycling, and pest and disease control on coconut and other palms can they be integrated? Food Insects Newsletter 3 (2): 1, 3-4, 6.
De Foliart, G.R. 2002. The
human use of insects as a food resource: A bibliographic account in progress.
URL: http://www.food-insects.com/book7_31/Chapter%2015%20C%20
and%20E%20Africa%20Overview.htm. (Date:
06.10.2003)
Dounias, E. 1999. Lexploitation méconnue dune ressource connue: La récolte des larves comestibles de charançons dans les palmiers raphia au Cameroun. Présentation orale. In: Balinga (2003).
Dreyer, J.J., Wehmeyer, A.S. 1982. On the nutritive value of mopanie worms. South African Journal of Science 78: 33-35.
Duffey, S.S. 1980. Sequestration of plant natural products by insects. Annual Review of Entomology 25: 447-477.
FAO. 1995. Non-wood forest products for rural income and sustainable forestry. Non-wood forest products 7. FAO, Rome.
FAO. 2003. URL: http://coin.fao.org/coin/coin_start.jsp. (Date: 16.09.2003)
Gomez, P.A., Halut, R., Collin, A. 1961. Production de protéines animales au Congo. Bulletin agricole du Congo 52 (4): 689-815.
Hladik, C.M., Bahuchet, S., De Garine, I. (ed.) 1990. Food and nutrition in the African rain forest. UNESCO, Paris.
Hladik, C.M., Hladik, A., Pagezy, H., Linares, O., Koppert, G.J.A., Froment, A. 1996. Lalimentation en forêt tropicale, interactions bioculturelles et perspectives de développement. Vol. 1: Les ressources alimentaires: production et consommation. UNESCO, Paris.
Holden, S. 1991. Edible caterpillars a potential agroforestry research? They are appreciated by local people, neglected by scientists. Food Insects Newsletter 4 (2): 3-4.
INTERNET (2003): URL: http://www.saturniidae-moths.de/Lepidoptera/Saturniidae/Database_-_caterpillars_from_S/epimethea/epimethea.html. (Date: 06.10.2003)
INTERNET (2003): URL: http://www.actias.de/GALLERY/SATURNIIDAE/show.asp?language=DE&Index=1&Folder=IMBRASIA&Time=. (Date: 14.11.2003)
Latham, P. 1999. Edible caterpillars of the Bas-Congo region of the Democratic Republic of the Congo. Antenna. Bulletin of the Royal Entomological Society (23) 3: 134-139.
Latham, P. 2002. Edible
caterpillars in Bas-Congo. Tropical Agriculture Association Newsletter (22) 1:
14-17.
(URL: http://www.taa.org.uk/TAAScotland/EdibleCaterpillars2.htm.
(Date: 06.10.2003)
Laurent, C. 1981. Conservation des produits dorigine animale en pays chauds. Collection Techniques vivantes. Presses Universitaires de France. Paris.
Lees, H.M.N. 1962. Working plan for the forests supplying the Copperbelt, western province, 1962-1967. Government Printer. Lusaka. In: Chidumayo, Mbata (2002).
Leleup, N., Daems, H. 1969. Les chenilles alimentaires du Kwango. Causes de leur raréfaction et mesures préconisées pour y remédier. Journal dagriculture tropicale et de botanique appliqué (16): 1-21.
Malaisse, F. 1997. Se nourrir en forêt claire africaine. Approche écologique et nutritionnelle. Les Presses agronomiques de Gembloux. Gembloux, Belgique.
Merle (Médecin Lt-Colonel) 1958. Des chenilles comestibles. Notes africaines 77: 20-23.
Monzambe Mapunzu, P. 2002. Contribution de lexploitation des chenilles et autres larves comestibles dans la lutte contre linsécurité alimentaire et la pauvreté en République démocratique du Congo. Rapport de Consultation. FAO. Rome.
Moussa, J.B. 2002. Les chenilles comestibles du Congo: Intérêt alimentaire et circuits de commercialisation: Cas de Brazzaville. Rapport de Consultation. FAO. Rome.
Munthali, S.M. et Mughogho, D.E.C. 1992. Economic incentives for conservation: Beekeeping and Saturniidae caterpillar utilisation by rural communities. Biodiversity and Conservation 1: 143-154.
NGasse, G. 2003. Contribution des chenilles/larves comestibles à la réduction de linsécurité alimentaire en République centrafricaine (RCA). Rapport de Consultation. FAO. Rome.
Paulin, R. 1963. Coeliades libeon Druce, chenille comestible du Congo. Bulletin de l'Institut de recherche scientifique du Congo 2: 5-6. In: Malaisse (1997).
Quin, P.J. 1959. Foods and feeding habits of the Pedi. Witwatersrand University. Johannesbourg, Afrique du Sud.
Ramos-Elorduy, J. 1996. Rôle des insectes dans lalimentation en forêt tropicale. In: Hladik et al. (1996).
Reeler, B., Campbell, B., Price, L. 1991. Defoliation of Brachystegia spiciformis by a species-specific insect, Melasoma quadralineata, over two growing seasons. Journal of African Ecology 29: 271-274.
Ruddle, K. 1973. The human use of insects: Examples from the Yupka. Biotropica 5: 94-101.
Sutton, M.Q. 1988. Insects as food: aboriginal entomophagy in the Great Basin. Ballena Press Anthropological Papers No. 33. Ballena Press. Menlo Park, Californie.
Tabuna, H. 2000. Evaluation des échanges des produits forestiers non ligneux entre l'Afrique subsaharienne et l'Europe. FAO, Rome et CARPE (Central African Regional Program for the Environment), USAID.
Vantomme, P., Göhler, D., Ndeckere-Ziangba, F. 2004. Contribution of forest insects to food security and forest conservation: The example of caterpillars in Central Africa. ODI Wildlife Policy Briefing nº 3. Http://www.odi-bushmeat.org/wildlife_policy_briefs.htm
Wu Leung, W.T., Busson, F., Jardin, C. (éd.) 1970. Table de composition des aliments à lusage de lAfrique. FAO, Rome et Department of Health, Education, and Welfare, Bethesda, Maryland.
Zitzmann, G. 1999. Multiple use and livelihood strategies in Mopane woodland. The case of Ditladi, north-east district, Botswana. Schriftenreihe des Institutes für Internationale Forst- und Holzwirtschaft Nr
1
Institut du développement dOutremer.
2 Identification taxonomique au moins du
genre.
3 Les
références de cette étude ne sont pas données.
4 Lidentification taxonomique des trois
espèces mentionnées nest pas donnée.
5 Le mot velt
en afrikaans signifie savane herbeuse claire dAfrique du Sud.
6 Il
y a deux périodes de récolte par an: décembre-janvier et mars-avril.
7
Pays de la Communauté économique et monétaire dAfrique centrale (CEMAC) comme le
Cameroun, la RCA, la RC, la RDC, le Gabon, la Guinée équatoriale et le
Tchad.
8 Dans ce contexte, «très peu de temps»
veut dire durant les semaines proches du début de la saison des pluies.
9
Overseas Development Institute.
10 Taxonomic identification at least up to
the genus.
11 The reference of that survey is not
given.
12
The taxonomic identification of the three mentioned species is not
given.
13
Velt: Afrikaans word for open grassland areas of southern Africa.
14
There are two periods of harvest within one year: December/January and
March/April.
15 These are the countries of the Economic and Monetary Community of Central Africa (CEMAC):
CAR, CMF, RC, DRC, Gabon, Equatorial Guinea and Chad.
16
Late, in this context, means in the weeks before the beginning of the
rainy season.