IDENTIDAD
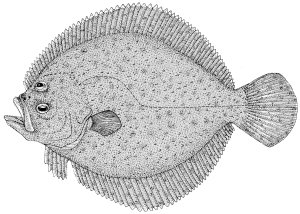
Rasgos biológicos
Pez plano con cuerpo asimétrico y casi redondo (ojos sobre el lado izquierdo). Piel sin escamas pero con protuberancias óseas irregularmente distribuidas. Boca grande y ojos pequeños. Las aletas dorsal y anal se expanden ampliamente sobre los costados dorsal y ventral. El lado ciego (derecho) de color blanquecino y el lado del ojo con coloración variable, generalmente café-grisácea con puntos oscuros.
PERFIL
Antecedentes históricos
La acuicultura del rodaballo comenzó en los 1970s en Escocia (Reino Unido). Fue subsecuentemente introducida en Francia y en España. Al comienzo, el número de instalaciones en España fue más bien limitado debido a la escasez de juveniles. El desarrollo tecnológico de la producción de juveniles cambió eso. Al comienzo de los 1990s, ya había 16 productores en España. Una crisis significativa en el cultivo de rodaballo ocurrió en 1992; hubo un aumento de 52 por ciento en la producción pero la industria carecía de una red consolidada para la comercialización. Otro factor que contribuyó a esta crisis fue que las granjas eran pequeñas y tenían costos muy altos de producción. Esta crisis causó el cierre de algunas granjas. Desde ese momento en adelante, comenzó una reorganización del sector, la cual dio origen a un crecimiento tanto en producción como en el número de países donde se cultiva el rodaballo. España, con sus condiciones oceanográficas altamente convenientes, es ahora el mayor productor del mundo, pero el rodaballo también se cultiva actualmente en Dinamarca, Alemania, Islandia, Irlanda, Italia, Noruega, Gales (Reino Unido) y Portugal y fue criado previamente en los Países Bajos. La distribución natural del rodaballo incluye las aguas costeras de todos estos países. El rodaballo también ha sido introducido en otras regiones (notablemente Chile a fines de los 1980s) y más recientemente, China.
Además de la inversión comercial en mejores instalaciones o la construcción de nuevas granjas, otros factores decisivos han asistido en la consolidación y desarrollo del sector. Estos han incluido la producción de alimentos secos y el desarrollo de vacunas para las enfermedades más importantes que afectan al rodaballo.
Además de la inversión comercial en mejores instalaciones o la construcción de nuevas granjas, otros factores decisivos han asistido en la consolidación y desarrollo del sector. Estos han incluido la producción de alimentos secos y el desarrollo de vacunas para las enfermedades más importantes que afectan al rodaballo.
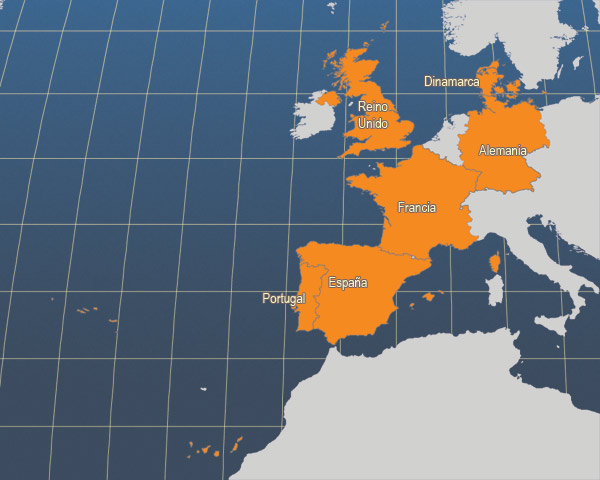
Principales países productores

Principales países productores de Psetta maxima (FAO Estadísticas pesqueras, 2006)
Hábitat y biología
Psetta maxima es una especie marina bentónica, que vive sobre fondos arenosos y fangosos, desde aguas someras hasta 100 m. Los individuos más jóvenes tienden a vivir en áreas menos profundas. Crípticos, imitando el color del substrato. Carnívoros, los juveniles se alimentan de moluscos y crustáceos y los adultos principalmente de peces y cefalópodos. El desove (secuencial, cada 2-4 días) usualmente ocurre en el Mediterráneo entre febrero y abril inclusive y en el Atlántico entre mayo y julio inclusive. Los huevos tienen una sola gota de grasa. Las larvas son inicialmente simétricas, pero hacia el final de la metamorfosis (día 40-50, 25 mm) el ojo derecho se ha movido a la izquierda, dando lugar a la asimetría. Antiguamente conocido como Scophthalmus maximus.
PRODUCCIÓN

Psetta maxima es una especie gonocórica con sexos separados. Los reproductores son mantenidos en tanques cuadrados de concreto o cemento, con volúmenes entre 20-40 m³ a densidades de 3-6 kg/m³ y alimentados con pellets húmedos. Los desoves se obtienen extrayendo los gametos (esperma y huevos) de los reproductores. Las hembras experimentan ciclos ovulatorios con un período aproximado de 70-90 horas. Los huevos son pelágicos y de forma esférica. El diámetro de los huevos varía entre 0,9 mm y 1,2 mm. El dsarrollo embrionario toma 60-70 días. Después de eclosionar, las larvas de rodaballo miden 2,7-3,1 mm de longitud..
El cultivo de larvas puede ser semi-intensivo o intensivo. En los sistemas semi-intensivos, las larvas son cultivadas a baja densidad (2-5 larvas/litro) en un gran volumen (50 m³), mientras que en el cultivo intensivo la densidad de larvas es más alta (15-20/litro) y el volumen del tanque es 20-30 m³. En ambos sistemas la temperatura de crianza es 18-20 °C. Las larvas recién eclosionadas se alimentan de sus propias reservas vitelinas; la apertura de la boca ocurre al día 3. Entonces la alimentación se basa en rotíferos y artemia. Se agrega fitoplancton al medio de cultivo. La primera alimentación se proporciona en tanques cuadrados con esquinas redondeadas y bombeo de agua de mar en circuito abierto. Se emplean varios alimentos comerciales en la etapa de primera alimentación.
La crianza de los rodaballos se realiza en tanques cuadrados o circulares (10-30 m³) con bombeo de agua de mar en circuito abierto. Usualmente se usan sistemas de aireación para mantener el agua saturada de oxígeno. Los juveniles son alimentados con dietas secas peletizadas, introducidas manualmente o automáticamente. El peso varía entre 5-10 g y 80-100 g durante el período de pre-engorda (4-6 meses de duración).
Los rodaballos son engordados ya sea en tanques en tierra (la técnica más común para esta especie) o en jaulas de fondo plano.
Tanques en tierra
Se usan tanques de cemento cuadrados o circulares (25-100 m³), con bombeo de agua de mar en circuito abierto. Normalmente se usan sistemas de aireación u oxigenación para mantener el agua saturada de oxígeno. La alimentación consiste de pellets extruídos, que se introducen manualmente o automáticamente. Los elementos que determinan la productividad son la temperatura y la calidad de los alevines. Las temperaturas óptimas para la alimentación varían entre 14-18 °C, mientras que la gama extrema para el cultivo del rodaballo es 11-23 °C. Los factores limitantes son patologías, tecnologías de cultivo y mercados.
Jaulas
Se usan jaulas sumergidas a varios niveles, o jaulas flotantes, en ambos casos de fondo plano. Los marcos son metálicos, con un fondo de metal o red. Los alimentos extruídos peletizados se entregan manualmente. Los elementos que determinan la productividad son localización apropiada, temperatura del agua y calidad de los alevines.
Dietas comerciales para rodaballo están disponibles, con un costo actual (2003) de 900 EUR/tonelada. La tasa de conversión del alimento (TCA) típica es 1,1-1,2:1.
Los peces son cosechados manualmente y sacrificados colocándolos en contenedores llenos con hielo y agua de mar, transportándolos luego a unidades de procesamiento.
Los peces cosechados son embalados en cajas de poliestireno, cubiertos con una capa de hielo y película plástica. En España, los rodaballos generalmente son comercializados enteros y en fresco, mientras que en el resto de Europa generalmente son eviscerados antes de la venta. España ha comenzado a producir rodaballo fileteado para satisfacer otra demanda del mercado europeo. La demanda por tamaño ha cambiado. Antes abarcaba entre 1,5-2,0 kg pero ahora tamaños más pequeños son aceptables; actualmente las ventas varían entre 0,7 kg y 2,0 kg.
El costo de producción de engorda es alrededor de 5-6 EUR/kg en tanques y 5 EUR/kg en jaulas. A pesar de los costos más altos del cultivo en tanques en tierra, este sigue siendo la norma debido a que el cultivo en jaula de esta especie está aun en etapa experimental y hay pocas localizaciones que reúnen las condiciones óptimas para la engorda.
Ciclo de producción

Ciclo de producción de Psetta maxima
Sistemas de producción
Suministro de semilla
Psetta maxima es una especie gonocórica con sexos separados. Los reproductores son mantenidos en tanques cuadrados de concreto o cemento, con volúmenes entre 20-40 m³ a densidades de 3-6 kg/m³ y alimentados con pellets húmedos. Los desoves se obtienen extrayendo los gametos (esperma y huevos) de los reproductores. Las hembras experimentan ciclos ovulatorios con un período aproximado de 70-90 horas. Los huevos son pelágicos y de forma esférica. El diámetro de los huevos varía entre 0,9 mm y 1,2 mm. El dsarrollo embrionario toma 60-70 días. Después de eclosionar, las larvas de rodaballo miden 2,7-3,1 mm de longitud..
Producción en viveros
El cultivo de larvas puede ser semi-intensivo o intensivo. En los sistemas semi-intensivos, las larvas son cultivadas a baja densidad (2-5 larvas/litro) en un gran volumen (50 m³), mientras que en el cultivo intensivo la densidad de larvas es más alta (15-20/litro) y el volumen del tanque es 20-30 m³. En ambos sistemas la temperatura de crianza es 18-20 °C. Las larvas recién eclosionadas se alimentan de sus propias reservas vitelinas; la apertura de la boca ocurre al día 3. Entonces la alimentación se basa en rotíferos y artemia. Se agrega fitoplancton al medio de cultivo. La primera alimentación se proporciona en tanques cuadrados con esquinas redondeadas y bombeo de agua de mar en circuito abierto. Se emplean varios alimentos comerciales en la etapa de primera alimentación.
Criadero
La crianza de los rodaballos se realiza en tanques cuadrados o circulares (10-30 m³) con bombeo de agua de mar en circuito abierto. Usualmente se usan sistemas de aireación para mantener el agua saturada de oxígeno. Los juveniles son alimentados con dietas secas peletizadas, introducidas manualmente o automáticamente. El peso varía entre 5-10 g y 80-100 g durante el período de pre-engorda (4-6 meses de duración).
Producción en viveros
Los rodaballos son engordados ya sea en tanques en tierra (la técnica más común para esta especie) o en jaulas de fondo plano.
Tanques en tierra
Se usan tanques de cemento cuadrados o circulares (25-100 m³), con bombeo de agua de mar en circuito abierto. Normalmente se usan sistemas de aireación u oxigenación para mantener el agua saturada de oxígeno. La alimentación consiste de pellets extruídos, que se introducen manualmente o automáticamente. Los elementos que determinan la productividad son la temperatura y la calidad de los alevines. Las temperaturas óptimas para la alimentación varían entre 14-18 °C, mientras que la gama extrema para el cultivo del rodaballo es 11-23 °C. Los factores limitantes son patologías, tecnologías de cultivo y mercados.
Jaulas
Se usan jaulas sumergidas a varios niveles, o jaulas flotantes, en ambos casos de fondo plano. Los marcos son metálicos, con un fondo de metal o red. Los alimentos extruídos peletizados se entregan manualmente. Los elementos que determinan la productividad son localización apropiada, temperatura del agua y calidad de los alevines.
Suministro de alimento
Dietas comerciales para rodaballo están disponibles, con un costo actual (2003) de 900 EUR/tonelada. La tasa de conversión del alimento (TCA) típica es 1,1-1,2:1.
Técnicas de cosecha
Los peces son cosechados manualmente y sacrificados colocándolos en contenedores llenos con hielo y agua de mar, transportándolos luego a unidades de procesamiento.
Manipulación y procesamiento
Los peces cosechados son embalados en cajas de poliestireno, cubiertos con una capa de hielo y película plástica. En España, los rodaballos generalmente son comercializados enteros y en fresco, mientras que en el resto de Europa generalmente son eviscerados antes de la venta. España ha comenzado a producir rodaballo fileteado para satisfacer otra demanda del mercado europeo. La demanda por tamaño ha cambiado. Antes abarcaba entre 1,5-2,0 kg pero ahora tamaños más pequeños son aceptables; actualmente las ventas varían entre 0,7 kg y 2,0 kg.
Costos de producción
El costo de producción de engorda es alrededor de 5-6 EUR/kg en tanques y 5 EUR/kg en jaulas. A pesar de los costos más altos del cultivo en tanques en tierra, este sigue siendo la norma debido a que el cultivo en jaula de esta especie está aun en etapa experimental y hay pocas localizaciones que reúnen las condiciones óptimas para la engorda.
Enfermedades y medidas de control
En algunos casos se han utilizado antibióticos y otros productos farmacéuticos en el tratamiento, pero su inclusión en esta tabla no implica una recomendación de la FAO.
Proveedores con experiencia en patología
Consejo experto en patología se puede obtener de:
| ENFERMEDAD | AGENTE | TIPO | SINDROME | MEDIDAS |
| Enfermedad Amébica de las Agallas (AGD) | Neoparamoeba pemaquidensis | Ectoparásito | Parasitismo de las agallas; dificultad y daño respiratorio | Baño de agua dulce |
| Tricodiniasis | Trichodina spp. | Ectoparásito | Destello; obscurecimiento de la piel; letargo; dificultades respiratorias; frotamiento de la cubierta de las agallas y del cuerpo contra las superficies de los estanques o jaulas | Baño desinfectante |
| Escuticociliatosis | Philasteridis dicentrarchi | Ecto, Endoparásito | Ulceras cutáneas; piel obscurecida; alteraciones del comportamiento natatorio; ojos abombados; distensión abdominal | Reducción de la densidad |
| Microsporidiosis | Tetramicra brevifilum | Endoparásito | – | Reducción de la densidad |
| Mixosporidiosis | Enteromysum scophthalmi | Endoparásito | Numerosos quistes blancos sobre la piel y agallas | Reducción de la densidad; desinfección completa de las instalaciones |
| Flexibacteriosis | Tenacibaculum maritimun | Bacteria | Al principio manchas grises en el área de la aleta dorsal; lesiones en la cabeza y boca; a veces podredumbre de las agallas | Vacuna; antibióticos |
| Furunculosis | Aeromonas salmonicida | Bacteria | Lesiones como ebullición de la piel | Antibióticos; vacunas hechas en la granja |
| Streptococcosis | Streptococcus parauberis | Bacterium | Hemorragia de las aletas, piel y superficies serosas; úlceras | Vacuna |
| Vibriosis | Vibrio anguillarum | Bacterium | Piel obscurecida; letargo; aletas raídas; úlceras en la piel; exoftalmia | Vacuna; antibióticos |
Proveedores con experiencia en patología
Consejo experto en patología se puede obtener de:
- Juan Luis Barja Pérez, Alicia Estévez Toranzo & Carlos Pereira Dopazo, Instituto de Acuicultura, Universidad de Santiago de Compostela
- Carlos Zarza, Servicio de Patología Skretting España ([email protected])
- Frances Padrós. Servicio de Diagnóstico Patológico en Peces. Universidad Autónoma de Barcelona ([email protected])
ESTADÍSTICAS
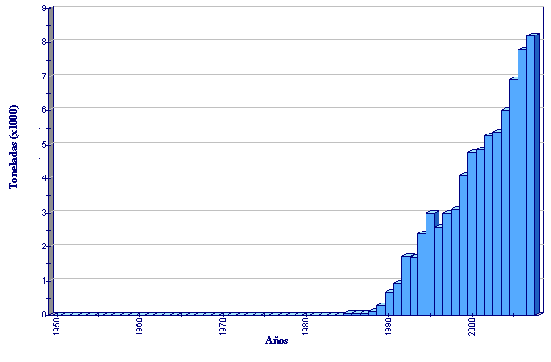
Estadísticas de producción
Producción de acuicultura global de Psetta maxima
(FAO Estadísticas pesqueras)
(FAO Estadísticas pesqueras)

Mercado y comercio
La mayoría del rodaballo cultivado es consumida actualmente en los países productores. En España, alrededor del 75 por ciento de la producción es consumida internamente; el resto es exportado a Francia, Italia y Alemania. El producto es generalmente vendido fresco y entero, aunque en Francia una pequeña proporción de la producción se vende eviscerada. El mercado europeo del rodaballo no tiene regulaciones específicas y no hay límites sobre el comercio dentro de los países de la UE, ni tamaños mínimos, ni precio de retiro.
ESTATUS Y TENDENCIAS
La acuicultura del rodaballo puede ser considerada actualmente como una tecnología madura. Parece probable que la industria verá una marcada expansión en el futuro, con la construcción de nuevas unidades de crianza y el aumento de la capacidad de las granjas existentes. Sin embargo, se requiere un esfuerzo continuado de investigación y desarrollo en las siguientes áreas:
- Producción de alevines, enfocada a aumentar las tasas de sobrevivencia larval.
- Mejoramiento de los sistemas de cultivo y automatización.
- Prevención y control de enfermedades.
- Supervisión de reproductores y mejoramiento genético.
- Mejoramiento de la comercialización, con la consolidación de los mercados existentes y el desarrollo de nuevos mercados; se necesita explorar nuevas avenidas para el procesamiento.
- Entrenamiento para personal técnico con habilidades combinadas en tecnología de acuicultura y manejo de negocios.
PRINCIPALES ASUNTOS
El sector está evolucionando y está consolidado en tierra; el cultivo en jaulas está comenzando recién y se considera que está en su etapa piloto.
Prácticas de acuicultura responsable
El cultivo del rodaballo es reconocido por su responsabilidad. La mayoría de las compañías han implementado ISO 14001 y algunas cumplen con el sistema EMAS II de la UE. En estudios sobre la acuicultura en tierra del rodaballo no se ha detectado impacto sobre el ambiente. Sin embargo, debiera adherirse a los principios del Código de Conducta para las Pesquerías Responsables de la FAO.
REFERENCIAS
Bibliograf�a
| Barton, L.A. 1981. Egg-quality of turbot (Scophthalmus maximus L.) kept in captive conditions. PhD Thesis, University of Liverpool, UK. 127 pp. |
| Devesa, S. 1996. Patología del rodaballo (Scophthalmus maximus L.) cultivado en Galicia. Tesis doctoral, Universidad de Santiago de Compostela. España. 342 pp. |
| Fauvei, C., Ommes, M.E., Mugnier, C., Normand, Y., Dorange, G. & Suquet, M. 1993. La reproduction du turbot. Aspects biologiques et gestion des reproducteurs. La Pisciculture Francaise, 112: 23-39. |
| Fernandez, B. & Rodríguez, X.L. 2003. European Fish Farming Guide. Consellería de Pesca e Asuntos Maritimos Xunta de Galicia. [ISBN: 84-453-3470-0] |
| Fernández Pato, C.A. 1998. Aspectos biológicos y tecnológicos del cultivo de rodaballo (Scophthalmus maximus L.). Tesis doctoral. Microfichas del Instituto Español de Oceanografía. MAPA, 12: 16 pp. + 185 pp. (2 microfiches). [ISBN: 84-491-0343-6] |
| Hall, J. 1997. Turbot farming in Europe: an overview. In M.D.B. Burt & S. Waddy (eds.), Aquaculture to the Year 2000, Proceedings of the Coldwater Aquaculture to the Year 2000 Conference, September 1995, St. Andrews, New Brunswick, Canada. Bulletin of the Aquaculture Association of Canada, Special Publication, 2:31-36. |
| Iglesias, J., Olmedo, M., Otero, J.J., Peleteiro, J.B. & Solorzano, M. 1987. Growth under laboratory conditions of turbot (Scophthalmus maximus L.) from the Ría de Vigo (NW Spain). Marine Biology, 98:11-17. |
| Jones, A. 1970. Some aspects of the biology of the turbot (Scophthalmus maximus L.) with special reference to feeding and growth in the juvenile stage. PhD Thesis, University of East Anglia, U.K. 145 pp. |
| Josupeit, H. 1995. European markets for seabass, seabream and turbot. European Aquaculture 20(2):6-12. |
| Labarta, U. 2000. Desarrollo e innovación empresarial en la acuicultura una perspectiva gallega en un contexto internacionalizado. Documentos de Economía 6, Fundación Caixa Galicia, Spain. 79 pp. |
| Lythgoe, J. & Lythgoe, G. 1994. Guia de los peces de mar del Atlántico Norte y del Mediterraneo. Ed Omega. 256 pp. [ISBN 84-282-0977-4] |
| McEvoy, L.A. 1984. Ovulatory rhythms and over-ripening of eggs in cultivated turbot (Scophthalmus maximus L.). Journal of Fish Biology, 24:437-448. |
| Olmedo, M. 1995. Contribución al desarrollo del cultivo intensivo de larvas de rodaballo. (Scophthalmus maximus Linnaeus, 1758.) (Pisces, Pleuronectiformes) en Galicia. Tesis Doctoral, Universidad de Santiago de Compostela, España. 142 pp. |
| Peleteiro, J.B. 2001. Control de la reproducción del rodaballo (Scophthalmus maximus L.) en cautividad. Tesis Doctoral, Universidad de Santiago de Compostela, España. 161 pp. |
| Stottrup, J.S. 1994. The intensive rearing of turbot (Scophthalmus maximus L.) larvae. PhD. Thesis, Odense University, Denmark. 113 pp |