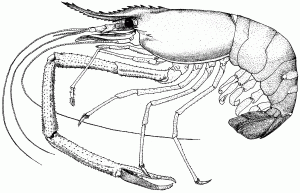
IDENTIFICATION
Caractéristiques biologiques
Les mâles peuvent atteindre 320 mm de long, les femelles 250 mm. Corps normalement verdâtre à gris-brûnatre, parfois plus bleuâtre, plus foncé chez les grands spécimens. Les antennes souvent de couleur bleue, chélipèdes bleu orange. Antennes souvent bleues; chélipèdes bleue ou orange. 14 somites dans le céphalothorax couvert par une grande boucle (carapace); carapace lisse et dure. Rostre long, arrivant normalement au delà du niveau de l'antenne, mince et quelque peu sigmoïde; la partie distale courbée un peu vers le haut; Dents 11-14 dorsales et 8-10 ventrales. La partie céphalique contient des yeux, antennules, antennes, mandibules, maxillipèdes, et maxille. Présence des pédoncules oculaires, à l'exception du premier stade larvaire. Thorax contient trois paires de maxillipèdes, utilisées comme des parties de la bouche, et cinq paires de péréiopodes (vrais pieds). Les deux premières paires péréiopodes chélates; chaque paire de chélipèdes est égale en taille. Les chélipèdes secondaires portent de nombreuses spinules; fortes; minces; peuvent être excessivement longs; pince mobile couverte par une dense, solide plutôt courte pubescence. Abdomen a 6 somites, chacun avec une paire de pléopodes ventrale (swimmerets). Pléopodes de six somites abdominales rigides et dures, avec un telson médian, qui sert comme une queueéventail. Onze différents stades larvaires.
Galerie d'images
 |
 |
Mâle de grande taille (Photo: Deborah Ismael) |
Mâles capturés en milieu naturel |
 |
 |
Femelles œuvées (Photo: Takuji Fujimura) |
PB, PO, et PM de crevettes (Photo: Assaf Barki) |
PROFIL

Noter: Le Viet Nam est aussi un grand producteur de M. rosenbergii; ceci n’est pas illustré sur la carte car le Viet Nam inclut sa production dans la catégorie ‘crevette d’eau douce, shrimps nei’ (n’est pas incluse ailleurs) quand les données sont communiquées à la FAO.
Contexte historique
Bien qu’elle soit élevée en captivité depuis un temps immémorial, l’élevage moderne de cette espèce a commencé au début de 1960 quand un expert de la FAO Shao-Wen Ling, en travaillant en Malaisie, a trouvé que les larves de la crevette d’eau douce (Macrobrachium rosenbergii) ont besoin de conditions saumâtres pour survivre. Cette découverte a mené à un élevage larvaire sur une base expérimentale. En 1972 l’équipe Hawaiienne dirigée par Takuji Fujimura a développé des techniques d’élevage en masse pour la production de postlarves (PL) de crevettes sur une échelle commerciale. Ce développement a donné naissance à la première ferme commerciale à Hawaii et ailleurs. Aussi bien la Thaïlande et le Taiwan sont devenus des pionniers dans la culture moderne de la crevette de rivière géante. L’introduction de géniteurs, initialement de Hawaii et de Thaïlande, dans des zones non indigènes partout dans le monde a commencé en 1970. Le premier grand projet de la FAO désigné pour étendre la culture de cette espèce a débuté en 1978 en Thaïlande. Depuis, la culture du bouquet géant s’est développée dans tous les continents, particulièrement en Asie et en Amériques. La production globale a augmenté à plus de 200 000 tonnes/an en 2002 (incluant la production au Viet Nam). De plus, il y’a une production considérable d’autres espèces de crevettes d’eau douce, notamment M. nipponense qui ne figure pas dans les statistiques officielles.
Principaux pays producteurs

Principaux pays producteurs de Macrobrachium rosembergii (FAO Statistiques des pêches, 2006)
Noter: Le Viet Nam est aussi un grand producteur de M. rosenbergii; ceci n’est pas illustré sur la carte car le Viet Nam inclut sa production dans la catégorie ‘crevette d’eau douce, shrimps nei’ (n’est pas incluse ailleurs) quand les données sont communiquées à la FAO.
Habitat et biologie
Cette espèce vit dans des environnements d’eau douce tropicaux influencés par des zones adjacentes d’eaux saumâtres. Elle est souvent rencontrée dans des conditions extrêmement turbides. Les femelles gravides migrent vers l’avale des rivières vers les estuaires, où les œufs éclorent en larves qui nagent librement dans l’eau saumâtre. Avant de se métamorphoser en post larves (PL), les larves planctoniques passent par plusieurs stades. Après métamorphose, les PL adoptent un style de vie plus benthique et commencent à émigrer vers l’eau douce en amont. Les larves nagent activement queue en premier, côté ventral en dessus. Ce n’est qu’à partir du stade PL et même plus tard, que les crevettes commencent à nager vers l’avant, côté dorsal au dessus. A partir de la métamorphose, les crevettes peuvent aussi marcher, pas seulement sur le substratum mais aussi sur des zones humides incluant des graviers de par les bords des rivières, jusqu’aux surfaces verticales (petites cascades, déversoirs, etc.) et à travers les terres. Les larves consomment en grande partie des zooplanktons (principalement miniatures de crustacés), de très petits vers, et les différents stades larvaires d’autres crustacés. Les postlarves et les adultes sont omnivores, se nourrissant des algues, plantes aquatiques, mollusques, insectes aquatiques, vers et autres crustacés. Les mâles et les femelles ont des taux de croissance différents et les mâles montrent une croissance individuelle hétérogène (HIG); ce sont des facteurs très important dans la gestion du grossissement. Trois mâles morphotypes différents (et certains de types intermédiaires) existent : petit mâle (PM), mâles à pince orange (PO), et mâles à pince bleue (PB). La ligne de développement normale d’un mâle normal est PM→ PO → PB. Les mâles PB ont des péréiopodes extrêmement secondaires; ceux des mâles PO sont de couleur or; les PM ont des petits, minces, presque des pinces translucides. Le type et le comportement des mâles affectent les taux de croissance d'autres crevettes. La transition de la croissance rapide des mâles PO aux mâles PB dont la morphotype est à croissance lente suit le modèle de croissance appelé "leapfrog". Un male PO se métamorphose en PB seulement s'il devient plus grand que le plus grand PB de son entourage. La présence de nouveaux mâles PO retarde donc la transition du PO suivant au morphotype PB, en le poussant à atteindre une taille plus grande suivant sa métamorphose. Les mâles PB dominent les mâles PO OC, malgré leur taille, et inhibent la croissance des PM.
PRODUCTION

Les géniteurs femelles nécessaires pour l’écloserie sont normalement obtenus des étangs de grossissement mais parfois aussi des captures de pêche. Normalement, les femelles « oeuvées » (porteuses d’œufs » sont utilisées seulement une fois. Les fermes commerciales dans les régions tropicales ne gardent pas normalement des géniteurs en captivité pour la reproduction mais les adultes sont maintenus à l’intérieur durant tout l’hiver dans des régions tempérées pour pourvoir les étangs avec des PL aussitôt que possible durant la saison courte de grossissement. Le rapport typique mâle / femelle dans les systèmes de maintien des géniteurs est 1-2 mâle PB ou 2-3 mâle PO pour 20 femelles à une densité totale de 1 crevette par 40 litres. Dans quelques heures de copulation, la fécondation a lieu à l’extérieur, et les œufs sont transférés dans la chambre d’incubation sous l’abdomen. Les oeufs restent adhérés aux femelles durant le développement embryonnaire, qui dure environ 3 semaines. A l’éclosion, les zoés nageant librement sont produites. Selon la taille de la femelle oeuvée, entre 5 000 et 100 000 oeufs sont portés. Les œufs sont oranges jusqu’à 2-3 jours avant l’éclosion, après, ils deviennent gris -noirs.
Certaines larves (PL, juvéniles) sont capturées dans le milieu naturel où M. rosenbergii est indigène, typiquement dans le sub-continent indien, mais la majorité provient des écloseries. Le premier stade zoé est juste de 2 mm de long et grandit, en passant par 11 stades larvaires, jusqu’à presque 8 mm pour se métamorphoser en PL. La métamorphose individuelle peut être achevée après 16 jours mais normalement dure beaucoup plus, selon les conditions environnementales. Dans les écloseries commerciales, la majorité des larves se métamorphosent après 32 à 35 jours à une température optimale de (28-31°C). L’élevage larvaire se fait normalement dans de l’eau saumâtre d’une salinité de 12‰, et les écloseries sont soit en flux ouvert (où une partie d’eau d’élevage est régulièrement remplacée) ou en re-circulation (où une variété de systèmes impliquant des filtres physiques et biologiques sont utilisés pour minimiser l’utilisation d’eau). Les deux types d’écloseries peuvent être continentales ou côtières. Les écloseries continentales préparent de l’eau saumâtre en mélangeant l’eau douce avec l’eau de mer transportée de la côte par des camions, ou avec une eau de mer artificielle. Certaines écloseries en flux ouvert utilisent le système d’« eau verte », qui implique la fertilisation pour augmenter la croissance de phytoplanctons (principalement Chlorella spp.), qui est sensée améliorer la qualité de l’eau et augmenter la survie des larves; d’autres opèrent en régime « eau claire ». Les systèmes d’alimentation varient largement mais incluent typiquement l’artémia (Artemia salina) distribuée plusieurs fois par jour au début, réduites à une fois par jour pendant le stade larvaire 10. L’aliment préparé (normalement une crème d'œuf 'egg custard' contenant moule ou chair de poisson, calamars, ou autres ingrédients) est introduit au stade 3 et la fréquence d’alimentation est augmentée en s’approchant de la métamorphose. Certaines écloseries sont intégrées avec les installations de nurserie et grossissement.
Bien que certains fermiers mettent dans les étangs de grossissement des jeunes PL, nombreux sont ceux qui achètent des juvéniles de plus grande taille ou cultivent les PL dans leurs étangs de nurseries avant de les transférer dans les étangs de grossissement. Dans les zones tempérées avec une saison de grossissement limitée, les nurseries closes contrôlées sont utilisées pour augmenter la taille des animaux avant le stockage à l’extérieur aussitôt que les températures deviennent assez élevées. Les nurseries contrôlées ont des densités de 1 000-2 000 PL/m³, selon si les substrats sont utilisés ou non. Les nurseries en plein air peuvent contenir des PL qui viennent de se métamorphoser ou des juvéniles provenant des nurseries fermées. Les taux de stockage classiques sont 1 000 PL /m², 200 petits juvéniles (0,02 g)/m² ou 75 juvéniles de 0,3-0,4 g/m², mais des densités plus élevées sont possibles si les substrats sont utilisés.
Les crevettes d’eau douce sont élevées dans des enclos variés d’eau douce, comme les bacs, les fossés d’irrigation, les cages, les enclos, les réservoirs, et dans des eaux naturelles, la forme commune étant les étangs en terre. Les méthodes normales d’élevage comprennent des combinaisons variées utilisant en premier des systèmes « en continu » (des étangs fonctionnant indéfiniment, avec des récoltes et re-stockage réguliers et sélectionnés) et en « batch » (un seul stockage, une seule récolte), ces systèmes sont connus comme des « systèmes combinés ». La plupart des systèmes impliquent des monocultures, mais la polyculture du bouquet géant avec des poissons et parfois autres crustacés est aussi pratiquée, particulièrement en Chine (avec des carpes). L’intégration de la culture du bouquet géant avec des produits agricoles est aussi possible (courante en Viet Nam).
Les densités de stockage d’étangs dans les monocultures tropicales varient largement. Dans les systèmes d’élevage extensif (produisant typiquement <500 kg/ha/an), les PL ou les jeunes juvéniles sont stockés à 1-4 ind./m²; les systèmes semi-intensifs (produisant 1-4 ind./m²; dans les zones tempérées avec une densité limitée d’environ 5-10 PL/m² ou 4 juvéniles/m² sont stockés ; les niveaux peuvent être augmentés en présence de substrat.
Les crevettes sont nourries avec de l’aliment commercial ou avec un aliment “préparé à la ferme”. Ce dernier est utilisé seul ou mélangé avec d’autres ingrédients, souvent extrudé à travers un hachoir et il est soit apporté humide soit (normalement) après avoir été séché au soleil. Les aliments classiquement utilisés contiennent 5 pour cent de lipides et 30-35 pour cent de protéines. Un TCA de 2:1 ou 3:1 est obtenu par un apport supplémentaire d’aliments secs. Les taux de croissance moyenne dépendent de plusieurs facteurs, particulièrement de la manière avec laquelle les mâles HIG sont gérés. Le taux de croissance des PM est rabougri par la présence des mâles PB; durant leur absence les PM se métamorphosent en PO et finalement en mâles PB. Ainsi, la méthode avec laquelle les étangs de grossissement sont gérés (par exemple, la fréquence avec laquelle les crevettes de grande taille sont sélectionnées, ainsi que la plus part des mâles) influence la productivité totale.
La récolte est soit totale (en élevage "batch") ou partielle (en élevage "continu" ou "combiné"). La récolte totale se fait en vidant l’eau par gravité ou pompage, alors que les filets de seine sont utilisés pour la sélection régulière des grands animaux. Des mailles élastiques de taille 1,8 cm sont utilisées pour récolter des crevettes de petites tailles et des mailles de 3,8-5,0 cm pour les crevettes de plus grandes tailles. Le temps et la fréquence de récolte dépendent du volume et des caractéristiques (taille des animaux) ainsi que de la demande du marché.
Une manipulation soigneuse est essentielle pendant et après la récolte pour assurer une bonne qualité des produits. Les crevettes d’eau douce tendent à devenir « froissées » si elles ne sont pas correctement manipulées et traitées. Premièrement, il faut éviter d’écraser les crevettes durant la récolte. Deuxièment, si elles ne sont pas destinées à la vente vivantes, elles doivent être tuées immédiatement dans un mélange d’eau avec de la glace à 0°C (au bord de l’étang), et nettoyées dans de l’eau chlorée. Les crevettes destinées à la vente vivantes peuvent être transportées dans de l’eau aérée à 20-22°C. Les crevettes vendues fraîches ne doivent pas être gardées dans de la glace pendant plus de 3 jours. Les crevettes qui sont destinées à être vendues congelées doivent être rapidement congelées à -10°C (pas simplement placées dans un congélateur «domestique») et gardées à -20°C ou moins.
Fournir des données sur les frais de production n’est pas facile, non seulement parce que l’information est normalement une propriété privée mais aussi parce qu’elle est spécifique au site. Par exemple, un aperçu sur les coûts des opérations en écloserie (toutes les valeurs sont normalisées au USD du 1997) a donné une moyenne de 10,6 USD/1 000 PL mais la rangée était de 1,1 to 17,0 USD/1 000 PL. Les coûts d’investissement en écloserie oscillent entre 12,4 et 19,0 USD pour 1 000 PL comme capacité de production. Les coûts d’investissement en nurseries pour produire 4 millions de juvéniles de 2 g en Amérique Latine, par exemple, ont été estimés à 50 000 USD. Les coûts de fonctionnement de nurseries ont été évalués à 6 USD par mille juvéniles de 2 g et 50 USD par mille juvéniles de 10 g en Thaïlande. Généralement, les dépenses relatives à l’aliment représentent au moins 40 pour cent des coûts totaux de production en nurserie. Les coûts d’investissement dans les facilités de grossissement varient entre 400 USD/ha (rendement de 600 kg/ha/an) en Inde à presque 64 000 USD/ha (rendement 2 270 kg/ha/an) aux Etats-Unis d’Amérique. D’une manière similaire, les coûts des opérations de grossissement varient entre moins de 2 USD à plus 15 de USD/kg/an. Le coût moyen divisé était 30 pour cent d’aliment, 20 pour cent juvéniles, 15 pour cent main d’oeuvre et 35 pour cent autres dépenses.
Cycle de production

Cycle de production de Macrobrachium rosenbergii
Systèmes de production
Approvisionnement en juvéniles
Les géniteurs femelles nécessaires pour l’écloserie sont normalement obtenus des étangs de grossissement mais parfois aussi des captures de pêche. Normalement, les femelles « oeuvées » (porteuses d’œufs » sont utilisées seulement une fois. Les fermes commerciales dans les régions tropicales ne gardent pas normalement des géniteurs en captivité pour la reproduction mais les adultes sont maintenus à l’intérieur durant tout l’hiver dans des régions tempérées pour pourvoir les étangs avec des PL aussitôt que possible durant la saison courte de grossissement. Le rapport typique mâle / femelle dans les systèmes de maintien des géniteurs est 1-2 mâle PB ou 2-3 mâle PO pour 20 femelles à une densité totale de 1 crevette par 40 litres. Dans quelques heures de copulation, la fécondation a lieu à l’extérieur, et les œufs sont transférés dans la chambre d’incubation sous l’abdomen. Les oeufs restent adhérés aux femelles durant le développement embryonnaire, qui dure environ 3 semaines. A l’éclosion, les zoés nageant librement sont produites. Selon la taille de la femelle oeuvée, entre 5 000 et 100 000 oeufs sont portés. Les œufs sont oranges jusqu’à 2-3 jours avant l’éclosion, après, ils deviennent gris -noirs.
Certaines larves (PL, juvéniles) sont capturées dans le milieu naturel où M. rosenbergii est indigène, typiquement dans le sub-continent indien, mais la majorité provient des écloseries. Le premier stade zoé est juste de 2 mm de long et grandit, en passant par 11 stades larvaires, jusqu’à presque 8 mm pour se métamorphoser en PL. La métamorphose individuelle peut être achevée après 16 jours mais normalement dure beaucoup plus, selon les conditions environnementales. Dans les écloseries commerciales, la majorité des larves se métamorphosent après 32 à 35 jours à une température optimale de (28-31°C). L’élevage larvaire se fait normalement dans de l’eau saumâtre d’une salinité de 12‰, et les écloseries sont soit en flux ouvert (où une partie d’eau d’élevage est régulièrement remplacée) ou en re-circulation (où une variété de systèmes impliquant des filtres physiques et biologiques sont utilisés pour minimiser l’utilisation d’eau). Les deux types d’écloseries peuvent être continentales ou côtières. Les écloseries continentales préparent de l’eau saumâtre en mélangeant l’eau douce avec l’eau de mer transportée de la côte par des camions, ou avec une eau de mer artificielle. Certaines écloseries en flux ouvert utilisent le système d’« eau verte », qui implique la fertilisation pour augmenter la croissance de phytoplanctons (principalement Chlorella spp.), qui est sensée améliorer la qualité de l’eau et augmenter la survie des larves; d’autres opèrent en régime « eau claire ». Les systèmes d’alimentation varient largement mais incluent typiquement l’artémia (Artemia salina) distribuée plusieurs fois par jour au début, réduites à une fois par jour pendant le stade larvaire 10. L’aliment préparé (normalement une crème d'œuf 'egg custard' contenant moule ou chair de poisson, calamars, ou autres ingrédients) est introduit au stade 3 et la fréquence d’alimentation est augmentée en s’approchant de la métamorphose. Certaines écloseries sont intégrées avec les installations de nurserie et grossissement.
Nurserie
Bien que certains fermiers mettent dans les étangs de grossissement des jeunes PL, nombreux sont ceux qui achètent des juvéniles de plus grande taille ou cultivent les PL dans leurs étangs de nurseries avant de les transférer dans les étangs de grossissement. Dans les zones tempérées avec une saison de grossissement limitée, les nurseries closes contrôlées sont utilisées pour augmenter la taille des animaux avant le stockage à l’extérieur aussitôt que les températures deviennent assez élevées. Les nurseries contrôlées ont des densités de 1 000-2 000 PL/m³, selon si les substrats sont utilisés ou non. Les nurseries en plein air peuvent contenir des PL qui viennent de se métamorphoser ou des juvéniles provenant des nurseries fermées. Les taux de stockage classiques sont 1 000 PL /m², 200 petits juvéniles (0,02 g)/m² ou 75 juvéniles de 0,3-0,4 g/m², mais des densités plus élevées sont possibles si les substrats sont utilisés.
Techniques de grossissement
Les crevettes d’eau douce sont élevées dans des enclos variés d’eau douce, comme les bacs, les fossés d’irrigation, les cages, les enclos, les réservoirs, et dans des eaux naturelles, la forme commune étant les étangs en terre. Les méthodes normales d’élevage comprennent des combinaisons variées utilisant en premier des systèmes « en continu » (des étangs fonctionnant indéfiniment, avec des récoltes et re-stockage réguliers et sélectionnés) et en « batch » (un seul stockage, une seule récolte), ces systèmes sont connus comme des « systèmes combinés ». La plupart des systèmes impliquent des monocultures, mais la polyculture du bouquet géant avec des poissons et parfois autres crustacés est aussi pratiquée, particulièrement en Chine (avec des carpes). L’intégration de la culture du bouquet géant avec des produits agricoles est aussi possible (courante en Viet Nam).
Les densités de stockage d’étangs dans les monocultures tropicales varient largement. Dans les systèmes d’élevage extensif (produisant typiquement <500 kg/ha/an), les PL ou les jeunes juvéniles sont stockés à 1-4 ind./m²; les systèmes semi-intensifs (produisant 1-4 ind./m²; dans les zones tempérées avec une densité limitée d’environ 5-10 PL/m² ou 4 juvéniles/m² sont stockés ; les niveaux peuvent être augmentés en présence de substrat.
Les crevettes sont nourries avec de l’aliment commercial ou avec un aliment “préparé à la ferme”. Ce dernier est utilisé seul ou mélangé avec d’autres ingrédients, souvent extrudé à travers un hachoir et il est soit apporté humide soit (normalement) après avoir été séché au soleil. Les aliments classiquement utilisés contiennent 5 pour cent de lipides et 30-35 pour cent de protéines. Un TCA de 2:1 ou 3:1 est obtenu par un apport supplémentaire d’aliments secs. Les taux de croissance moyenne dépendent de plusieurs facteurs, particulièrement de la manière avec laquelle les mâles HIG sont gérés. Le taux de croissance des PM est rabougri par la présence des mâles PB; durant leur absence les PM se métamorphosent en PO et finalement en mâles PB. Ainsi, la méthode avec laquelle les étangs de grossissement sont gérés (par exemple, la fréquence avec laquelle les crevettes de grande taille sont sélectionnées, ainsi que la plus part des mâles) influence la productivité totale.
Techniques de récolte
La récolte est soit totale (en élevage "batch") ou partielle (en élevage "continu" ou "combiné"). La récolte totale se fait en vidant l’eau par gravité ou pompage, alors que les filets de seine sont utilisés pour la sélection régulière des grands animaux. Des mailles élastiques de taille 1,8 cm sont utilisées pour récolter des crevettes de petites tailles et des mailles de 3,8-5,0 cm pour les crevettes de plus grandes tailles. Le temps et la fréquence de récolte dépendent du volume et des caractéristiques (taille des animaux) ainsi que de la demande du marché.
Manipulation et traitement
Une manipulation soigneuse est essentielle pendant et après la récolte pour assurer une bonne qualité des produits. Les crevettes d’eau douce tendent à devenir « froissées » si elles ne sont pas correctement manipulées et traitées. Premièrement, il faut éviter d’écraser les crevettes durant la récolte. Deuxièment, si elles ne sont pas destinées à la vente vivantes, elles doivent être tuées immédiatement dans un mélange d’eau avec de la glace à 0°C (au bord de l’étang), et nettoyées dans de l’eau chlorée. Les crevettes destinées à la vente vivantes peuvent être transportées dans de l’eau aérée à 20-22°C. Les crevettes vendues fraîches ne doivent pas être gardées dans de la glace pendant plus de 3 jours. Les crevettes qui sont destinées à être vendues congelées doivent être rapidement congelées à -10°C (pas simplement placées dans un congélateur «domestique») et gardées à -20°C ou moins.
Coûts de production
Fournir des données sur les frais de production n’est pas facile, non seulement parce que l’information est normalement une propriété privée mais aussi parce qu’elle est spécifique au site. Par exemple, un aperçu sur les coûts des opérations en écloserie (toutes les valeurs sont normalisées au USD du 1997) a donné une moyenne de 10,6 USD/1 000 PL mais la rangée était de 1,1 to 17,0 USD/1 000 PL. Les coûts d’investissement en écloserie oscillent entre 12,4 et 19,0 USD pour 1 000 PL comme capacité de production. Les coûts d’investissement en nurseries pour produire 4 millions de juvéniles de 2 g en Amérique Latine, par exemple, ont été estimés à 50 000 USD. Les coûts de fonctionnement de nurseries ont été évalués à 6 USD par mille juvéniles de 2 g et 50 USD par mille juvéniles de 10 g en Thaïlande. Généralement, les dépenses relatives à l’aliment représentent au moins 40 pour cent des coûts totaux de production en nurserie. Les coûts d’investissement dans les facilités de grossissement varient entre 400 USD/ha (rendement de 600 kg/ha/an) en Inde à presque 64 000 USD/ha (rendement 2 270 kg/ha/an) aux Etats-Unis d’Amérique. D’une manière similaire, les coûts des opérations de grossissement varient entre moins de 2 USD à plus 15 de USD/kg/an. Le coût moyen divisé était 30 pour cent d’aliment, 20 pour cent juvéniles, 15 pour cent main d’oeuvre et 35 pour cent autres dépenses.
Maladies et mesures de contrôle
Le problème majeur de maladies affectant Macrobrachium rosenbergii généralement a lieu à cause de la pauvre qualité de l’eau entrant, de la pauvre qualité d’élevage, du sur-stockage, de la pauvre hygiène, et de la non-existence de quarantaine ou de procédures inadéquates. Les mesures pour combattre ces problèmes sont référées comme une pratique d’élevage améliorée (PEA) dans le tableau suivant, qui englobe certaines des maladies les plus importantes. Dans quelque cas, les antibiotiques et d’autres médicaments pharmaceutiques ont été utilisés dans le traitement mais même s’ils sont mentionnés dans ce tableau ils ne sont pas recommandés.
| MALADIE | AGENT | TYPE | SYNDROME | MESURES |
| MMV (Virus du Muscle de Macrobrachium) | Virus comme virus Parvo | Virus | Infecte les tissus qui deviennent opaques, avec des nécroses progressives; affectent les juvéniles | PEA |
| WSBV (Taches Blanches Syndrome BaculoVirus) | Baculovirus | Virus | Taches blanches; affectent les juvéniles | PEA |
| Maladie virale non nommée | Nodavirus | Virus | Queue blanchâtre; affecte les larves | PEA |
| Taches noires; taches brunes; maladie de carapace | Vibrio; Pseudomonas; Aeromonas | Bactérie | Lésions mélanisées; affectent tous les stades de vie, mais plus fréquemment observés chez les juvéniles & adultes | PEA; acide oxolinique; nifurpurinol |
| Nécrose bactérienne | Pseudomonas; Leucothrix | Bactérie | Similaire aux taches noires mais affectent seulement les larves, spécialement stades IV & V | PEA; nifurpurinol; érythromycine; penicilline-streptomycine; chloramphénicol |
| Syndrome de luminescence larvaire Luminescent larval syndrome |
Vibrio harveyi | Bactérie | Larves Moribondes & mortes luminescentes | PEA; chloramphénicol; furazolidone |
| Maladie des postlarves blanches « White postlarval disease » | Ricksettsia | - | Larves blanches, spécialement stades IV & V | PEA; oxytetracycline; furazolidone; chaux avant stockage |
| Infection aux champignons non nommée | Lagenidium | Champignon | Extensive mycélium réseau visible à travers l'exosquelette de larve | PEA; trifluraline; merthiolate |
| Infection aux champignons non nommée (souvent associé avec IMN – voir ci-dessous) | Fusarium solani | Champignon | Infection secondaire; affecte les adultes | PEA |
| Infection au champignon "levure" non nommée | Debaryomyces hansenii; Metschnikowia bicuspidata | Champignon | Tissus musculaires jaunâtres, grisâtres ou bleuâtres chez les juvéniles | PEA |
| Infestation protozoaire | Zoothamnium; Epistylis; Vorticella; Opercularia; Vaginicola; Acineta; Podophyra; etc. | Protozoaire | Parasites externes qui inhibent la nage, l’alimentation, et la mue; affectent tous les stades de développement | PEA, formol; merthiolate; copper-based algicides |
| Nécrose Idiopathique du Muscle (NIM) (Idiopathic Muscle Necrosis) (IMN) | maladie environnementale | Inconnu | Couleur blanchâtre des tissus striés de la queue et appendices; quand l'infection est avancée, zones nécrotiques peuvent devenir rouges; affecte tous les stades de vie | PEA |
| Maladie du Mi-Cycle (MMC) (Mid-Cycle Disease) (MCD) | étiologie non déterminé | Inconnu | Léthargie; nage en spirale; réduction d’alimentation et croissance; couleur du corps bleuâtre-gris; affecte les larves, spécialement stades VI et VII | PEA; désinfection d’écloserie |
| EED (Exuvia Entrapment Disease), parfois connue comme MDS (Moult Death Syndrome) | étiologie non déterminé | Inconnu mais probablement causes multiples, incluant manque nutritionnel | Déformations localisées; échec dans l’achèvement de la mue; affecte les derniers stades larvaires; aussi observée chez les postlarves, juvéniles & adultes | PEA; enrichissement alimentaire |
STATISTIQUES
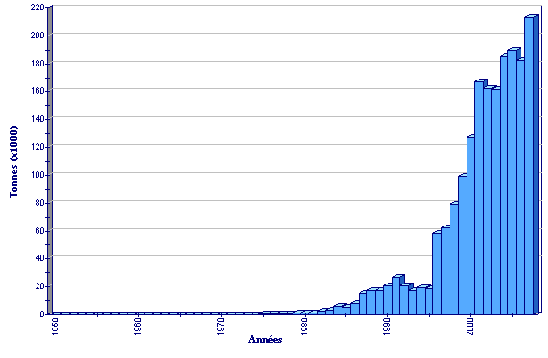
Statistiques de production
Production globale d’aquaculture de Macrobrachium rosenbergii
(FAO Statistiques des pêches)
(FAO Statistiques des pêches)
Marché et commercialisation
Aussi bien le marché local que l’international existent et sont en expansion. Décortiquée, essentiellement du Macrobrachium rosenbergii capturée en milieu naturel a été pendant longtemps exportée seule, mais des crevettes d’eau douce issues de culture avec carapace (et normalement sans tête) sont aussi devenues familières à l’œil dans les supermarchés européen. A un certain degré, ceci a aussi lieu aux Etats-Unis d’Amérique (principalement pour consommation par les Asiatiques ou dans les restaurants qui servent des repas asiatiques) et au Japon. L’Inde, le Bangladesh, le Viet Nam et la Thaïlande exportent une quantité significative de leurs crevettes capturées en milieu naturel ainsi que des crevettes d’élevage. Le potentiel de développement existe mais des producteurs de petite échelle peuvent avoir besoin de coopérer dans un marketing collectif pour profiter de ces opportunités. Les crevettes d’eau douce sont un produit différent des crevettes marines, qui a ses propres caractéristiques culinaires.
SITUATION ET TENDANCES
La production d’aquaculture est en expansion rapide en Asie. Le taux d’expansion dans le pays le plus producteur, la Chine, s’est ralentie, en partie à cause de la culture d’autres espèces indigènes (Macrobrachium nipponense) et en partie car les crevettes marines sont maintenant en élevage en eaux douce (et sont parfois référées erronément comme crevette d’eau douce). La production chinoise a chuté en 2002 mais, comme le marché global est en expansion, il est prévu qu’elle gagne encore du terrain plus tard. La production en Inde et en Thaïlande s’est élevée de plus de 50 pour cent par an entre 1999 et 2002, et il est prévu que cette situation continue. Il y a aussi un potentiel d’expansion à Bangladesh, un exportateur traditionnel à partir de ses captures de pêche. La production Indonésienne est reportée en 2002 pour la première fois. Le Viet Nam est un producteur et exportateur significatif de Macrobrachium d’élevage, même si sa production est masquée en étant inclue dans la catégorie des statistiques ‘crevette d’eau douce, shrimps nei’. Statistiquement, le Brésil apparaît aussi comme un producteur majeur (> 4 000 tonnes/an depuis 2000) mais ceci n’est pas vrai.
En total, la production de M. rosenbergii issue de l’aquaculture a augmenté durant la décade 1993-2002 de 17 000 tonnes à 195 000 tonnes, un APR de 31 pour cent/an. Depuis 1996, la production chinoise constitue une grande partie (58 pour cent in 2002); cependant, même si elle est exclue il devient clair que la production d’ailleurs s’est élevée de 17 000 tonnes en 1993 à presque 82 000 tonnes en 2002, soit un APR de 19 pour cent/an. De plus, de 1999 à 2002, l’expansion à l’extérieur de la Chine (41 pour cent/an) était beaucoup plus rapide qu’en Chine (13 pour cent).
Il est difficile de prédire l’expansion globale, puisque elle dépend principalement de la demande du consommateur. Cependant, même si une expansion très modeste de 10 pour cent/an se produit, la production globale de M. rosenbergii issue d’élevage excédera significativement 400 000 tonnes en 2010. La culture d’autres espèces de Macrobrachium, notamment M. nipponense (déjà très substantielle en Chine), M. malcolmsonii et M. amazonicum, s’élargira aussi.
En total, la production de M. rosenbergii issue de l’aquaculture a augmenté durant la décade 1993-2002 de 17 000 tonnes à 195 000 tonnes, un APR de 31 pour cent/an. Depuis 1996, la production chinoise constitue une grande partie (58 pour cent in 2002); cependant, même si elle est exclue il devient clair que la production d’ailleurs s’est élevée de 17 000 tonnes en 1993 à presque 82 000 tonnes en 2002, soit un APR de 19 pour cent/an. De plus, de 1999 à 2002, l’expansion à l’extérieur de la Chine (41 pour cent/an) était beaucoup plus rapide qu’en Chine (13 pour cent).
Il est difficile de prédire l’expansion globale, puisque elle dépend principalement de la demande du consommateur. Cependant, même si une expansion très modeste de 10 pour cent/an se produit, la production globale de M. rosenbergii issue d’élevage excédera significativement 400 000 tonnes en 2010. La culture d’autres espèces de Macrobrachium, notamment M. nipponense (déjà très substantielle en Chine), M. malcolmsonii et M. amazonicum, s’élargira aussi.
PROBLÈMES ET CONTRAINTES MAJEURS
Le développement de la culture de crevette d’eau douce a été inhibé dans le passé par la longueur de la phase d’écloserie et du faible rendement du grossissement comparé à la crevette marine. Ces contraintes sont maintenant équilibrées par un certain nombre de facteurs positifs concernant sa durabilité (voir ci-dessous des pratiques d’aquaculture responsable) et le développement d’un marché distinct et l’expansion des niches de marché pour la crevette d’eau douce. De plus, peu de produits de pauvre qualité entrent dans les marchés internationaux maintenant que la technique pour éviter la ressemblance "mushiness" est devenue bien connue.
Pratiques pour une aquaculture responsable
La culture de Macrobrachium spp est moins susceptible d’avoir un impact négatif car les crevettes d’eau douce ne peuvent pas être cultivées à des densités aussi élevées que celles classiquement utilisées dans l’élevage de crevettes marines. La productivité est généralement plus basse, la gestion nécessite moins de main d’oeuvre et le potentiel pour un abus ou une pollution des ressources est minimale, et (différent de la culture continentale de crevette marine) le grossissement de Macrobrachium ne cause pas de salinisation des terres agricoles. Des effets négatifs spécifiques de la culture de M. rosenbergii sur l’environnement doivent être documentés. L’adhérence au Code de Conduite pour une Pêche Responsable de la FAO pourrait assurer que cette culture reste durable et responsable. Il est particulièrement bien convenable que de petites affaires familiales de long terme, soient gérées par des gens ruraux et des pêcheurs inexpérimentés, pour générer des produits qui peuvent être consommés par toutes les classes sociales et soient souples pour l’intégration avec d’autres productions agricoles.
RÉFÉRENCES
Bibliographie
| FAO, 1995. Code of Conduct for Responsible Fisheries. FAO, Rome, Italy. 41p. |
| FAO, 1997. Aquaculture development. FAO Technical Guidelines for Responsible Fisheries. No. 5. FAO, Rome, Italy. 40p. |
| Griessinger, J-M., Lacroix, D. & Gondouin, P. 1991. L'élevage de la crevette tropicale d'eau douce. IFREMER, Plouzané, France. 372 pp. |
| Jayachandran, K.V.2001. Palaemonid prawns: biodiversity, taxonomy, biology and management. Science Publishers, Enfield (NH), USA. 624 pp. |
| New, M.B., 2002. Farming freshwater prawns: a manual for the culture of the giant river prawn (Macrobrachium rosenbergii). FAO Fisheries Technical Paper No. 428. FAO, Rome, Italy. 212p. |
| New, M.B. & Valenti, W.C. (editors), 2000. Freshwater Prawn Culture: the farming of Macrobrachium rosenbergii. Blackwell Science, Oxford, England. 443p. |
| New, M.B. & Valenti, W.C. (editors), 2009. Freshwater Prawn Culture: the farming of Macrobrachium rosenbergii. Blackwell Science, Oxford, England. 512p. |
| Valenti, W.C. 1998. Carcincultura de água doce: tecnologia para a produção de camarões. FAPESP, São Paulo and IBAMA, Brasília, Brasil. 383 pp. |
| Wickins, J.F. & Lee, D.O'C. 2002. Crustacean farming: ranching and culture, 2nd Ed. Blackwell Science, Oxford, England. 446 pp. |