(Sections à l’étape 3)
Table des matières
SECTION 2 |
Définitions | |
2.3 |
Mollusques bivalves vivants et [crus] | |
2.7 |
Poisson salé | |
2.8 |
Poisson fumé | |
2.9 |
Homards et crabes | |
2.10 |
Crevettes | |
2.11 |
Céphalopodes | |
2.13 |
Transport | |
2.14 |
Vente au détail | |
SECTION 7 |
Mollusques bivalves vivants et [crus] | |
7.1 |
Généralités – supplément au Programme de conditions préalables | |
7.2 |
Classement et surveillance des zones conchylicoles | |
7.3 |
Récolte et transport des mollusques vivants | |
7.4 |
Reparcage | |
7.5 |
Épuration des mollusques dans les bacs, viviers et cadres flottants | |
7.6 |
Envoi des mollusques dans un centre d’expédition | |
7.7 |
Traitement thermique/décoquillage des mollusques dans les usines | |
7.8 |
Documents et registres | |
7.9 |
Identification des lots et procédures de retrait | |
SECTION 11 |
Transformation du poisson salé | |
11.1 |
Généralités | |
11.2 |
Préparation avant salage | |
11.3 |
Manutention du sel et prescriptions relatives au sel | |
11.4 |
Salage et maturation | |
11.5 |
Triage, pesage, emballage, empaquetage et étiquetage | |
11.6 |
Entreposage frigorifique | |
11.7 |
Emballage, étiquettes et ingrédients | |
SECTION 12 |
Transformation du poisson fumé | |
12.1 |
Pré-salage | |
12.2 |
Fumage | |
12.3 |
Tranchage des produits fumés à froid | |
12.4 |
Refroidissement et/ou congélation | |
12.5 |
Emballage des produits fumés à chaud et des produits fumés à froid | |
12.6 |
Étiquetage | |
12.7 |
Entreposage, distribution et vent au détail | |
12.8 |
Décongélation | |
SECTION 13 |
Transformation des homards et des crabes | |
13.1 |
Généralités – Supplément au programme de conditions préalables | |
13.2 |
Considérations générales pour la manutention des homards et des crabes | |
13.3 |
Opérations de transformation – homards et crabes | |
SECTION 14 |
Transformation des crevettes | |
14.1 |
Crevettes congelées - généralités | |
14.2 |
Opérations de transformation | |
14.3 |
Crevettes surgelées individuellement - décortiquées, décortiquées et déveinées, cuites ou panées | |
SECTION 15 |
Transformation des céphalopodes | |
15.1 |
Réception des céphalopodes | |
15.2 |
Entreposage des céphalopodes | |
15.3 |
Décongélation contrôlée | |
15.4 |
Tranchage, éviscération et lavage | |
15.5 |
Épiautage, parage | |
15.6 |
Calibrage/emballage | |
15.7 |
Congélation | |
15.8 |
Emballage, étiquettes et ingrédients– Réception et entreposage | |
SECTION 17 |
Transport | |
17.1 |
Pour les produits frais, réfrigérés et congelés | |
17.2 |
Pour les poissons, mollusques et crustacées en conserve | |
17.3 |
Pour les poissons, mollusques et crustacées en conserve | |
17.4 |
Pour tous les produits | |
SECTION 18 |
Vente au détail | |
18.1 |
Réception du poisson des mollusques, des crustacés et de leurs produits pour la vente au détail – généralités | |
ANNEXES |
||
Annexe I |
Conditionnement sous atmosphère modifiée | |
Annexe II |
Prescriptions facultatives concernant le produit fini - Mollusques [à terminer] | |
Annexe III |
Prescriptions relatives au produit fini – Poisson frais, congelé ou haché | |
Annexe IV |
Prescriptions relatives au produit fini – Surimi congelé | |
Annexe V |
Prescriptions relatives au produit fini – Produits de la pêche enrobés surgelés | |
Annexe VI |
Prescriptions relatives au produit fini – Poisson salé [à terminer] | |
Annexe VII |
Prescriptions relatives au produit fini – Poisson fumé [à terminer] | |
Annexe VIII |
Prescriptions relatives au produit fini – Langoustes, homards, cigales de mer et crabes [à terminer] | |
Annexe IX |
Prescriptions relatives au produit fini – Crevettes
| |
Annexe X |
Prescriptions relatives au produit fini – Céphalopodes [à terminer] | |
Annexe XI |
Prescriptions relatives au produit fini – Poisson en conserve | |
Annexe XII |
Prescriptions relatives au produit fini – Codes et Normes Codex concernant le poisson et les produits de la pêche et documents connexes | |
2.3 MOLLUSQUES BIVALVES VIVANTS ET [CRUS] | |||||
Accepté/ Acceptable/ Approuvé |
accepté par l’autorité compétente; | ||||
Dégorgement |
opération qui consiste à placer des mollusques bivalves vivants dans des bassins fixes, des viviers flottants ou des sites naturels, pour leur permettre de se débarrasser du sable, de la boue ou de la vase et, partant, améliorer l’acceptabilité du produit; | ||||
Centre de distribution |
toute installation ou tout établissement à terre ou en mer pour la réception, le dégorgement, le lavage, le nettoyage, le calibrage et l’emballage de mollusques bivalves vivants propres à la consommation humaine; | ||||
Zones conchylicoles |
bassins d’eaux saumâtres ou zones marines où la production et la récolte de mollusques bivalves sont autorisées, soit dans des gisements naturels soit dans des parcs d’élevage, destinés à la consommation humaine. Les zones conchylicoles peuvent être approuvées comme zones de production ou de récolte de mollusques bivalves pour la consommation directe ou comme zones de production ou de récolte de mollusques bivalves pour l’épuration ou le reparcage. | ||||
Décoquillage par la chaleur |
tout traitement thermique, tel que par la vapeur, l’eau chaude ou la chaleur sèche, appliqué pendant une brève durée aux mollusques bivalves pour permettre de séparer aisément et rapidement la chair de la coquille aux fins de décoquillage; | ||||
[Mollusques bivalves traités après récolte] |
[produits préparés à partir de mollusques bivalves vivants qui ont été traités après récolte pour éliminer, réduire ou limiter des organismes spécifiques se trouvant dans le produit et conserver les qualités organoleptiques d’un mollusque bivalve vivant. Comme pour les mollusques bivalves crus, les mollusques bivalves traités après récolte doivent satisfaire à tous les critères microbiologiques correspondant aux contrôles courants de l’eau de récolte pour éviter la contamination fécale et les pathogènes entériques qui y sont associés. Ces contrôles ne sont cependant pas conçus pour vérifier la présence de pathogènes comme les Vibrios qui sont indépendants de la contamination fécale.] | ||||
Épuration |
procédé consistant à réduire les micro-organismes à un niveau acceptable pour la consommation directe en mettant des mollusques bivalves vivants, pendant un certain temps, dans des conditions agréées et contrôlées, dans de l’eau de mer naturelle ou artificielle convenant à cette opération, traitée ou non; | ||||
Reparcage |
immersion dans une zone salubre agréée et sous contrôle de l’autorité compétente, de mollusques bivalves provenant d’une zone contaminée microbiologiquement, pendant le temps nécessaire pour réduire la contamination à un niveau acceptable pour la consommation humaine. | ||||
2.7 POISSON SALÉ | |||||
Baril |
Récipient cylindrique en bois ou en plastique muni d’un couvercle permettant d’en assurer l’étanchéité | ||||
Membrane noire |
Péritoine pariétal, membrane pigmentée qui tapisse la cavité abdominale | ||||
Saumure |
solution de sel et d’eau; | ||||
Injection de saumure |
injection directe de saumure dans la chair du poisson; | ||||
Saumurage |
procédé qui consiste à placer du poisson dans la saumure pendant une durée assez longue pour que les tissus de poisson absorbent une quantité importante de sel; | ||||
Salage à sec |
procédé consistant à mélanger du poisson et du sel approprié et à l’empiler de telle manière que la saumure qui en résulte s’égoutte; | ||||
Brume |
Décoloration ou développement de la moisissure Sporendonema epizoum qui affecte la surface du poisson et lui donne un aspect tacheté. La chair du poisson n’est pas affectée; | ||||
Poisson gras |
Poisson dont les principales réserves de graisse se trouvent dans le tissu cellulaire [et dont la teneur en matières grasses dépasse 2% ??] | ||||
« Gibbing » |
Procédé qui consiste à ôter les branchies, l’intestin et l’estomac d’un poisson gras comme le hareng, en insérant un couteau ou en introduisant la main dans les branchies; on laisse dans le poisson les œufs ou la laitance et une partie du caecum pylorique; | ||||
Poisson fortement salé |
la teneur en sel des muscles du poisson est supérieure à 20 g/100 g en phase aqueuse; NOTE: N’EST PAS UTILISÉ DANS LE TEXTE | ||||
Poisson moyennement salé |
la teneur en sel des muscles du poisson est supérieure à 10 g/100 g en phase aqueuse ou inférieure ou égale à 20 g de sel/100 g d’eau; NOTE: N’EST PAS UTILISÉ DANS LE TEXTE | ||||
Poisson maigre (Poisson blanc) |
Poisson dans lequel les principales réserves de graisse se trouvent dans le foie [et dont le tissu cellulaire contient moins de 2 % de graisse)] | ||||
Poisson légèrement salé |
la teneur en sel des muscles du poisson est supérieure à 4 g/100 g en phase aqueuse ou est inférieure ou égale à 10 g de sel/100 g d’eau; NOTE: N’EST PAS UTILISÉ DANS LE TEXTE ? | ||||
Maturation |
Procédé qui consiste à saler le poisson jusqu’à ce qu’il atteigne le stade salé maturé | ||||
« Nobbing » |
Procédé qui consiste à enlever la tête et les viscères d’un poisson gras, comme le hareng, en une seule opération en sectionnant partiellement la tête et en tirant les branchies auxquelles les viscères restent attachés; on laisse dans le poisson les œufs ou la laitance | ||||
Marinade |
Saumure pouvant contenir du vinaigre et des épices; | ||||
Rougissement |
Décoloration provoquée par la bactérie halophile rouge qui endommage la chair du poisson | ||||
Sel |
produit cristallin composé principalement de chlorure de sodium. On l’extrait de la mer, des dépôts de sel dans les roches souterraines ou de la saumure transformée et raffinée sous vide; | ||||
Poisson salé fermenté |
poisson conservé dans du sel; NOTE: N’EST PAS UTILISÉ DANS LE TEXTE | ||||
Poisson salé maturé |
poisson salé qui a l’aspect, la consistance et la saveur caractéristiques du produit fini; | ||||
Poisson ou filet de poisson salé |
poisson/filets de poisson qui ont été traités par saumurage, injection de saumure, salage à sec, salage en saumure ou par une combinaison de ces traitements; | ||||
Saturée |
La phase aqueuse du muscle de poisson est saturée avec du sel (26,4 g sel/100g phase aqueuse); | ||||
Poisson tranché |
poisson qu’on a ouvert depuis la gorge ou le collet jusqu’à la queue, pour retirer les branchies, les viscères et les œufs ou la laitance. On peut laisser ou ôter la tête et tout ou partie de l’arête dorsale; | ||||
Empilage (réempilage) |
Opération qui consiste à empiler le poisson en recouvrant uniformément la surface de sel. | ||||
Poisson très légèrement salé |
La teneur en sel des muscles de poisson est de 4g/100g ou moins en phase aqueuse Note: N’EST PAS UTILISÉ DANS LE TEXTE | ||||
Salage humide (salage en saumure) |
procédé dans lequel du poisson en général maigre est mélangé à du sel de qualité appropriée et entreposé dans des récipients étanches dans la saumure qui se forme par dissolution du sel dans l’eau extraite du liquide cellulaire des tissus de poisson. On peut ajouter de la saumure dans le récipient. On enlève ensuite le poisson du récipient et on l’empile de manière à ce qu’il s’égoutte. | ||||
2.8 POISSON FUMÉ | |||||
Fumage à froid |
Traitement par la fumée à une température inférieure à celle où la chair du poisson serait dénaturée par la chaleur; | ||||
Fumage à chaud |
Traitement par la fumée à une température permettant la dénaturation complète de la chair du poisson; | ||||
Fumage mécanique |
méthode de fumage où la fumée est produite à l’extérieur du fumoir et un courant forcé de fumée passe autour du poisson par ventilation artificielle; | ||||
Fumée |
mélange de particules et gouttelettes dans les gaz provenant de la combustion du bois. On peut séparer la fumée du goudron avant de l’envoyer dans le fumoir; | ||||
Fumoir traditionnel |
enceinte fermée comme un foyer ou une cheminée où la fumée se forme sous les poissons et peut circuler autour d’eux sous l’effet du tirage naturel; | ||||
Bois |
bois, dont la sciure de bois et les copeaux, les plantes ligneuses à l’état sec ou naturel. Les bois ou plantes ligneuses peints, imprégnés ou ayant subi un autre traitement ne peuvent être utilisés pour la production de fumée. | ||||
2.9 HOMARDS ET CRABES | |||||
Autolyse |
décomposition ou détérioration de la chair ou des viscères des crustacés sous l’action des enzymes présentes ; | ||||
Procédés discontinus |
méthodes de transformation supposant la transformation du crabe en lot; | ||||
Tâche noire |
apparition d’une pigmentation sombre aux articulations et aux parties ayant subi des lésions entre les segments des homards, causée par réaction enzymatique d'oxydation; | ||||
Parage |
Processus consistant à enlever le bouclier, les viscères et les branchies. Dans certaines pêcheries, il peut également comporter l’ablation des pattes et des pinces. Le parage peut avoir lieu avant ou après la cuisson ; | ||||
Extrémité antérieure de la queue |
partie du muscle caudal du homard qui se prolonge dans le céphalothorax ; | ||||
Carpe |
deuxième segment de la patte à partir de l’épaule du crabe; NOTE: N’EST PAS UTILISÉ DANS LE TEXTE | ||||
Céphalothorax |
partie du corps d’un homard constituée, du point de vue anatomique, par la fusion de la tête et du thorax ; | ||||
Pince |
appendice situé à l’extrémité de la patte antérieure du crabe ou du homard; | ||||
Pince-cocktail |
Produit constitué de pinces de crabe dont la carcasse a été partiellement enlevée pour découvrir la chair ; | ||||
Cuisson |
opération consistant à faire bouillir les crustacées dans de l’eau potable, de l’eau de mer propre ou de la saumure ou à les faire chauffer à la vapeur pendant un temps suffisant pour que leur centre thermique atteigne une température propre à permettre la coagulation des protéines ; | ||||
Crabe |
espèces de l’ordre des Décapodes, sections des Brachyoures et des Anomoures, commercialement importantes | ||||
Dactyle |
dernier segment de la patte d’un crabe. NOTE: N’EST PAS UTILISÉ DANS LE TEXTE | ||||
Détérioration |
processus naturels de réduction de qualité qui apparaissent après la récolte et qui sont totalement indépendant de l’intervention délibérée de l’homme ; | ||||
Déveiner |
retirer l’intestin/la veine de la queue du homard ; | ||||
Queue désarticulée |
défaut observé chez les homards cuits, morts ou altérés avant d’être transformés. La queue de l’animal ne se recourbe pas et l’on observe un vide entre la queue et le céphalothorax; NOTE: N’EST PAS UTILISÉ DANS LE TEXTE | ||||
Activité enzymatique |
action catalytique des enzymes sur les réactions biochimiques ; | ||||
Insensible |
état caractérisé par l’absence de réaction des homards ou des crabes résultant d’un procédé thermique, électrique ou physique appliqué aux homards ou aux crabes avant cuisson. | ||||
Intestin/Veine |
utilisé dans le présent code pour indiquer la portion postérieure du tube digestif du homard; | ||||
Bouts des pattes |
troisième segment des pattes en comptant à partir de la carapace du crabe; | ||||
Homard |
Espèces commercialement importantes de l’ordre des Decapoda, et familles des Nephropidae, Palinuridae ou Scyllaridae ou autres familles taxonomiques économiques importantes; | ||||
« Loose neck » |
a la même signification dans certaines régions que “Queue désarticulée”; NOTE: N’EST PAS UTILISÉ DANS LE TEXTE | ||||
Mérus |
premier segment de la patte à compter de l’épaule du crabe; NOTE: N’EST PAS UTILISÉ DANS LE TEXTE | ||||
Pasteurisation |
procédé consistant à soumettre la chair des crustacées à la chaleur pendant des temps et températures qui détruisent une forte proportion de micro-organismes sans modification notable de l’apparence, de la texture et de la saveur du produit; | ||||
Décorticage |
procédé, qui peut être mécanique ou manuel, consistant à retirer la chair des crabes; | ||||
Parcage |
opération consistant à conserver les crabes et homards vivants dans des bacs ou des viviers flottants pour une période prolongée; | ||||
Propodus |
troisième segment de la patte à compter de l’épaule du crabe; NOTE: N’EST PAS UTILISÉ DANS LE TEXTE | ||||
Sections |
parties nettoyées du crabe, dont les viscères et les branchies ont été supprimées et comprennent en général la moitié du crabe avec les pattes motrices et la pince qui y sont attachées; | ||||
Secouage |
méthode industrielle d’extraction manuelle de la chair utilisée pour le crabe royal, le crabe de Tanner et le dormeur du Pacifique. Les sections cuites sont frappées ou secouées pour extraire la chair; | ||||
Carapace |
enveloppe dure qui recouvre les homards et les crabes; | ||||
Épaule |
section contenant la chair dans le corps du crabe; | ||||
Décorticage |
procédé qui consiste à retirer la chair de la carapace et des appendices des homards; | ||||
Queue |
chez les crustacés, il s’agit de l’abdomen ou de la partie postérieure du corps; | ||||
Équeutage |
opération qui consiste à séparer la queue du céphalothorax; | ||||
Parage |
opération qui consiste à retirer tous les signes de sang, de membrane ou de restes d’intestin pouvant être attachés à la carapace ou à la chair des homards. | ||||
Viscères |
contenus de l’intestin des crabes; | ||||
Déchets |
parties du crabe ou du homard restant une fois la chair ôtée. | ||||
2.10 CREVETTES | |||||
Étêtage |
opération qui consiste à enlever la tête de la crevette; | ||||
Crevette déveinée |
crevette décortiquée dont le dos des segments décortiqués a été ouvert et l’intestin (« veine ») ôté; | ||||
Crevette fraîche |
crevette capturée depuis peu qui n’a pas subi de traitement de conservation ou qui a été conservée uniquement par réfrigération. N’inclut pas les crevettes cuites récemment; | ||||
Crevette décortiquée |
crevette dont la tête et la carapace ont été enlevées; | ||||
Crevette crue étêtée |
crevette crue étêtée mais avec sa carapace; | ||||
Crevette |
Dans le présent code, toutes les espèces commercialisées de crustacées désignées sous le nom de "crevette" des familles de Penaeidae, Pandalidae, Palaemonidae et Crangonidae; | ||||
2.11 CÉPHALOPODES | |||||
Tranchage |
opération consistant à fendre le céphalopode le long du manteau afin d’en obtenir un seul filet. | ||||
2.13 TRANSPORT | |||||
2.14 VENTE AU DÉTAIL | |||||
Vente au détail |
opération qui consiste à entreposer, préparer, emballer, servir ou fournir de toute autre manière des poissons, des mollusques bivalves, des crustacées et leurs produits directement au consommateur qui les préparera pour sa consommation. Il peut s’agir de marchés de poissons indépendants, de sections spécialisées dans des magasins d’alimentation générale ou des grands magasins, de produits emballés réfrigérés ou congelés et/ou de poissonneries à service complet. | ||||
Emballé |
le produit est emballé à l’avance et exposé réfrigéré ou congelé pour que le consommateur se serve directement. | ||||
Présentation en étalage |
présentation en étalage des poissons, mollusques, crustacées et leurs produits réfrigérés pour être pesés et emballés par le personnel de l’établissement à la demande du consommateur. | ||||
SECTION – 7 – MOLLUSQUES BIVALVES VIVANTS ET [CRUS]
En ce qui concerne les contrôles à effectuer aux différentes étapes de transformation, cette section donne des exemples de dangers et de défauts potentiels et des conseils techniques qui pourront servir pour élaborer des mesures de maîtrise et des actions correctives. À chaque étape, seuls sont énumérés les dangers et les défauts qui peuvent être introduits ou maîtrisés à cette même étape. Il convient de noter que, lors de la mise au point d’un plan HACCP et/ou DAP, il est indispensable de consulter la section 5 où l’on trouve des conseils pour l’application des principes HACCP et de l’analyse DAP. Cependant, dans le cadre du présent code, il est impossible d’indiquer en détail les seuils critiques, la surveillance, la tenue des registres et la vérification relatifs à chaque étape, car ils diffèrent selon les dangers et défauts.
[Le diagramme ci-après est présenté uniquement à titre d’exemple. Pour mettre en œuvre un plan HACCP, un diagramme complet et détaillé devra être établi pour chaque produit.]
Les références indiquent les sections correspondantes du présent code.
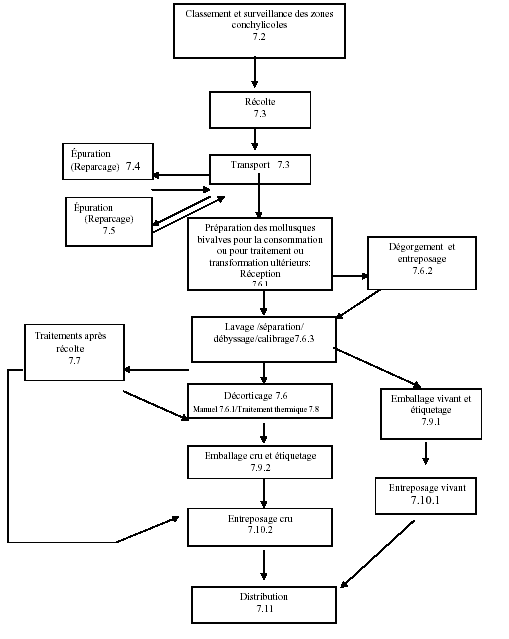
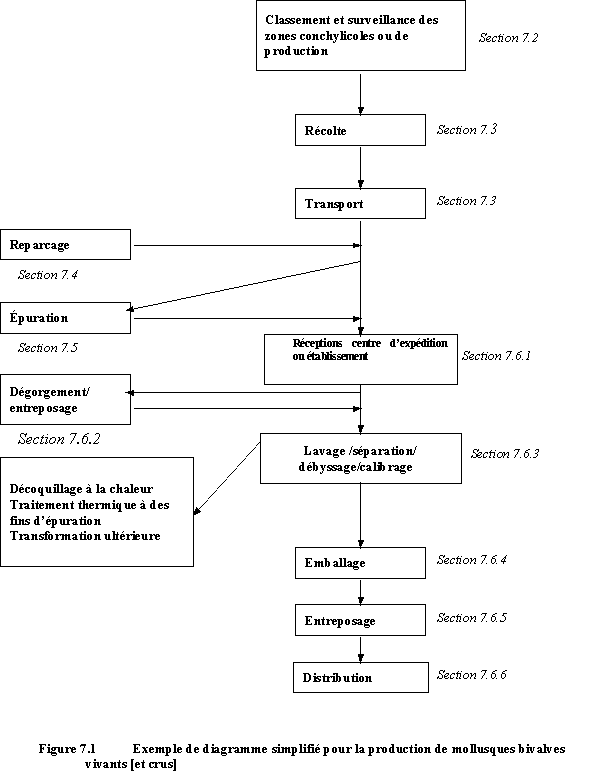
7.1 GÉNÉRALITÉS - SUPPLÉMENT AU PROGRAMME DE CONDITIONS PRÉALABLES
Les espèces de mollusques bivalves comme les huîtres, les moules, les palourdes et les clams à coquille dure peuvent survivre hors de l’eau durant des périodes prolongées et être vendues pour la consommation humaine comme animaux vivants. D’autres espèces comme les coques peuvent être commercialisées vivantes si elles sont manipulées avec soin, mais, habituellement, elles sont transformées. Les espèces non adaptées à un milieu sec meurent une fois hors de l’eau et sont de préférence traitées comme produits réfrigérés ou transformées.
Au moment de la ponte (après « maturation des gonades »), il est déconseillé et, dans de nombreux cas impossible, de les commercialiser comme animaux vivants. Le stress peut provoquer la ponte.
Les principaux dangers qui menacent la production de mollusques bivalves sont la contamination microbiologique des eaux dans lesquelles ils se développent, notamment quand ils sont destinés à être consommés crus. Étant donné que les mollusques sont des filtreurs, ils peuvent accumuler des contaminants dans des concentrations supérieures à celles qui se trouvent dans l’eau ambiante. Dans les zones conchylicoles, la contamination par des bactéries et des virus est donc décisive pour les spécifications concernant les produits finis et détermine les prescriptions à respecter pour une transformation ultérieure. La gastro-entérite et d’autres maladies graves comme l’hépatite peuvent se produire à la suite d’une contamination par les ruissellements des terres agricoles et/ou les eaux d’égout, par exemple par des pathogènes bactériens et/ou viraux entériques (virus du type Norwalk, virus causant l’hépatite) ou de pathogènes bactériens d’origine naturelle (Vibrio spp.). Les biotoxines sont également un danger. Les biotoxines produites par certaines algues peuvent provoquer diverses formes d’empoisonnement graves comme l’intoxication diarrhéique par les mollusques (IDM), l’intoxication paralysante par les mollusques (IPM), l’intoxication neurotoxique par les mollusques (INM), l’intoxication amnésique par les mollusques (IAM) ou azaspiracide (AZP). Les substances chimiques, comme les métaux lourds, les pesticides, les composés organochlorés, les substances pétrochimiques peuvent aussi constituer un danger dans certaines zones.
Afin de maîtriser les dangers, l’identification et la surveillance des zones conchylicoles sont très importantes pour la salubrité des mollusques bivalves. L’identification, le classement et la surveillance de ces zones sont du ressort des autorités compétentes en coopération avec les pêcheurs et les principaux producteurs. En attendant de disposer de meilleures méthodes, on considère les coliformes fécaux/E.coli ou les coliformes totaux comme un indicateur de la présence éventuelle de pathogènes bactériens et viraux. Si on détecte des biotoxines dans la chair des mollusques bivalves en quantités dangereuses, la zone conchylicole sera interdite pour la récolte jusqu’à ce qu’une étude toxicologique ait démontré clairement que la chair des mollusques bivalves ne contient pas de biotoxines en concentrations dangereuses. Les substances chimiques dangereuses ne devraient pas être présentes en quantités telles que l’apport alimentaire calculé dépasse la dose journalière admissible.
Les mollusques bivalves provenant d’eaux sujettes à une contamination microbiologique faible, déterminée par les autorités compétentes, peuvent être rendus salubres moyennant le reparcage dans une zone appropriée ou par un processus d’épuration qui réduira la quantité de bactéries et de virus si le processus dure assez longtemps, ou par traitement thermique qui détruira les agents pathogènes. L’épuration est un procédé de brève durée couramment appliqué pour réduire une contamination bactérienne peu importante, mais si le risque de contamination virale est élevé, la durée du reparcage devra être plus longue.
En particulier lorsque les mollusques bivalves doivent être soumis au reparcage ou à l’épuration pour être consommés crus, le stress et les chocs excessifs doivent être évités. Cela est très important car ces mollusques bivalves devraient pouvoir assurer à nouveau leurs fonctions durant l’épuration, le reparcage ou le dégorgement.
On considère que de nombreuses espèces de mollusques bivalves, mais pas toutes les espèces, sont adaptées à l’épuration.
7.2 CLASSEMENT ET SURVEILLANCE DES ZONES CONCHYLICOLES
Dangers potentiels: |
Agents pathogènes microbiologiques, biotoxines, contamination chimique. |
Défauts potentiels: |
peu probables |
Conseils techniques: |
|
Il y a 5 types différents de dangers importants venant des zones de production de mollusques bivalves:
• bactéries pathogènes entériques;
• bactéries pathogènes virales (virus du type Norwalk, virus causant l’hépatite);
• bactéries pathogènes d’origine naturelle (espèce Vibrio);
• biotoxines (IDM, IPM, INM, IAM);
• contaminants chimiques.
7.2.1 Classement des zones conchylicoles
Il faudrait étudier la zone conchylicole, le littoral ou le bassin hydrographique de façon à déterminer les sources de pollution, aussi bien ménagère qu’industrielle, qui pourraient affecter la qualité des eaux des zones conchylicoles et des mollusques bivalves. Ces sources pourraient comprendre les déversements d’égouts municipaux, les déchets industriels, les rebuts miniers, les contaminants géophysiques, les enclos pour animaux domestiques, les centrales nucléaires, les raffineries, etc. Les aspects hygiéniques devraient être réévalués en fonction des déplacements de population et des changements dans les activités agricoles et industrielles intervenant dans la zone côtière. Ces études devraient être programmées selon une fréquence acceptable et les sources connues de pollution devraient être réévaluées à intervalles réguliers afin de déterminer toute évolution de leur impact sur la zone conchylicole.
Après avoir identifié et évalué les sources de pollution, il faudrait créer des stations d’échantillonnage pour l’eau, les mollusques bivalves et/ou les sédiments et entreprendre des études pour déterminer les effets des polluants sur la qualité de l’eau et des mollusques bivalves. Les données recueillies devraient être évaluées par l’autorité compétente et les zones conchylicoles devraient être classées en fonction des normes et critères officiels.
En interprétant ces données, l’autorité compétente devrait tenir compte des variations susceptibles d’affecter le niveau de la pollution quand les conditions hydrographiques et climatiques sont les plus défavorables sous l’influence des précipitations, des marées, des vents, des méthodes de traitement des eaux usées, des changements démographiques et d’autres facteurs locaux, étant donné que les mollusques bivalves répondent rapidement à une augmentation du nombre de bactéries ou de virus dans leur environnement en accumulant ces agents. L’autorité compétente devrait également tenir compte du fait que les mollusques bivalves ont la propriété d’accumuler dans leur chair des substances chimiques toxiques dans des concentrations supérieures à celles qui se trouvent dans l’eau ambiante. Les normes établies par la FAO, l’OMS ou toute autre norme internationale ou nationale applicable aux denrées alimentaires peuvent servir de guide à l’établissement de niveaux acceptables.
L’autorité compétente devrait faire immédiatement part des décisions concernant le classement des zones conchylicoles aux producteurs, aux stations d’épuration et aux centres de distribution intéressés.
Lorsque les limites fixées pour un danger biologique ou chimique dans la spécification concernant le produit fini sont dépassées, des mesures appropriées doivent être prises sous la responsabilité de l’autorité compétente.
Les zones conchylicoles devraient être clairement déterminées par l’autorité compétente comme convenant à la récolte pour:
- la consommation humaine directe;
- le reparcage dans des eaux acceptables ou l’épuration dans un centre d’épuration agréé ou d’autres formes de traitement approuvées par exemple, un traitement thermique ou les rayonnements U.V;
- elles ne conviennent pas à l’élevage ni à la récolte des mollusques.
La présence de pathogènes Vibrio ou de virus n’est pas en corrélation avec les organismes bactériens utilisés comme indicateurs de la contamination fécale.
7.2.2 Surveillance des zones conchylicoles
Les zones conchylicoles devraient faire l’objet de contrôles réguliers afin de déceler d’éventuels changements dans la qualité de l’eau et/ou des mollusques, et les zones de qualité inférieure devraient être surveillées afin d’empêcher qu’on y récolte des mollusques à des fins autres que celles qui ont été fixées par l’autorité compétente.
La présence de biotoxines dans les mollusques bivalves peut-être due au plancton contenant des toxines. À des fins d’alerte rapide, il est recommandé de mettre en place un programme permettant de surveiller la présence dans les zones conchylicoles d’espèces de plancton susceptibles de produire des toxines et de reconnaître à d’autres signes ambiants qu’un épisode toxique risque de se développer.
Les substances chimiques dangereuses ne devraient pas être présentes en quantités telles que l’apport journalier calculé dépasse la dose journalière admissible. Un système de surveillance des substances chimique dangereuses devrait être en place.
Lorsque les programmes de surveillance continue ou les réévaluations indiquent que la zone conchylicole ne répond plus aux critères de classement, l’autorité compétente devrait reclasser la zone ou y interdire immédiatement la récolte.
En déterminant l’innocuité des zones conchylicoles classées pour la santé publique, l’autorité compétente devrait prendre les mesures suivantes:
- Classement/reclassement des zones conchylicoles par une étude sanitaire, une surveillance régulière des coliformes fécaux/E.coli ou des coliformes totaux, et autres mesures de contrôle sanitaire appropriées.
- Classement/reclassement des zones conchylicoles par une surveillance régulière des pathogènes dans la chair des mollusques bivalves (voir 7.2.2.2).
- Fermeture/réouverture des zones conchylicoles par la surveillance des biotoxines dans les mollusques bivalves ou en association avec la surveillance du phytoplancton dans l’eau de mer à une fréquence appropriée en fonction du risque de contamination.
- Contrôle des contaminants chimiques.
Sous la responsabilité de l’autorité compétente, les zones conchylicoles fournissant des mollusques bivalves destinés à la consommation humaine directe répondent aux prescriptions suivantes au moment de la récolte:
- la zone n’est pas sujette à une contamination qui pourrait présenter un danger réel ou potentiel pour la santé humaine;
- les mollusques bivalves récoltés répondent à la spécification concernant le produit fini.
Les zones conchylicoles fournissant des mollusques bivalves pour la consommation humaine indirecte devraient être définies par rapport au traitement ultérieur que doit subir le lot.
7.2.2.1 Coliformes fécaux/E. Coli/coliformes totaux
Toutes les zones conchylicoles devraient faire l’objet de contrôles fréquents afin de déceler la présence de coliformes fécaux/ E. Coli ou de coliformes totaux.
Il faudrait effectuer des analyses portant sur les bactéries indicatrices telles que les coliformes fécaux ou Escherichia coli ou les coliformes totaux, afin de déterminer le degré de contamination fécale. Il faudrait contrôler de manière continue que les bactéries indicatrices utilisées permettent une mesure fiable de la contamination fécale. Si celle-ci dépasse un certain seuil l’autorité compétente pourra autoriser le reparcage ou l’épuration dans une zone appropriée pendant une période fixée.
Les coliformes fécaux/E.coli ou les coliformes totaux peuvent être utilisés comme un indicateur de la présence de pathogènes bactériens entériques, de pathogènes viraux entériques ou de pathogènes bactériens d’origine naturelle.
[Les bactériophages et la détection virale pourraient aussi être utilisés comme indicateurs lorsque des méthodes d’analyse validées seront disponibles]
7.2.2.2 Surveillance des pathogènes
Les programmes sanitaires concernant les mollusques reposent sur l’utilisation d’organismes indicateurs de la présence de contamination plutôt que sur la surveillance de pathogènes spécifiques. Cependant, dans le cas d’incident épidémique causé par un pathogène identifié comme la Salmonella, il peut être utile de contrôler la chair des mollusques dans le cadre du processus de levée d’interdiction de la zone de récolte concernée. L’espèce et, en règle générale la souche proprement dite, devraient être connues pour garantir que le contrôle porte bien sur la source du pathogène. Des niveaux d’acceptation et de rejet du pathogène devraient avoir été fixés afin d’utiliser ces résultats de surveillance pour prendre les décisions. La zone concernée restera interdite tant que d’autres conditions y compris les prescriptions de l’enquête sanitaire n’auront pas été remplies.
7.2.2.3 Surveillance des biotoxines marines
Toutes les zones conchylicoles devraient faire l’objet de contrôles réguliers afin de déceler la présence d’algues pouvant produire des biotoxines marines et de biotoxines marines, le cas échéant. Le risque de prolifération d’algues toxiques est variable selon la saison et les zones peuvent être également affectées par des algues toxiques inconnues jusque là dans la mer ou les eaux côtières ambiantes. Il faudrait tenir compte de ces risques en établissant les plans de surveillance.
L’autorité compétente devrait interdire immédiatement et surveiller de près les zones où des niveaux inadmissibles ont été observés dans les parties comestibles des mollusques bivalves. Les zones devraient être interdites jusqu’à ce que l’analyse toxicologique ait montré clairement que la chair des mollusques bivalves ne contient pas de biotoxines en quantités dangereuses.
L’autorité compétente devrait faire immédiatement part de ces décisions aux producteurs, aux stations d’épuration et aux centres de distribution intéressés.
7.2.2.4 Contaminants chimiques
Il faudrait surveiller à intervalles réguliers les contaminants chimiques présents dans les zones conchylicoles.
7.3 RÉCOLTE ET TRANSPORT DES MOLLUSQUES BIVALVES VIVANTS
Voir aussi Sections 3.1, 3.3, 3.4 et 3.5
Cette section s’applique au transport de mollusques bivalves destinés à la consommation humaine directe, à une transformation ultérieure, au reparcage et à l’épuration.
Les procédures de manipulation sont fonction des espèces, de la zone conchylicole et de la saison.
Dangers potentiels: |
Agents pathogènes microbiologiques, biotoxines, contamination chimique |
Défauts potentiels: |
Dommages physiques |
Conseils techniques: |
|
• Les dragues et autre matériel de capture, les ponts, les cales et les récipients qui sont contaminés à la suite de leur utilisation dans une zone polluée, devraient être nettoyés, et au besoin, désinfectés avant d’être utilisés pour des mollusques bivalves provenant d’une zone non polluée.
• Les cales où sont placés les mollusques bivalves ou les récipients devraient être conçus de telle manière que les mollusques bivalves soient surélevés par rapport au niveau du sol et le système d’écoulement devrait empêcher tout contact avec les eaux de lavage, l’eau de cale ou l’eau intervalvaire. Au besoin, on installera un système de pompage de l’eau de cale.
• Des précautions judicieuses devraient être prises pour protéger les mollusques bivalves de la contamination par de l’eau polluée, les déjections d’oiseaux marins, les chaussures, bottes, etc. ayant été en contact avec des matières fécales ou d’autre matériel pollué.
• Les pompes servant à amener l’eau de lavage devraient puiser uniquement de l’eau de mer non contaminée.
• Les mollusques bivalves devraient être récoltés et placés dans une zone conchylicole ou une zone de reparcage agréées par l’autorité compétente.
• Après avoir été retirés de l’eau, ou pendant la manipulation et le transport, les mollusques bivalves ne devraient pas être soumis à des températures extrêmes ni à des variations brutales de température. Le contrôle de la température est déterminant dans la manipulation des mollusques bivalves vivants. Un matériel spécial, par exemple des récipients isothermes et du matériel de réfrigération, devrait être utilisé si la température ambiante et la durée des opérations l’exigent. Les mollusques bivalves ne devraient pas être exposés au plein soleil ou à des surfaces chauffées par le soleil, ni entrer directement en contact avec de la glace ou d’autres surfaces glacées, non plus qu’être maintenus dans des conteneurs clos renfermant de la neige carbonique. En général, on évitera d’entreposer les mollusques à plus de 10o C (50o F) et à moins de 2o C (35o F).
• Aussitôt après avoir été récoltés, les mollusques bivalves devraient être débarrassés de l’excès de vase et d’algues qui les recouvrent au moyen d’un jet suffisamment puissant d’eau de mer propre ou d’eau potable. L’eau de lavage ne devrait pas pouvoir couler sur les mollusques bivalves qui ont déjà été nettoyés. L’eau ne devrait pas être recyclée.
• L’intervalle compris entre la récolte et l’immersion dans l’eau en vue du reparcage, de l’entreposage ou de l’épuration devrait être aussi court que possible. Cela s’applique également à l’intervalle entre la fin de la récolte et la manutention dans un centre de distribution.
• Si les mollusques bivalves doivent être replongés dans l’eau après la récolte, il devra s’agir d’eau de mer propre.
• Les documents appropriés concernant les activités de récolte et de transport devraient être établis.
7.4 REPARCAGE
Les prescriptions concernant le classement et la surveillance des zones conchylicoles s’appliquent également aux zones de reparcage.
Le reparcage vise à réduire la quantité de contaminants biologiques que pourraient contenir les mollusques bivalves qui ont été récoltés dans des zones contaminées à des niveaux tels que les mollusques bivalves seront propres à la consommation humaine sans subir de traitement ultérieur. Les mollusques bivalves destinés à être reparqués ne devraient être récoltés que dans des zones qui ont été classées/désignées telles par l’autorité compétente.
Dangers potentiels: |
Pathogènes microbiologiques, biotoxines, contamination chimique. |
Défauts potentiels: |
peu probables. |
Conseils techniques: |
|
• Les opérations de reparcage devraient se faire sous le contrôle rigoureux de l’autorité compétente pour empêcher que des mollusques bivalves contaminés ne soient directement envoyés sur les marchés ou ne contaminent d’autres mollusque bivalves. Les limites des zones de reparcage devraient être indiquées clairement par des balises flottantes, des poteaux ou d’autres moyens.
• L’autorité compétente fixera la durée de rétention et la température minimale dans la zone agréée jusqu’au moment de la récolte, compte tenu du degré de contamination avant le reparcage, de la température de l’eau, de l’espèce des mollusques bivalves en cause ainsi que des conditions géographiques ou hydrographiques locales.
• Les mollusques bivalves devraient être répartis selon une densité qui leur permette de s’ouvrir et de subir une épuration naturelle.
• Les documents appropriés concernant les opérations de reparcage devraient être établis.
7.5 ÉPURATION DES MOLLUSQUES BIVALVES DANS LES BACS, VIVIERS ET CADRES FLOTTANTS
Voir aussi Sections: 3.2, 3.3, 3.4 et 3.5
L’épuration vise à réduire le nombre de bactéries pathogènes que pourraient contenir les mollusques bivalves qui ont été récoltés dans des zones modérément polluées à des niveaux tels que les mollusques seront propres à la consommation humaine sans subir de traitement ultérieur. L’épuration seule ne suffit pas pour nettoyer des mollusques bivalves provenant de zones fortement contaminées ou de zones sujettes à contamination par des hydro-carbures, des métaux lourds, des pesticides ou des biotoxines. Les mollusques bivalves destinés à être épurés ne devraient être récoltés que dans des zones désignées/classées comme telles par l’autorité compétente.
Les conditions requises varient selon l’espèce du mollusque et la conception du système d’épuration.
Pour que les mollusques assurent leurs fonctions naturelles, et par conséquent, puissent être épurés, il est indispensable qu’ils ne subissent ni stress ni chocs excessifs durant la récolte ou la manutention jusqu’au moment de l’épuration et ne se trouvent pas dans un état de faiblesse passagère ou en phase de ponte.
Les centres d’épuration devraient respecter les mêmes normes d’hygiène que celles énoncées aux sections 3.2, 3.3, 3.4, 3.5.
Dangers potentiels: |
Agents pathogènes microbiologiques |
Défauts potentiels: |
Dommages physiques |
Conseils techniques: |
|
Les stations d’épuration et les bacs doivent être agréés par l’autorité compétente.
• Les mollusques bivalves soumis à l’épuration ne devraient pas contenir d’ions métalliques, de pesticides, de déchets industriels ou de biotoxines marines dans des quantités susceptibles de présenter un risque pour la santé du consommateur.
• N’utiliser que les stocks approuvés par l’autorité compétente.
• Le procédé et le matériel, les bacs, viviers et cadres flottants utilisés pour l’épuration devraient être approuvés par l’autorité compétente.
• Les mollusques bivalves affaiblis ou morts devraient être éliminés avant l’opération d’épuration, chaque fois que possible. Les coquilles devraient être débarrassées de la vase et des épibiontes mous. Le cas échéant, on lavera les mollusques bivalves avec de l’eau de mer propre ou de l’eau potable avant de les épurer.
• La durée de l’opération devrait être adaptée à la température de l’eau et aux paramètres physiques de la qualité de l’eau (eau de mer propre, salinité, niveaux d’oxygène dissous et de Ph permettant aux mollusques bivalves d’assurer leurs fonctions normalement), au degré de contamination avant l’épuration et à l’espèce du mollusque bivalve. Il faudrait effectuer une analyse microbiologique de l’eau de traitement et de la chair des mollusques bivalves afin d’évaluer les paramètres d’épuration. Il faudrait tenir compte du fait que les virus et Vibrio spp. sont plus persistants durant l’épuration que les bactéries indicatrices utilisées principalement pour la surveillance microbiologique (coliformes fécaux et E. coli).
• L’eau utilisée dans les réservoirs d’épuration devrait être renouvelée continuellement ou à des intervalles convenables ou, si elle est recyclée, être traitée correctement. Le débit de l’eau à l’heure devrait suffire pour la quantité de mollusques bivalves traités et être adapté au degré de contamination des mollusques bivalves.
• Les mollusques bivalves en cours d’épuration devraient rester immergés dans de l’eau de mer propre jusqu’à ce qu’ils répondent aux conditions d’hygiène exigées par l’autorité compétente.
• Les mollusques bivalves devraient être répartis selon une densité qui leur permette de s’ouvrir et de subir une épuration naturelle.
• La température de l’eau, durant le traitement d’épuration, ne devrait pas descendre au-dessous du minimum nécessaire pour que les mollusques bivalves conservent une activité physiologique; il conviendrait d’éviter que l’eau atteigne une température élevée, qui aurait une influence défavorable sur le rythme de pompage et le processus d’épuration; les réservoirs devraient, au besoin, être protégés des rayons directs du soleil.
• L’équipement en contact avec l’eau, c’est-à-dire les bacs, les pompes, les tuyaux et canalisations et tout autre équipement, devraient être fabriqués en matériaux non poreux et non toxiques. Le cuivre, le zinc, le plomb et leurs alliages, ne devraient pas, de préférence, être utilisés dans la construction des bacs, pompes et canalisations d’épuration.
• Pour éviter la recontamination des mollusques bivalves en cours d’épuration, il ne faudrait pas immerger dans le même bac des mollusques bivalves non épurés.
• Après leur retrait des bassins d’épuration, les mollusques bivalves devraient être lavés avec de l’eau potable ou de l’eau de mer propre, et être traités de la même manière que les mollusques bivalves vivants provenant d’une zone non polluée. Les mollusques bivalves morts, avec des coquilles brisées ou tout autre défaut devraient être éliminés.
• Avant de retirer les mollusques bivalves des bacs, il faudrait drainer l’eau du système pour éviter une nouvelle suspension et une réingestion. Les bacs devraient être nettoyés après chaque utilisation et désinfectés à des intervalles appropriés.
• Après le traitement d’épuration, les mollusques doivent satisfaire aux spécifications concernant les produits finis.
• Les documents appropriés concernant l’épuration devraient être établis.
7.6 [TRANSFORMATION DES MOLLUSQUES BIVALVES DANS UN CENTRE DE DISTRIBUTION OU DANS UN ÉTABLISSEMENT]
Les centres de distribution devraient observer les mêmes normes d’hygiène que celles énoncées aux sections 3.2, 3.3, 3.4, 3.5.
7.6.1 Réception
Dangers potentiels: |
Pathogènes microbiologique, contamination chimique et physique, parasites viables |
Défauts potentiels: |
Dommages physiques, matières étrangères, mollusques bivalves morts ou en train de mourir |
Conseils techniques: |
|
• Les mollusques bivalves expédiés par un centre de distribution doivent quitter le centre vivants. Il faut donc leur éviter le stress et les chocs excessifs.
• Les centres de distribution ne devraient accepter que les mollusques bivalves qui satisfont aux spécifications concernant les produits finis et qui proviennent directement de zones conchylicoles agréées ou qui ont été reparqués dans une zone de reparcage agréée ou épurés dans une station d’épuration ou des bacs approuvés.
7.6.2 Dégorgement et entreposage des mollusques dans des réservoirs d’eau de mer, bassins, etc.
Voir aussi les sections 3.2, 3.3, 3.4 et 3.5
Dangers potentiels: |
Pathogènes microbiologiques, contamination chimique, biotoxines |
Défauts potentiels: |
Dommages physiques, matières étrangères, mollusques bivalves morts ou en train de mourir |
Conseils techniques: |
|
On entend par dégorgement l’entreposage des mollusques en eau de mer dans des bacs, bassins, viviers, cadres flottants ou sites naturels en vue d’éliminer la boue, le sable et le mucus.
• Les mollusques bivalves peuvent être entreposés en eau de mer dans des bacs, des bassins, des cadres, des viviers flottants ou des sites naturels si le procédé est agréé par l’autorité compétente.
• Seule l’eau de mer propre devrait être utilisée dans les bacs, viviers, cadres flottants ou sites naturels, être d’une salinité suffisante et posséder les paramètres physiques de qualité de l’eau appropriés pour permettre aux mollusques bivalves d’assurer normalement leurs fonctions. La salinité optimale variera en fonction de l’espèce et de la zone de récolte. La qualité de l’eau devra convenir au procédé.
• Avant le dégorgement ou l’entreposage, il faudrait laver les mollusques bivalves pour les débarrasser de la boue et des épibiontes mous, et éliminer les mollusques bivalves morts ou affaiblis chaque fois que possible.
• Durant l’entreposage, les mollusques bivalves devraient être répartis selon une densité et dans des conditions telles qu’ils puissent s’ouvrir et assurer normalement leurs fonctions.
• La teneur en oxygène de l’eau de mer des réservoirs devrait être maintenue en permanence à un niveau adéquat.
• La température de l’eau contenue dans les bacs ne devrait pas s’élever au point d’affaiblir les mollusques bivalves. Si la température ambiante est excessivement élevée, les bacs devraient être placés dans une construction convenablement aérée ou à l’abri des rayons directs du soleil. La durée du dégorgement devrait être adaptée à la température de l’eau.
• Les mollusques bivalves ne devraient être entreposés dans l’eau de mer que pendant le temps où ils demeurent sains et actifs.
• Les bacs devraient être vidés, nettoyés et désinfectés à des intervalles appropriés.
• Les systèmes d’entreposage utilisant de l’eau recyclée doivent utiliser des méthodes de traitement de l’eau approuvées.
7.6.3 Lavage, séparation, débyssage et calibrage
Voir aussi les Sections 3.2, 3.3, 3.4 et 3.5
Dangers potentiels: |
Pathogènes microbiologiques, contamination chimique et physique |
Défauts potentiels: |
Dommages mécaniques |
Conseils techniques: |
|
• Toutes les étapes de la production, y compris l’emballage, devraient être exécutées sans retard inutile et dans des conditions de nature à empêcher toute possibilité de contamination et de détérioration ou le développement de micro-organismes pathogènes ou de décomposition.
• Les lésions aux coquilles et le stress raccourciront la durée de vie des mollusques bivalves et augmenteront le risque de contamination et de détérioration. Il faudra donc manipuler les mollusques bivalves avec soin:
- on réduira au minimum le nombre de manipulations;
- on évitera les chocs excessifs.
• Les différentes étapes du traitement devraient être supervisées par du personnel techniquement compétent.
• Il faudrait débarrasser les coquilles de la vase et de tous les organismes mous qui y adhérent. Il faudrait également éliminer chaque fois que possible les épibiontes durs en prenant soin de ne pas ébrécher les bords des coquilles par un lavage vigoureux. Le lavage devrait être effectué à l’aide d’un jet d’eau (de mer) propre.
• Le cas échéant, les mollusques bivalves ayant formé des paquets seront séparés et débyssés. Le matériel utilisé devrait être conçu et ajusté de manière à endommager le moins possible les coquilles.
7.6.4 Emballage
Voir aussi les sections 3.2, 3.3, 3.4 et 3.5
Dangers potentiels: |
Pathogènes microbiologiques, contamination physique |
Défauts potentiels: |
Étiquetage erroné, présence de mollusques endommagés ou morts, matières étrangères |
Conseils techniques: |
|
• Avant d’être emballés, les mollusques bivalves devraient subir un examen visuel. Les mollusques morts, ceux dont les coquilles sont brisées, ou auxquelles adhèrent encore de la vase ou qui présentent un autre défaut ne devraient pas être approuvés pour la consommation humaine.
• Les matériaux d’emballage devraient convenir au type de produit et aux conditions d’entreposage prévues; ils ne devraient pas transmettre au produit de substances dangereuses ou inadmissibles, ni une odeur ni un goût. Ils devraient offrir des garanties de sécurité et protéger efficacement le produit contre les chocs et la contamination.
• Il faudra veiller à ce que les matériaux d’emballage ne puissent être contaminés et les égoutter.
• Les étiquettes devraient être clairement imprimées et être conformes aux lois sur l’étiquetage du pays où le produit est commercialisé. Le matériau d’emballage peut porter une indication de la manière dont les mollusques bivalves devraient être conservés à partir du moment où ils sont achetés chez le détaillant. Il est recommandé d’indiquer la date de l’emballage.
• Tous les matériaux d’emballage devraient être entreposés dans des conditions de propreté et d’hygiène. Les récipients ne devraient pas avoir servi à d’autres utilisations pouvant donner lieu à une contamination du produit. Il faudrait les inspecter immédiatement avant de les utiliser afin de s’assurer qu’ils sont dans un état satisfaisant et, si nécessaire, les éliminer, ou les nettoyer et/ou les désinfecter; après les avoir lavés, il faudrait les laisser égoutter complètement avant de les remplir. Seuls les matériaux d’emballage destinés à un emploi immédiat devraient être conservés dans la zone d’emballage ou de remplissage.
7.6.5 Entreposage
Dangers potentiels: |
Pathogènes microbiologiques |
Défauts potentiels: |
Dommages physiques |
Conseils techniques: |
|
• Le produit fini devrait être entreposé dans des conditions de nature à empêcher sa contamination par des micro-organismes ou la prolifération de ces derniers. Les matériaux d’emballage du produit fini ne devraient pas entrer en contact avec le sol mais être placés sur une surface propre et surélevée.
• La durée de l’entreposage devrait être aussi brève que possible.
• Il ne faudrait pas réimmerger dans l’eau les mollusques bivalves vivants, ni les arroser au jet, après qu’ils ont été emballés et ont quitté le centre de distribution, sauf s’ils sont vendus au détail dans le centre de distribution.
7.6.6 Distribution
Voir aussi Section 3.6
Dangers potentiels: |
peu probables |
Défauts potentiels: |
Dommages physiques |
Conseils techniques: |
|
• Le produit devrait être expédié dans l’ordre de succession des lots.
• Les mollusques bivalves destinés à la consommation humaine ne devraient quitter le centre de distribution que dans des emballages fermés.
• Le moyen de transport devrait protéger suffisamment les mollusques bivalves contre les chocs qui pourraient endommager leurs coquilles. Les mollusques bivalves ne devraient pas être transportés avec d’autres produits susceptibles de les contaminer.
[7.7. TRAITEMENT APRèS RÉCOLTE
Voir aussi les sections 3.2, 3.3, 3.4, et 3.5.
Les mollusques bivalves traités après récolte sont des produits préparés à partir de mollusques bivalves vivants qui ont reçu un traitement destiné à éliminer, réduire ou limiter les concentrations d’organismes spécifiques dans le produit à des niveaux satisfaisants pour l’autorité compétente. Le traitement après récolte conserve les qualités organoleptiques du mollusque bivalve vivant. Tout comme les mollusques bivalves vivants et crus, les mollusques bivalves traités après récolte doivent être conformes à tous les critères microbiologiques associés aux contrôles normaux de l’eau de récolte destinés à éviter la contamination fécale et la présence de pathogènes entériques qui en résulte ainsi que les toxines et autres contaminants. Ces contrôles normaux ne permettent cependant pas de contrôler les pathogènes ne relevant pas de la contamination fécale. Ces traitements sont notamment l’application de températures peu élevées, la pression hydrostatique (par exemple, 60K lb/6 min.), l’irradiation, et la surgélation individuelle.
Dangers potentiels: |
Non élimination ou réduction de la contamination microbiologique due aux organismes ciblés |
Défauts potentiels: |
Coagulation de la chair, texture défectueuse de la chair, pénétration du milieu hydrostatique dans la chair. |
Conseils techniques: |
|
• Les traitements mis au point pour éliminer ou réduire les pathogènes devraient être scientifiquement validés afin de garantir leur efficacité.
• Les traitements (chaleur, pression, etc.) devraient être étroitement surveillés afin de garantir qu’ils n’entraînent pas de modifications dans la texture de la chair des produits qui seraient inacceptables pour le consommateur.
• Les paramètres des traitements établis pour réduire ou éliminer les pathogènes devraient être approuvés par l’autorité compétente.]
Cette section ne traite que le traitement thermique/décoquillage des mollusques qui est propre au présent code d’usages en matière d’hygiène.
La plupart des prescriptions relatives aux opérations suivantes: réception, dégorgement, entreposage, lavage, séparation des paquets, débyssage, calibrage, emballage, entreposage et distribution s’appliqueraient également aux mollusques bivalves destinés à être soumis à un traitement thermique et à un décoquillage.
Le stress et les chocs excessifs subis par les mollusques bivalves qui seront traités par la chaleur sont un peu moins graves que dans le cas des mollusques destinés à être distribués.
7.7.1 Traitement thermique à des fins d’épuration
Voir aussi Sections 3.2, 3.3, 3.4 et 3.5
Dangers potentiels: |
Agents pathogènes microbiologiques |
Défauts potentiels: |
peu probables |
Conseils techniques: |
|
Au lieu de recourir au reparcage ou à l’épuration, il est possible dans certains cas d’éliminer la contamination microbiologique par un traitement thermique. Il pourra s’agir d’un procédé de stérilisation ou de pasteurisation. Il est très important de contrôler la durée de l’opération et la température à laquelle elle sera effectuée (F >= 15) et, le cas échéant, la pression. Le traitement thermique est très délicat et doit être approuvé par l’autorité compétente. Les établissements doivent procéder à des contrôles fréquents afin de s’assurer que le traitement thermique est satisfaisant.
Très importants également sont les documents qui accompagnent les lots de mollusques bivalves. Les mollusques bivalves pollués ne devraient pas entrer en contact ou être mélangés avec des mollusques bivalves qui satisfont aux spécifications concernant les produits finis.
• Les mollusques bivalves doivent provenir de zones conchylicoles désignées comme acceptables par l’autorité compétente.
• Les mollusques bivalves destinés à un traitement thermique ne doivent pas dépasser les concentrations acceptables de substances chimiques ou de biotoxines.
• Chaque établissement qui épure les mollusques bivalves par traitement thermique devrait élaborer un programme des opérations, approuvé par l’autorité compétente, qui prenne en compte des facteurs critiques comme l’espèce et la taille des mollusque bivalves, la durée de l’exposition à la chaleur, la température interne des mollusques bivalves, le type de traitement effectué, les rapports eau/vapeur-mollusques bivalves, la nature du matériel utilisé, les instruments de mesure et leur calibrage, les opérations de refroidissement après le traitement thermique, le nettoyage et la désinfection du matériel servant pour le traitement thermique.
• Le procédé de traitement thermique doit être approuvé par l’autorité compétente.
• Tous les mollusques bivalves devraient être lavés avec de l’eau potable ou de l’eau de mer propre sous pression et les mollusques bivalves morts ou affaiblis devraient être éliminés avant le traitement thermique.
• Les mollusques bivalves pollués ne devraient pas entrer en contact avec des mollusques bivalves qui satisfont aux spécifications concernant les produits finis.
• Après le traitement thermique, les mollusques doivent répondre aux spécifications concernant les produits finis énoncées dans la Norme Codex.
7.7.2 Décoquillage des mollusques suivi de l’emballage
Le décoquillage est une méthode consistant à éliminer la coquille des mollusques bivalves.
Voir aussi Sections 3.2, 3.3, 3.4 et 3.5
Dangers potentiels: |
Contamination physique |
Défauts potentiels: |
peu probables |
Conseils techniques: |
|
• Les mollusques bivalves doivent provenir de zones conchylicoles agréées et/ou après reparcage dans une zone de reparcage agréée ou épuration dans une station d’épuration ou des bacs approuvés. Chaque établissement qui décoquille les mollusques bivalves devrait élaborer un programme des opérations, agréé par l’autorité compétente, qui prenne en compte des facteurs critiques comme l’espèce et la taille des mollusques bivalves, la durée de l’exposition à la chaleur, la température interne des mollusques bivalves, le type de traitement effectué, les rapports eau/vapeur-mollusques bivalves, la nature du matériel utilisé, les instruments de mesure et leur calibrage, les opérations de refroidissement après le traitement thermique, le nettoyage et la désinfection du matériel servant pour le traitement thermique.
• Tous les mollusques bivalves devraient être lavés avec de l’eau potable ou de l’eau de mer propre sous pression et les mollusques bivalves morts ou affaiblis devraient être éliminés avant le traitement thermique.
• Avant le décoquillage, il faudrait s’assurer que les mollusques bivalves sont vivants et ne sont pas très affaiblis.
• Les mollusques bivalves décoquillés devraient être refroidis jusqu’à 7°C ou moins dans les deux heures suivant le traitement thermique (ce laps de temps inclut l’opération de décoquillage). Cette température devrait être maintenue durant le transport, l’entreposage et la distribution.
• Les mollusques bivalves décoquillés devraient être emballés dès que possible. Avant de les emballer, il faudrait vérifier que les produits sont exempts de matières inadmissibles telles que des morceaux de coquille.
• Une fois décoquillés, les mollusques bivalves doivent satisfaire aux spécifications concernant les produits finis énoncées dans la Norme Codex.
7.8 DOCUMENTS ET REGISTRES
• Le transport des mollusques bivalves vivants d’une zone conchylicole jusqu’à un centre de distribution, une station d’épuration, une zone de reparcage ou une usine de transformation doit être accompagné de documents pour l’identification des lots de bivalves vivants.
• Il faudrait tenir pour chaque lot des registres permanents, lisibles et datés relatifs aux opérations de reparcage et d’épuration, et les conserver pendant au moins un an.
• Les stations d’épuration ou les bacs, ainsi que les centres de distribution et les usines de transformation ne devraient accepter que les lots de mollusques bivalves vivants accompagnés d’un document délivré ou approuvé par l’autorité compétente. Ce document devrait contenir les renseignements suivants :
- l’identité et la signature de l’exploitant pêcheur;
- la date de la récolte;
- le nom et la quantité de mollusques bivalves;
- l’emplacement de la zone conchylicole.
• Des relevés détaillés indiquant la date et le lieu de la récolte, ainsi que la durée des opérations de reparcage ou d’épuration de chaque lot, devraient être établis par le centre de distribution ou l’usine de transformation et conservés aussi longtemps que l’exige l’autorité compétente.
7.9 IDENTIFICATION DES LOTS ET PROCÉDURES DE RETRAIT
Voir aussi Section 3.7
• Chaque produit qui sort du centre de distribution ou de l’usine de transformation devrait porter un numéro permettant d’identifier facilement le lot. Ce numéro de lot devrait inclure un code d’identification, le numéro du centre de distribution ou de l’usine de transformation, le pays d’origine et le jour et le mois de l’emballage afin de pouvoir retrouver plus facilement le produit. Les centres de distribution devraient tenir un registre où seront inscrits ces numéros de lots, de manière que chaque lot de mollusques puisse être suivi depuis la zone conchylicole jusqu’à l’utilisateur final.
• Pour effectuer un retrait de manière satisfaisante, il faut que la direction du centre de distribution prenne au préalable les mesures nécessaires.
• Il faudra tenir compte en particulier des aspects suivants:
- Le produit en cause doit être facilement identifiable par le numéro du lot;
- La destination et les clients du produit en cause doivent être identifiables;
- Les tâches et les responsabilités de la direction et du personnel doivent être claires;
- Les noms et numéros de téléphone du personnel, des organisations et des clients intéressés doivent être indiqués.
SECTION 11 – TRANSFORMATION DU POISSON SALÉ
En ce qui concerne les contrôles à effectuer aux différentes étapes de transformation, cette section donne des exemples de dangers et de défauts potentiels et des conseils techniques qui pourront servir pour élaborer des mesures de maîtrise et des actions correctives. À chaque étape, seuls sont énumérés les dangers et les défauts qui peuvent être introduits ou maîtrisés à cette même étape. Il convient de noter que, lors de la mise au point d’un plan HACCP et/ou DAP, il est indispensable de consulter la section 5 où l’on trouve des conseils pour l’application des principes HACCP et de l’analyse DAP. Cependant, dans le cadre du présent code, il est impossible d’indiquer en détail les seuils critiques, la surveillance, la tenue des registres et la vérification relatifs à chaque étape, car ils diffèrent selon les dangers et défauts.
Le poisson salé ou les produits dérivés devraient être propres à la consommation humaine, bien préparés et emballés de manière à être protégés de la contamination et à demeurer attrayants et sains. Afin de maintenir la qualité du poisson, il est important d’adopter des procédés de manutention rapides, méticuleux et efficaces.
Cette section ne couvre pas le poisson salé séché (cf. klippfish) ou les produits dérivés.
11.1 GÉNÉRALITÉS
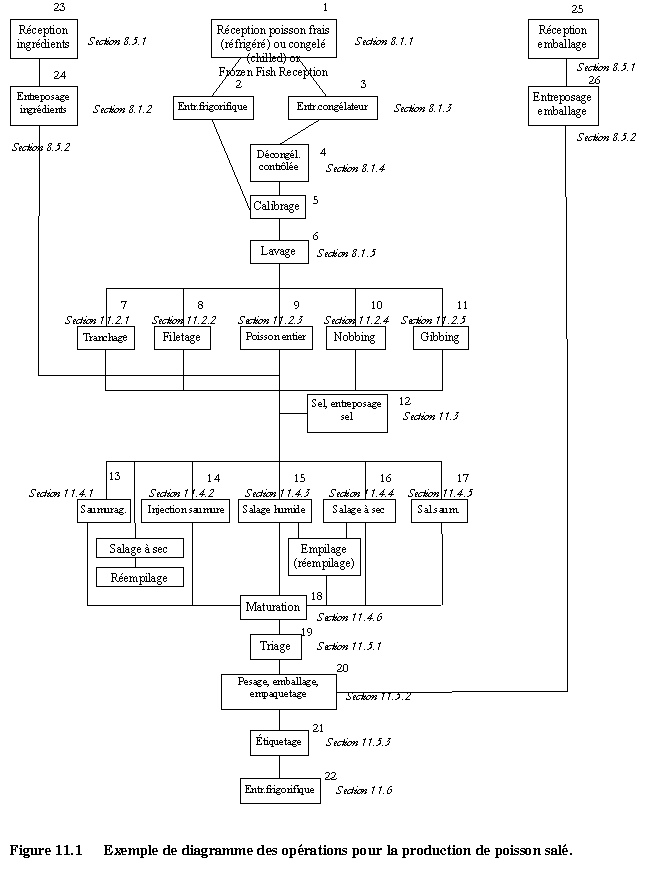
Voir aussi la section 8.1 pour la manipulation générale avant la transformation et la Figure 11.1 pour un exemple de diagramme des opérations pour la production de poisson salé.
• selon les espèces utilisées pour le salage, le poisson devrait être saigné complètement dans les meilleurs délais;
• il faut contrôler le poisson frais destiné à être salé pour déceler la présence de parasites visibles;
• le poisson congelé ne devrait pas être salé avant d’avoir été parfaitement décongelé et inspecté;
• la congélation, la chaleur ou une association adéquate de teneur en sel et de durée d’entreposage peuvent être utilisés pour tuer les parasites;
• la pénétration du sel sera fonction de paramètres comme la teneur en matières grasses, la température, la quantité de sel, la composition du sel, le titre de la saumure, etc.
Le diagramme ci-après est présenté uniquement à titre d’exemple. Pour mettre en œuvre un plan HACCP, un diagramme complet et détaillé devra être établi pour chaque produit.
Les références indiquent les sections correspondantes du présent code
11.2 PRÉPARATION AVANT LE SALAGE
11.2.1 Tranchage, lavage et rinçage (Étape de transformation 7)
Dangers potentiels: |
Parasites, contamination microbiologique, chimique et physique |
Défauts potentiels: |
Parasites, décomposition |
Conseils techniques: |
|
• la chaîne de tranchage devrait être conçue de manière à permettre le passage continu des poissons sans interruptions ni ralentissements;
• les poissons devraient être découpés par une entaille parallèlement à l’arête principale depuis l’encolure ou le collet jusqu’à la queue, et de telle sorte que l’on évite d’entailler ou de déchirer les bords ou de gaspiller de la chair. Si l’arête centrale doit être éliminée, les poissons devront être tranchés assez profondément pour que les restes de l’arête centrale (la nageoire caudale) soient libres. Il vaut mieux couper l’arête que l’arracher de la chair;
• le découpage du poisson devrait être effectué par un expert de manière à ce que le sang dans le collet et les caillots de sang soient éliminés;
• immédiatement après avoir été découpés, les poissons devraient être lavés dans une grande quantité d’eau potable ou d’eau de mer propre, afin d’éliminer tout le sang du poisson;
• toutes les impuretés, le sang et le foie devraient être éliminés;
• les parasites visibles devraient être éliminés;
• si la membrane noire doit être enlevée, il faut le faire après le tranchage;
11.2.2 Filetage, épiautage et parage (Étape de transformation 8)
Voir Section 8.1.6.
11.2.3 Poisson entier (Étape de transformation 9)
Voir Section 8.1.1 – 8.1.5.
11.2.4 Nobbing (Étape de transformation 10)
Dangers potentiels: |
Parasites, contamination microbiologique, chimique et physique, histamine |
Défauts potentiels: |
Restes de viscères (appât) et d’intestins autres que laitance et œufs, décomposition |
Conseils techniques: |
|
voir section 11.2.1, 2ème alinéa;
• après étêtage et éviscération (nobbing), il faudrait vérifier qu’il ne reste pas d’intestins ;
• il faudrait aussi laver soigneusement le poisson pour éliminer le sang, les restes d’intestin et, le cas échéant, les écailles;
• en fonction du déroulement des opérations sur le bateau ou dans l’usine de transformation et lorsqu’un seuil critique concernant la durée et la température de l’opération a été établi pour la maîtrise de l’histamine ou d’un défaut, le poisson étêté et éviscéré devrait être égoutté et mis sous glace ou réfrigéré convenablement dans des récipients propres et conservé dans des zones conçues à cet effet à l’intérieur de l’usine de transformation.
11.2.5 Gibbing (Étape de transformation 11)
Dangers potentiels: |
Parasites, contamination microbiologique, chimique et physique, histamine |
Défauts potentiels: |
Restes de viscères (appât), décomposition |
Conseils techniques: |
|
voir section 11.2.1, 2ème alinéa;
• après éviscération sans ouvrir l'abdomen (gibbing), il faudrait vérifier que l’opération a été effectuée correctement;
• il faudrait trier le poisson dont l’éviscération a été mal faite, et le destiner à d’autres fins;
• il faudrait aussi laver soigneusement le poisson pour éliminer le sang, les restes indésirables d’intestins, le cœur, etc. et, le cas échéant, les écailles;
• en fonction du déroulement des opérations sur le bateau ou dans l’usine de transformation et lorsqu’un seuil critique concernant la durée et la température de l’opération a été établi pour la maîtrise de l’histamine ou d’un défaut, le poisson éviscéré par gibbing devrait être égoutté et mis sous glace ou réfrigéré convenablement dans des récipients propres et conservé dans des zones conçues à cet effet à l’intérieur de l’usine de transformation.
11.3 MANUTENTION DU SEL ET PRESCRIPTIONS RELATIVES AU SEL (ÉTAPE DE TRANSFORMATION 12)
11.3.1 Manutention
Dangers potentiels: |
Contamination biologique, chimique, physique |
Défauts potentiels: |
Contamination biologique, chimique, physique |
Conseils techniques: |
|
• le sel devant servir au salage du poisson devrait être transporté et entreposé au sec et bien protégé dans des bacs à sel, des entrepôts, des récipients ou dans des sacs de plastique;
• afin de réduire au minimum le risque d’infection du poisson salé, il faudrait s’abstenir de réemployer le sel déjà utilisé;
11.3.2 Prescriptions relatives au sel
Dangers potentiels: |
Contamination biologique, chimique, physique |
Défauts potentiels: |
Contamination biologique, chimique, physique, composition défectueuse |
Conseils techniques: |
|
• le sel employé pour saler le poisson devrait être de qualité alimentaire et sa composition devrait convenir au produit;
• la composition du sel diffère suivant son origine. Le sel gemme et le sel d’origine marine contiennent plusieurs autres sels: sulfates ou chlorures de calcium ou de magnésium, etc., sous forme d’impuretés. Le sel transformé et raffiné sous vide est du chlorure de sodium presque pur;
• il faut employer pour le salage à sec du poisson gras un sel relativement pur; pour la préparation de certains produits, la présence de petites quantités de sel de calcium améliore quelque peu la présentation du produit. La présence d’une quantité trop forte de calcium est susceptible de réduire le taux de pénétration du sel, à tel point qu’elle peut entraîner l’altération du poisson;
• les teneurs trop élevées en sel de magnésium produisent un goût amer désagréable et peuvent entraîner l’altération en cours de salage;
• le sel marin peut contenir des bactéries halophiles et des moisissures qui continuent de vivre dans le sel et le poisson salé et peuvent contribuer à l’altération;
• il faudrait vérifier que le sel employé pour saler le poisson est propre, qu’il n’a pas été déjà utilisé, qu’il est exempt de matières et de cristaux étrangers,qu’il ne présente aucun signe visible de contamination par la saleté, les lubrifiants, l’eau de cale ou d’autres substances étrangères;
• la taille des grains de sel est un paramètre qui doit être soigneusement pris en considération. Les grains de sel très fins peuvent entraîner la formation d’aggrégats qui ne facilitent pas la répartition uniforme du sel sur le poisson. Les grains de sel très gros peuvent provoquer des lésions de la chair du poisson pendant le salage et réduire la vitesse de maturation;
• il faudrait utiliser de petits cristaux pour le salage à sec des poissons gras et de gros cristaux pour les poissons maigres;
• le sel employé devrait répondre aux prescriptions suivantes:
- la teneur en fer ne doit pas dépasser 10 mg/kg;
- la teneur en cuivre ne doit pas dépasser 0,1 mg/kg ;
- être exempt de micro-organismes qui nuisent à la qualité des produits finis;
• le sel utilisé pour le salage des poissons de la famille des gadidées devrait répondre aux prescriptions suivantes:
- des teneurs en sel de calcium de l’ordre de 0,15 à 0,35 % peuvent convenir;
- si des sels de magnésium sont présents, les concentrations ne doivent pas dépasser 0,15 %;
- si le sel n’est pas exempt de micro-organismes, le maintien de basses températures pourra en retarder le développement;
• la norme Codex pour le sel de qualité alimentaire (Codex Stan. 150-1985, Rév. 1-1997, Amend. 1-1999) vise le sel utilisé en tant qu’ingrédient alimentaire destiné aussi bien à la vente directe au consommateur qu’à l’industrie alimentaire.
11.4 SALAGE ET MATURATION
Le poisson salé devrait être propre à la consommation humaine. Il ne devrait pas contenir de restes de viscères, de foie ou d’autres entrailles.
Le salage du poisson par saumurage, injection de saumure, salage en saumure (salage en conditions humides) ou salage à sec devrait être effectué compte dûment tenu des effets sur la qualité du produit fini et dans de très bonnes conditions hygiéniques.
La qualité du poisson salé à sec peut être altérée par deux phénomènes: le « rougissement » et la « formation de moisissures brunes ». On peut combattre ces deux phénomènes en maintenant la température au-dessous de 8o C. Le sel marin peut contenir des bactéries halophiles qui continuent de vivre dans le sel et le poisson salé. Afin de réduire au minimum le risque d’infection du poisson salé, il faudrait éliminer de l’usine le sel déjà utilisé et/ou contaminé.
La qualité du poisson salé peut aussi être altérée par une décoloration marron (jaune) souvent due au rancissement causé par les catalyseurs métalliques dans le sel. La qualité du sel est importante, il faudrait maintenir une température basse pendant le processus, et éviter la lumière et l’oxygène.
11.4.1 Saumurage (Étape de transformation 13)
Dangers potentiels: |
Pathogènes microbiologiques, parasites, contamination chimique et physique, histamine, composition impropre de la saumure |
Défauts potentiels: |
Parasites, contamination microbiologique, chimique et physique, décomposition, histamine |
Conseils techniques: |
|
• il ne faudrait utiliser que de la saumure récemment stabilisée pour les opérations de salage; la qualité de l’eau est importante, il faudrait utiliser de l’eau potable pour la préparation de la saumure;
• le rapport entre la saumure et le poisson et le titre de la saumure devrait être adaptés au produit recherché; il est important de contrôler la durée et la température (<4°C) si le titre de la saumure est inférieur à la saturation;
• le titre de la saumure devrait être vérifié à intervalles réguliers et corrigé avant usage, le cas échéant;
11.4.2 Injection de saumure (Étape de transformation 14)
Dangers potentiels: |
Pathogènes microbiologiques, parasites, contamination chimique et physique, fragments d’aiguille d’injection, histamine, composition impropre de la saumure |
Défauts potentiels: |
Parasites, contamination biologique, chimique et physique, décomposition, histamine |
Conseils techniques: |
|
• les appareils utilisés pour l’injection de saumure devraient être nettoyés et désinfectés à intervalles réguliers;
• il faudrait vérifier tous les jours que les aiguilles ne sont pas épointées, bouchées ou déformées;
• seul un personnel dûment formé devrait utiliser les dispositifs d’injection de saumure;
11.4.3 Salage en conditions humides (Étape de transformation 15)
Dangers potentiels: |
Pathogènes microbiologiques, parasites, contamination chimique et physique, histamine |
Défauts potentiels: |
Parasites, contamination biologique, chimique et physique, décomposition, histamine |
Conseils techniques: |
|
• le poisson destiné à être salé en saumure devrait être salé et déposé avec soin dans la cuve de saumurage de façon à réduire au minimum les espaces vides entre les poissons;
• les quantités de sel, la durée et la température du traitement devraient être contrôlées avec soin pour obtenir le produit voulu;
• au cours du salage, le titre de la saumure devrait être contrôlé régulièrement avec un salinomètre, conformément aux spécifications;
• après le salage, le poisson pourrait être empilé. Il faudra s’assurer auparavant que le rapport sel/eau est correct. Si le poisson est entassé, il faudra ajouter du sel et le répartir régulièrement sur toute la surface du poisson;
• le poisson devrait être entreposé ou maintenu pendant une période suffisamment longue à des températures appropriées, afin que le traitement soit satisfaisant et pour éviter que le produit se détériore;
11.4.4 Salage à sec (Étape de transformation 16)
Dangers potentiels: |
Pathogènes microbiologiques, parasites, contamination chimique et physique, histamine |
Défauts potentiels: |
Parasites, contamination biologique, chimique et physique, décomposition, histamine |
Conseils techniques: |
|
• les poissons destinés à être salés à sec devraient être placés convenablement, de manière à réduire au minimum les espaces vides entre les poissons et à assurer des conditions uniformes et un écoulement approprié;
• les piles de poissons ne devraient jamais être placées à même le sol ou en contact direct avec le mur;
• les quantités de sel, la durée et la température du traitement devraient être contrôlées avec soin pour obtenir le produit voulu. Il est important que la quantité de sel soit suffisante pour assurer la qualité du produit;
• les poissons devraient être réempilés périodiquement, ceux se trouvant au sommet de la pile étant ensuite placés en bas; et on devrait ajouter du sel frais pour qu’il y ait suffisamment de sel pour terminer le traitement;
• si les poissons sont réempilés sur des palettes, celles-ci devraient être propres;
• le poisson ne devrait pas être soumis à des températures de congélation pendant le salage;
• les poissons salés des familles des clupéidés ou des scombridés devraient être entreposés ou maintenu à une température inférieure à 9° C afin d’éviter la formation de scombrotoxine/histamine;
11.4.5 Salage en saumure (Étape de transformation 17)
Dangers potentiels: |
Pathogènes microbiologiques, parasites, contamination chimique et physique, histamine |
Défauts potentiels: |
Parasites, contamination biologique, chimique et physique, décomposition, histamine |
Conseils techniques: |
|
• il faut ajuster la quantité de sel en fonction de la qualité du poisson (essentiellement) gras (teneur en graisse). Le sel, le sucre et les épices devraient être pesés/mesurés et répartis de manière uniforme;
• au cours de l’opération de saumurage, tous les poissons devraient être immergés dans la saumure produite par le salage en saumure;
• on devrait tasser les poissons dans les récipients, puis y ajouter du sel ou de la saumure avant de les fermer;
• les poissons gras traités devraient être maintenus dans de la saumure ou dans une solution de sel;
• les poissons gras devraient toujours être couverts de saumure en cours de traitement;
• le salage en saumure convient surtout pour les poissons gras. Dans certaines conditions, on peut utiliser le salage à sec pour les poissons gras de petite taille, comme les anchois ou les petits harengs;
11.4.6 Maturation (Étape de transformation 18)
Dangers potentiels: |
Pathogènes microbiologiques, parasites, contamination chimique et physique, histamine |
Défauts potentiels: |
Parasites, contamination biologique, chimique et physique, décomposition, histamine, rancissement et décoloration de la chair ou de la surface |
Conseils techniques: |
|
• la durée de la maturation varie en fonction du poisson (espèce, taille et qualité), de la température et de la quantité de sel absorbé par les tissus du poisson;
• la maturation d’un poisson de la famille des gadidées salé en conditions humides nécessite 10 à 12 jours dans la saumure et après empilage, et 7 à 10 jours en pile, alors que celle d’un poisson salé à sec nécessite 20 à 28 jours avec au moins un réempilage à une température de 5° à 8°;
• les poissons gras comme les harengs peuvent être conservés pendant la durée de la maturation à une température de 5o C à 10o C. La maturation peut nécessiter de quelques semaines à plusieurs mois selon le produit. Si les récipients doivent être placés à des températures plus basses, le processus sera plus long;
• la première partie de la période de traitement pour les poissons de la famille des clupéidés ou des scombridés devrait être effectuée à une température de 0°C à 5°C pour empêcher la formation d’histamine;
• durant le salage des poissons de la famille des clupéidés ou des scombridés, la teneur en histamine des produits finis devrait être contrôlée à intervalles réguliers;
11.5 TRIAGE, PESAGE, EMBALLAGE, EMPAQUETAGE ET ÉTIQUETAGE
Voir aussi Sections 6.4.4 et 6.5.
11.5.1 Triage (Étape de transformation 19)
Dangers potentiels: |
Peu probables |
Défauts potentiels: |
Triage défectueux (qualité, pesage, taille, espèce, etc.) |
Conseils techniques: |
|
• le poisson salé devrait être trié par espèce, taille et catégorie de qualité commerciale pour le marché auquel il est destiné;
• avant le triage, il faudra débarrasser les poissons du sel détaché et ajouter du nouveau sel avant de les emballer;
11.5.2 Pesage, emballage et empaquetage (Étape de transformation 20)
Dangers potentiels: |
Pathogènes microbiologiques, parasites, contamination chimique et physique |
Défauts potentiels: |
Déshydratation ultérieure, décomposition |
Conseils techniques: |
|
• les matériaux d’emballage devraient être propres, solides, durables, suffisants pour l’emploi auquel ils sont destinés et de qualité alimentaire;
• les barils dans lesquels les poissons gras doivent être commercialisés devraient être propres, intacts et hygiéniques.
• l’emballage devrait être effectué de manière à minimiser le risque de contamination et de décomposition;
• les produits devraient répondre aux normes pertinentes concernant l’étiquetage et les poids;
11.5.3 Étiquetage (Étape de transformation 21)
Voir aussi Sections 8.2.3 et 8.5.
11.6 ENTREPOSAGE FRIGORIFIQUE (ÉTAPE DE TRANSFORMATION 22)
Dangers potentiels: |
Pathogènes microbiologiques, contamination chimique, histamine |
Défauts potentiels: |
contamination biologique, chimique et physique, décomposition (histamine, poisson gras), « rougissement » et formation de « moisissures brunes » |
Conseils techniques: |
|
• après salage et maturation, le poisson devrait être placé dans un entrepôt frigorifique;
• la température dans l’entrepôt frigorifique devrait s’établir entre 1° C et 4°C;
• il faudrait surveiller et enregistrer à intervalles réguliers la température et la durée de l’entreposage;
• les produits devraient être manipulés avec soin et ne pas former de piles trop hautes;
11.7 EMBALLAGE, ÉTIQUETTES ET INGRÉDIENTS (ÉTAPES DE TRANSFORMATION 23, 24, 25 & 26)
Voir Section 8.5.
SECTION 12 – TRANSFORMATION DU POISSON FUMÉ
En ce qui concerne les contrôles à effectuer aux différentes étapes de transformation, cette section donne des exemples de dangers et de défauts potentiels et des conseils techniques qui pourront servir pour élaborer des mesures de maîtrise et des actions correctives. À chaque étape, seuls sont énumérés les dangers et les défauts qui peuvent être introduits ou maîtrisés à cette même étape. Il convient de noter que, lors de la mise au point d’un plan HACCP et/ou DAP, il est indispensable de consulter la section 5 où l’on trouve des conseils pour l’application des principes HACCP et de l’analyse DAP. Cependant, dans le cadre du présent code, il est impossible d’indiquer en détail les seuils critiques, la surveillance, la tenue des registres et la vérification relatifs à chaque étape, car ils diffèrent selon les dangers et défauts.
Il y a longtemps que le fumage est utilisé pour conserver le poisson. On a donc acquis au fil des ans beaucoup d’expérience concernant les dangers potentiels de cette méthode.
Les méthodes modernes de fumage et de conservation des produits fumés réfrigérés ont cependant modifié les obstacles traditionnels au développement des bactéries et les ont remplacés principalement par la réfrigération, ce qui prolonge la durée de conservation.
Il s’ensuit que ce que l’on savait au sujet de l’innocuité du produit ne suffit plus et qu’il faut faire fond sur les nouvelles connaissances.
[La question de savoir si l’emploi de fumée liquide est un procédé entrant dans le cadre du présent code ou doit être considéré comme l’emploi de substances aromatisantes doit être examinée.]
Néanmoins, les dangers et les défauts potentiels liés aux différents types de matières premières utilisés pour la production de poisson fumé sont connus.
En général, le programme de conditions préalables décrit à la section 3 s’applique ainsi que les généralités concernant la manipulation du poisson frais à la section 4, et la description du système HACCP et de l’analyse DAP à la section 5.
Les recommandations formulées pour la production de poissons et produits de la pêche frais à la section 6 s’appliquent à la préparation du poisson utilisé comme matière première pour la production de poisson fumé. Si du poisson frais d’une espèce risquant d’héberger des parasites viables [et dangereux] doit être utilisé comme matière première pour un produit fumé et n’est pas traité durant les derniers stades de la transformation d’une manière qui tuera les parasites, le poisson frais devrait être congelé [pendant au moins 24 heures à -20°C] ce qui représente une étape de la préparation du poisson. Par exemple, cela pourrait être nécessaire lorsqu’on utilise du saumon sauvage provenant de certaines eaux comme matière première pour le saumon fumé à froid, si le saumon fumé n’est pas congelé avant la vente.
Le poisson fumé à froid devrait répondre aux spécifications énoncées dans la Norme Codex pour le poisson fumé à froid préemballé1.
On examine dans le présent chapitre les caractéristiques des produits fumés et la manipulation de ces produits.
Lorsque la transformation, l’emballage ou les conditions d’entreposage du produit diffèrent de ce qui est décrit dans le présent code, l’opérateur devrait s’efforcer de valider scientifiquement la sécurité des opérations de transformation, d’emballage et d’entreposage du produit afin d’éliminer de nouveaux dangers pour le consommateur.
Le diagramme ci-après est présenté uniquement à titre d’exemple.
Pour mettre en œuvre un plan HACCP, un diagramme complet et détaillé devra être établi pour chaque produit.
Les références indiquent les sections correspondantes du présent Code

12.1 PRÉ-SALAGE (ÉTAPE DE TRANSFORMATION 1)
Dangers potentiels: |
contamination microbiologique, chimique et physique, développement microbiologique, contamination biochimique |
Défauts potentiels: |
décomposition, contamination physique |
Conseils techniques: |
|
Le poisson destiné à être fumé à chaud n’est habituellement pré-salé que pendant un bref laps de temps pour acquérir du goût, c’est-à-dire pendant 2 heures au maximum, par immersion dans une saumure moyennement salée.
D’ordinaire, le poisson destiné à être fumé à froid est salé à sec ou par injection d’une solution de saumure moyennement salée pour acquérir du goût. On laisse ensuite le poisson salé pendant environ 24 heures sous réfrigération pour qu’il s’équilibre.
La formation d’histamine peut avoir lieu chez les poissons d’une espèce sensible, si ceux-ci sont conservés à une température trop élevée pendant un laps de temps prolongé.
• de la saumure fraîche devrait être préparée chaque jour de production avec du sel de qualité alimentaire;
• il faudrait surveiller la quantité de sel dans la saumure;
• pour le poisson destiné à être fumé à froid, il faudrait augmenter la teneur en sel du poisson jusqu’à ce que le sel en phase aqueuse dépasse [3%] [3,5%] pour éviter le développement de Clostridium botulinum;
• il faudrait tenir au frais la saumure et surveiller la température, en particulier si la saumure est recyclée pour l’injection d’une solution de saumure;
• si la saumure est recyclée, une étape de décontamination devrait être instaurée;
• le flux de produits devrait être maintenu de manière à éviter une accumulation indésirable.
12.2 FUMAGE (ÉTAPE DE TRANSFORMATION 2 & 3)
Dangers potentiels: |
contamination microbiologique, chimique et physique, développement microbiologique, contamination biochimique |
Défauts potentiels: |
décomposition, contamination physique |
Conseils techniques: |
|
L’opération de fumage commence habituellement par une phase de séchage. Cette phase devrait être aussi brève que possible, car une exposition prolongée à la température ambiante pourrait conduire au développement de microbes indésirables et à la formation d’histamine chez les espèces sensibles.
Durant l’opération de fumage à chaud, la température dans la partie centrale du produit atteindra normalement [63°C][72°C] pendant environ une demi-heure. La durée et la température doivent être déterminées de façon à garantir que la coagulation de la chair par la chaleur est totale dans l’arête dorsale.
Durant l’opération de fumage à froid, la température des produits est maintenue inférieure à la température de coagulation pour le poisson, habituellement à moins de 30°C, mais peut varier entre 27°C et 38°C.
Afin d’éviter la contamination croisée par la sciure et les spores des moisissures, il faudrait produire de la fumée dans une pièce séparée. Lorsque les générateurs de fumée font partie des unités, on veillera particulièrement à ne pas contaminer la chambre de fumage par des copeaux ou la fumée émise par les générateurs.
Seul du bois qui n’a pas été traité par un produit chimique tel que de la peinture ou des substances imprégnantes devrait être utilisé pour la production de fumée.
• le bois utilisé pour produire de la fumée ne devrait pas avoir été traité avec des substances chimiques;
• il convient de stocker le bois dans un endroit sec séparé des aires de production;
• éviter la contamination croisée du bois avec les produits en plaçant le générateur de fumée dans une pièce séparée de l’aire de production;
• réduire au minimum la durée du séchage du poisson avant le fumage;
• surveiller la durée et la température de l’opération de fumage.
12.3 TRANCHAGE DES PRODUITS FUMÉS À FROID (ÉTAPES DE TRANSFORMATION 5 & 6)
Dangers potentiels: |
contamination croisée microbiologique, développement microbiologique |
Défauts potentiels: |
peu probables |
Conseils techniques: |
|
La plus grande partie des poissons et produits de la pêche fumés à froid est vendue sous forme de tranches de filets de tailles différentes ou de filets entiers en emballage. Avant le tranchage, les filets fumés peuvent être congelés à environ - 5°C pour stabiliser a chair du poisson à trancher.
L’opération de tranchage et le transport sur bandes transporteuses sont déterminants pour l’hygiène du produit fini.
On veillera particulièrement à contrôler la présence Listeria monocytogenes. Il faudrait éviter l’accumulation et le développement de Listeria monocytogenes en gardant les trancheuses et les bandes transporteuses propres et en éliminant la possibilité de prolifération bactérienne.
• maintenir un flux de produits pour éviter une accumulation excessive de produits sur la chaîne de production;
• garder propres les trancheuses et les bandes transporteuses par des lavages fréquents et réguliers durant l’opération.
12.4 REFROIDISSEMENT ET/OU CONGÉLATION (ÉTAPES DE TRANSFORMATION 4 & 9)
Dangers potentiels: |
contamination croisée microbiologique, développement microbiologique |
Défauts potentiels: |
décomposition, contamination physique |
Conseils techniques: |
|
Le refroidissement après le fumage (étape de transformation 4) est important et devrait être effectué avec soin.
Le refroidissement après l’emballage (étape de transformation 9) est aussi important.
• refroidir de manière appropriée les produits fumés à chaud [, c’est-à-dire que les produits devraient être refroidis à moins de 10°C dans les 2 heures et à moins de 3°C dans les 6 heures];
• refroidir de manière appropriée les produits fumés à froid [, c’est-à-dire que les produits devraient être refroidis de 0°C à 2°C dans les 2 heures].
12.5 EMBALLAGE DES PRODUITS FUMÉS À CHAUD ET DES PRODUITS FUMÉS À FROID (ÉTAPE DE TRANSFORMATION 7)
Dangers potentiels: |
contamination microbiologique, chimique et physique, développement microbiologique, dissolution des agents de conservation présents dans la fumée par condensation de l’eau |
Défauts potentiels: |
contamination physique |
Conseils techniques: |
|
Les poissons fumés à chaud sont présents sur le marché sous de nombreuses formes mais principalement dans des boîtes ou préemballés dans des sacs de plastique, si possible sous vide ou sous atmosphère modifiée (MAP).
Les poissons fumés à froid sont présents sur le marché en général préemballés dans des sacs en plastique sous vide ou tranchés au dernier moment pour la vente directe au consommateur.
Si les produits refroidis sont emballés dans une pièce à température ambiante, une condensation pourrait se produire à la surface des produits fumés, provoquant la dissolution des agents de conservation déposés durant l’opération de fumage.
• éviter la condensation de l’eau à la surface du produit fumé;
• maintenir un flux de produits pour éviter une accumulation excessive de produits sur la chaîne de production;
• les matériaux d’emballage devraient être propres, solides, durables, suffisants pour l’emploi prévu et de qualité alimentaire.
12.6ÉTIQUETAGE (ÉTAPE DE TRANSFORMATION 8)
Voir Section 8.2.3 « Étiquetage ».
Dangers potentiels: |
peu probables |
Défauts potentiels: |
étiquetage erroné |
Conseils techniques: |
|
Les produits fumés à chaud comme à froid sont obtenus à partir de poissons dont certaines espèces sont disponibles à certaines périodes alors que d’autres le sont toute l’année.
Les produits finis peuvent être conservés pendant un certain temps comme produits congelés, et ensuite décongelés et vendus comme produits réfrigérés.
L’étiquette doit indiquer clairement si les produits ont été conservés à l’état congelé et décongelés avant la vente.
• l’étiquette doit indiquer clairement si le produit a été conservé à l’état congelé puis décongelé avant la vente.
12.7 ENTREPOSAGE, DISTRIBUTION ET VENTE AU DÉTAIL (ÉTAPES DE TRANSFORMATION 10, 11 & 12)
Dangers potentiels: |
développement microbien |
Défauts potentiels: |
perte des caractéristiques de qualité du produit |
Conseils techniques: |
|
La définition de la température d’entreposage et de la durée de conservation pour les produits fumés à froid comme à chaud devrait prendre en compte le risque de développement microbiologique pendant l’entreposage frigorifique, en particulier le développement de Listeria monocytogenes dans les produits fumés à froid, mais aussi dans les filets épiautés fumés à chaud en sacs de plastique sous vide.
12.8 DÉCONGÉLATION (ÉTAPES DE TRANSFORMATION 13 & 14)
Dangers potentiels: |
Développement microbien, contamination biochimique et microbiologique |
Défauts potentiels: |
Décomposition |
Conseils techniques: |
|
Le procédé de décongélation suivra les recommandations pertinentes énoncées à la section 8.1.4.
SECTION 13 – TRANSFORMATION DES HOMARDS ET DES CRABES
Compte tenu des contrôles nécessaires aux différentes étapes de transformation, cette section présente des exemples de dangers et de défauts potentiels et contient des lignes directrices à caractère technique qui pourront servir pour élaborer des mesures de maîtrise et des actions correctrices. À une étape donnée seuls sont énumérés les dangers et les défauts qui risquent d’être introduits ou maîtrisés à cette même étape. Il convient de noter que, lors de la mise au point d’un plan HACCP et/ou DAP, il est impératif de consulter la section 5 qui donne des conseils pour l’application des principes HACCP et de l’analyse DAP. Cependant, dans le cadre du présent code d’usages, il est impossible de donner des détails sur les seuils critiques, la surveillance, la tenue des registres et la vérification relatifs à chaque étape, car ils diffèrent selon les dangers et les défauts.
La présente section est applicable aux langoustes, homards et cigales de mer du genre Homarus, famille des Nephropidae, ainsi que des familles des Palinuridae et des Scyllaridae, destinés à la consommation humaine et d’autres espèces voisines, Nephrops non comprises.
Elle est aussi applicable, en général, aux espèces commerciales de crabe du genre Cancer, aux espèces voisines du crabe royal (limule) (Lithodes et Paralithodes), aux étrilles (Portunidae), au genre Geryon et aux crabes de Tanner (Chionoectes), ainsi qu’à d’autres espèces dont la structure physique est analogue à celle des espèces susmentionnées.
13.1 GÉNÉRALITÉS - SUPPLÉMENT AU PROGRAMME DE CONDITIONS PRÉALABLES
Outre le programme de conditions préalables décrit à la section 3 du présent document, l’usine de transformation est invitée à évaluer la conception et la construction des installations ainsi que l’entretien et l’assainissement des opérations, spécifiques de la transformation des homards et des crabes. A cet effet, elle devrait s’appuyer sur les points suivants:
13.1.1 Conception et construction du matériel et des ustensiles
• dans les procédés discontinus, le réservoir d’inactivation, l’installation de cuisson et le réservoir de refroidissement devraient être situés près les uns des autres et pourraient être équipés au-dessus d’un appareil de levage ou d’un portique pour transférer les paniers de l’un à l’autre;
• l’installation de cuisson devrait être conçue de manière à fournir une chaleur constante et suffisante pour que tous les crustacés soient exposés à la même température pendant le même temps au cours de l’opération de cuisson ;
• une pièce de longueur appropriée, traversée par un tapis roulant et équipée d’asperseurs de sorte que les crabes soient pulvérisés de tous les côtés, peut être utilisée à cet effet.
13.1.2 Programme de contrôle sanitaire
• [lorsqu’on utilise un système de chloration de l’eau, la teneur minimale en chlore libre résiduel devrait être maintenue au seuil d’efficacité pour l’usage prévu.
• [la chloration ne saurait résoudre tous les problèmes d’assainissement].
• l’eau qui a été en contact avec les crustacés ne devrait pas être réutilisée afin d’éviter les problèmes d’altération ;
• si l’on ne peut éviter que les mêmes travailleurs manipulent le produit cru et le produit cuit, des précautions rigoureuses devraient être prises pour éviter de contaminer le produit cuit avec des micro-organismes provenant du produit cru;
13.2 Considérations générales pour la manutention des homards et des crabes
Voir Section 4 – Considérations générales pour la manipulation du poisson, des mollusques et des crustacés frais de l’Avant-projet de Code d’usages pour les poissons et les produits de la pêche (ALINORM 01/18 – ANNEXE V)
13.2.1. Dangers et défauts potentiels associés aux homards et aux crabes
Voir aussi Section 4.1 Dangers potentiels associés aux poissons, mollusques et crustacés frais et à la section 5.3.3.1 Identification des dangers et des défauts
13.2.1.1. Dangers biologiques
Parasites
Un trématode appartenant au genre Paragonimus est une douve du poumon très courante en orient. La consommation de crabes ou d’écrevisses crus ou mal cuits est cause d’infection chez l’homme. Le parasite adulte vit dans des kystes qui s’établissent dans les poumons, mais a également tendance à migrer vers d’autres sites comme le foie, la rate et le cerveau. Lorsque les vers se développent dans les poumons, une maladie pulmonaire chronique s’installe.
Bactéries
Staphylococcus aureus est un micro-organisme sphérique gram-positif aérobie ou anaérobie facultatif. Il est positif à la coagulase et fermente le glucose. Quelques souches peuvent produire des entérotoxines.
Le Staphylococcus ne se trouve pas dans la microflore normale sur le poisson. L’habitat normal de cet organisme est la peau et les muqueuses de l’animal et de l’homme. La présence de Staphylococcus sur le poisson est une indication de contamination après récolte due à une mauvaise hygiène corporelle. L’organisme est un mauvais compétiteur et ne se multipliera pas dans le poisson. Cependant, dans le poisson et les produits à base de poisson, de mollusques ou de crustacés, où la flore normale est réduite ou éliminée (tels les crevettes décortiquées ou la chair de crabe cuites), la présence de staphylococci indique l’éventualité d’empoisonnement alimentaire.
Bien que les données soient limitées, de récentes enquêtes font penser que le poisson et autres fruits de mer cuits peuvent être également contaminés par Lysteria monocytogenes.
Dangers chimiques
Biotoxines
Aux États-Unis, les toxines IPM et IAM ont été observées dans les crabes « Düngeness », les crabes de Tanner et les crabes « red rock ». La toxine IPM a aussi été observée dans les homards (Homarus spp.).
Défauts
Le bleuissement de la chair de crabe [NOTE: insérer une note brève et transférer le reste du texte dans l’annexe correspondante]
Le bleuissement de la chair de crabe en conserve a été un problème jusque récemment. Il apparaît souvent non seulement à la surface de la chair de crabe en conserve, mais aussi, sur la chair de crabe plusieurs heures après cuisson et refroidissement des carcasses. La chair bleuit plus souvent à la surface de l’articulation de la chair de l’épaule, de la pince et d’autres articulations des pattes. Le bleuissement est plus fréquent sur la chair de « crab horsehair » (« kegani ») que sur celle du crabe royal. Il est dû sans aucun doute au cuivre contenu dans l’hémocyanine, qui est un composant du sang des mollusques ou des arthropodes.
Inoue et Motohiro ont recherché la cause et le mécanisme du bleuissement. La teneur en cuivre dans les chairs bleues et dans les chairs normales était en moyenne de 2,80 mg/100 g et de 0,49mg/100 g (poids humide), respectivement. Les teneurs en cuivre observées sont plus élevées dans la chair de l’épaule, à la surface de la première patte et dans les chairs proches d’une articulation et dans la chair de la pince que dans celles des autres parties. Les teneurs en cuivre au-dessus desquelles apparaît le bleuissement semblent se situer aux environs de 2,0mg/100g. L’hémocyanine contenu dans l’hémolymphe du crabe peut réagir avec le sulfure d'hydrogène, pour produire en chauffant (100° C, 15 minutes) un pigment bleu. L’hémocyanine coagulée par la chaleur peut également réagir au sulfure d’hydrogène pour donner une couleur bleue. Le spectre de réflexion du complexe hémocianine-sulphide est très proche de celui de la chair bleue. La composition chimique de la substance bleue indique que la chair du crabe en conserve a été digérée par une protéase correspondant au complexe hémocianine-sulphide du crabe royal, excepté pour la teneur en sulfure. Inoue et Motohiro ont conclu que la substance provoquant le bleuissement de la chair du crabe en conserve est le complexe hémocianine-sulphide.
Osakabe a réussi à empêcher l’apparition du bleuissement du crabe en conserve par « chauffage fractionné à basse température » des crabes dont la carapace a été ôtée. Selon ses expériences, la température de coagulation de la protéine du sang des crabes se situe entre 69° C et 70° C, et celle de la protéine de la chair entre 59° C et 60° C. Donc, si les carcasses sont chauffées à 59° C - 60° C, la chair coagule, mais le sang non coagulé s’écoule. Une fois la chair ôtée de la carapace traitée à chauffage partiel, le sang s’écoule, laissant uniquement la chair. Lorsque celle-ci, qui a perdu son sang, est bouillie pendant quelques minutes et mise en conserve selon un procédé normal, le bleuissement n’apparaîtra pas dans le produit fini. En outre, lorsque la méthode de « chauffage fractionné à basse température » est utilisée, on peut préparer de la chair de crabe en conserve sans tendon (sans cartilage). Au Japon, la méthode d’Osakabe a révolutionné la mise en conserve de la chair de crabe.
Noircissement [NOTE: insérer une note brève et transférer le reste du texte dans l’annexe correspondante]
Le noircissement (mélanose) est causé par la formation de mélanine dans les segments ventraux de la queue des homards du fait de la réaction enzymatique d’oxydation (polyphénol-oxydase), suivie par auto-oxydation et polymérisation. On pense que les individus vivants ont un mécanisme latent de défense qui déclenche des processus enzymatiques provoquant la mélanose, dans certaines conditions anormales, selon l’importance des blessures et probablement le stress en cas de grandes souffrances.
Les essais enzymatiques hystochimiques menés avec des spécimens de homard soumis à deux traitements différents ont donné des résultats négatifs avec les homards anesthésiés dans l’eau glacée pendant 30 minutes, et positifs avec ceux porteurs de blessures. On peut en conclure que la distribution régulière des enzymes et des substrats est modifiée dans les tissus tégumentaires, et que l’accumulation de fluides (hémolymphe) dans les parties touchées résulte en des concentrations plus élevées de ces substances. En conséquence, le phénomène est probablement un mécanisme de défense hôte semblable à celui que l’on rencontre chez les insectes, où des réactions de défense humorale et/ou cellulaire les aident se remettre de blessures.
La croissance des homards est cyclique, des périodes de repos relatif alternant avec des périodes de modifications métaboliques dans l’épiderme, les tissus sous-épidermiques et l’hépatopancréas. Le noircissement se manifeste plus fréquemment lorsque les homards sont au stade C (entre mue) et au stade D (pré mue). Après la mue (ecdysis), au stade A et au début du stade B, les homards vivants endurcissent leur carapace (sclérotisation) puis forment de la mélanine, ce qui renforce leur protection contre les prédateurs, et ainsi les tâches noires apparaissent rarement.
On a constaté que la mélanose ne pouvait être évitée chez les homards traumatisés encore vivants pendant l’entreposage et la décongélation, alors qu’il n’y a aucun signe de noircissement chez ceux qui n’ont pas été endommagés avant de mourir.
Les traumatismes étant, en général, le fait de circonstances inévitables, les homards devraient être soumis, dans les plus brefs délais, à une congélation rapide et entreposés à une température aussi basse que possible afin d’éviter de déclencher la mélanisation. Il est recommandé de procéder à une décongélation rapide à l’aide d’eau courante afin d’éliminer les substances hydrosolubles formant la mélanine. Cependant, les homards affectés ne sont pas toujours de qualité inférieure, mais la manipulation sans précaution entraînera des pertes de qualité en peu de temps. Le noircissement ne se développe que dans les tissus tégumentaires et à la surface des muscles, et n’atteint pas les muscles internes.
Autres défauts
Les crabes du nord présentent souvent des infestations de sangsues marines qui sont des ectoparasites ou un noircissement de la carapace qui est une infection fungique. Ces défauts se rencontrent couramment.
13.2.2 Réduire au minimum la détérioration des crustacés – manipulation
Voir aussi Section 4.3 – Réduire au minimum la détérioration des poissons – manipulation, Avant-projet de Code d’usages des poissons et des produits de la pêche (ALINORM 01/18 – ANNEXE V)
• il est généralement admis que dans des conditions semblables, la qualité des crustacés se détériore plus rapidement que celle du poisson et il est donc fortement recommandé de maintenir les crustacés en vie jusqu’au moment où ils sont transformés ;
• les pattes et autres appendices des crustacés étant très fragiles et les dommages pouvant provoquer des infections et affaiblir le crustacé, les crustacés vivants devraient être manipulés à tout moment avec précaution ;
• les réservoirs utilisés pour contenir des crustacés vivants devraient être placés et construits de manière à assurer la survie des crustacés ;
• la durée est l’un des facteurs les plus importants pour contrôler la transformation des crabes. Il est fortement recommandé que toutes les opérations de transformation soient effectuées dans les délais les plus brefs;
• [la bonne qualité des sections de crabe produites au terme des opérations de parage peut être maintenue si elles sont cuites, réfrigérées ou congelées immédiatement;]
• les crustacés vivants devraient être entreposés avec soin dans des bacs, des puisards, des casiers, des sacs à large maille ou dans des boîtes recouvertes de sacs humides et maintenus à une température aussi basse que possible, selon l’espèce concernée ;
• les réservoirs destinés à l’entreposage sont considérés supérieurs aux puisards pour des opérations de manutention à long terme ;
• il est préférable d’employer pour le transport des sacs propres de chanvre grossier ou de jute. Il ne faudrait pas utiliser de sacs en matériaux synthétiques ;
• lorsqu’on utilise des sacs à larges mailles pour le transport, il faudrait éviter la présence de mucus ou de boue qui provoque la suffocation des crustacés ;
• il faudrait assurer l’humidité appropriée pour maintenir les crustacés en vie dans les sacs pour le transport ;
• il faudrait bander dès que possible après la capture les pinces des espèces qui tendent à se mutiler ;
• s’il n’est pas possible de conserver les crustacés en vie jusqu’au moment de la transformation, il faudrait tuer les homards et parer les crabes. Les queues et sections, respectivement, devraient être séparées et nettoyées avec soin avant d’être réfrigérées ou refroidies à la température de la glace fondante, dans les plus brefs délais.
13.3 Opérations de transformation – homards et crabes
Lorsqu’une usine de transformation a établi un programme de conditions préalables (section 3) les principes HACCP (section 5) peuvent être appliqués à chacun des procédés au sein de l’usine.
Cette section présente trois exemples de produits dérivés de homards et de crabes. Une place particulière a été accordée aux produits nécessitant un traitement thermique du fait de leur incidence potentielle sur la sécurité sanitaire de l’aliment (telle la manipulation après la transformation). Les produits et les diagrammes correspondants sont les suivants: Queues de homard cru congelées (fig. 13.3.1), Homard entier cuit réfrigéré/Chair de homard cuite réfrigérée (fig. 13.3.2) et Chair de crabe pasteurisée réfrigérée (fig. 13.3.3). On trouvera aux Annexe A et B une référence aux autres produits de homards et de crabes.
Figure 13.1. Exemple de diagramme pour une chaîne de transformation de queues de homard crues congelées
13.3.1 Queues de homard crues congelées
13.3.1.1 Réception des homards vivants (Étape de transformation n°1)
Dangers potentiels: |
Phycotoxines (IPM). |
Défauts potentiels: |
Réception de homards faibles ou blessés, mortalité des homards |
Conseils techniques: |
|
• les homards vivants devraient être inspectés dès réception afin de vérifier qu’ils sont en vie, ce dont témoigne l’activité vigoureuse des pattes et la queue qui se recourbe légèrement sous le corps du homard lorsqu’on le soulève ;
• les homards morts ou pouvant être un danger pour l’homme ne devraient pas être transformés, et devraient être rejetés et éliminés d’une manière appropriée;
• les homards faibles devraient être transformés immédiatement;
• les pattes et autres appendices des homards étant très fragiles et les dommages pouvant causer des infections et les affaiblir, les homards vivants devraient être manipulés à tout moment avec les plus grandes précautions. Ceux qui manipulent les homards devraient avoir les compétences voulues ;
• ceux qui manipulent les homards et le personnel approprié devraient recevoir une formation sur l’identification des espèces et avoir communication des spécifications du produit afin de garantir la salubrité des homards à leur arrivée. Il faudra être particulièrement attentif à la réception et au tri des espèces de homards présentant un risque de toxine IPM ;
• les homards devraient être rejetés s’il est avéré qu’ils contiennent des substances dangereuses ou étrangères et/ou des défauts qui ne seront pas éliminés ou réduits à un niveau acceptable par les procédures normales de tri ou de préparation. Il faudrait procéder à une évaluation appropriée afin de déterminer la ou les raisons de la perte de maîtrise et modifier le plan HACCP ou DAP en conséquence.
13.3.1.2 Conservation des homards vivants (Étape de transformation n° 2)
Voir aussi Section 13.2.2 – Réduire au minimum la détérioration des crustacés – manipulation, du présent document. Voir aussi « Section 6.1.2 – Qualité de l’eau »).
Dangers potentiels: |
Peu probables |
Défauts potentiels: |
Mortalité des homards |
Conseils techniques: |
|
• tous les homards vivants devraient être transformés dans les plus brefs délais;
• la durée d’entreposage devrait être contrôlée le cas échéant et aussi brève que possible;
• afin de réduire au minimum les pertes dues aux blessures et à la mortalité pendant la captivité, notamment au stade de la mue des homards, il faudrait éviter leur surnombre et contrôler la densité d’entreposage;
• en ce qui concerne l’entreposage à court terme, les homards vivants devraient être mis dans des récipients appropriés, et les réservoirs et puisards à terre devraient être dotés d’un système de circulation d’eau de mer;
• les homards morts ne devraient pas être transformés et devraient être rejetés et éliminés de manière appropriée. Il faudrait procéder à une évaluation appropriée afin de déterminer la ou les raisons de la perte de maîtrise et modifier le plan DAP en conséquence.
13.3.1.3 Équeutage (Étape de transformation n° 3)
Dangers potentiels: |
Contamination microbiologique |
|
Défauts potentiels |
peu probables | |
Conseils techniques: |
||
• lorsque les homards ne sont pas débarqués vivants, il faudrait séparer la queue du céphalothorax immédiatement après la capture. Cette opération devrait être effectuée dès que les homards sont amenés à bord. Les queues devraient être séparées et nettoyées avec précaution avant congélation ou réfrigération à la température de la glace fondante, ce qui doit être fait le plus rapidement possible;
• l’équeutage devrait être effectué le plus rapidement possible.
13.3.1.4 Lavage (Étape de transformation n°4)
Voir aussi section 8.1.5 – Lavage et éviscération
Dangers potentiels: |
peu probables |
Défauts potentiels: |
peu probables |
Conseils techniques: |
|
• [Les queues de homards devraient être lavées dans de grandes quantités d’eau potable ou d’eau de mer propre, [ou avec de l’eau chlorée] afin d’ôter toutes les impuretés]
13.3.1.5 Application d’additifs aux queues de homards (Étapes de transformation n°5 & 10)
Dangers potentiels: |
Utilisation d’additifs non autorisés; application inappropriée de sulfites2. |
Défauts potentiels: |
Contamination physique, tâches noires dues à l’application inappropriée de sulphites2, application incorrecte de phosphates2. |
Conseils techniques: |
|
• le mélange et l’application des additifs demande des compétences appropriées;
• vérifications régulières des quantités d’additifs appliquées.
13.3.1.6 Entreposage frigorifique (Étape de transformation n°6)
Voir sections 4.2 – Contrôle de la durée et de la température et 8.1.2 - Entreposage frigorifique.
Dangers potentiels: |
peu probables. |
Défauts potentiels: |
peu probables |
Conseils techniques: |
|
• il n’est pas recommandé d’entreposer les queues de homards dans l’eau de mer réfrigérée, car une quantité excessive de sel pénètre rapidement dans le muscle. Toutefois, on peut se servir de systèmes d’eau de mer réfrigérée pour un refroidissement rapide avant congélation ou entreposage sous glace;
13.3.1.7 Déveinage/Parage/Lavage (Étape de transformation n° 7)
voir Section 8.1.5 – Lavage et éviscération, Avant-projet de Code d’usages pour les poissons et les produits de la mer (ALINORM 01/18 – ANNEXE V)
Dangers potentiels: |
contamination microbiologique |
Défauts potentiels: |
déveinage incomplet, décomposition, membrane noire attachée à la carapace, contamination physique |
Conseils techniques: |
|
• les intestins devraient être éliminés immédiatement et les méthodes suivantes envisagées : éjection par pression de l’eau, aspiration, ou élimination physique avec des ustensiles appropriés (tels ciseaux, couteaux ou extracteurs) ;
• ceux qui manipulent les homards devraient acquérir les compétences nécessaires, notamment l’élimination de la membrane et du sang de l’extrémité thoracique de la queue ;
• un approvisionnement adéquat en eau de mer propre ou en eau potable [ou eau chlorée] devrait être assuré pour le lavage des queues de homards déveinées et parées en vue d’éliminer tous les débris d’intestins ou leurs contenus ;
• selon le déroulement des opérations sur le bateau ou dans l’usine de transformation, et lorsqu’un seuil critique pour le régime temps/température a été fixé pour la maîtrise des odeurs et des goûts indésirables, persistants et nets, indicateurs de décomposition, les queues de homards déveinées ou parées devraient être lavées et mises dans la glace ou réfrigérées de manière appropriée dans des récipients propres et entreposés dans des zones conçues à cet effet au sein de l’usine de transformation;
13.3.1.8 Calibrage (Étape de transformation n° 8)
Dangers potentiels: |
peu probables |
Défauts potentiels: |
calibrage incorrect |
Conseils techniques: |
|
• les queues de homards devraient être calibrées selon les espèces, tailles et poids requis pour le marché prévu, afin d’assurer l’intégrité économique du produit final ;
• des balances étalonnées sont nécessaires pour un calibrage correct.
13.3.1.9 Pesage (Étape de transformation n° 9)
Dangers potentiels: |
peu probables |
Défauts potentiels: |
poids net erroné |
Conseils techniques: |
|
• les balances devraient être étalonnées régulièrement à l’aide d’une masse normalisée pour en garantir l’exactitude.
13.3.1.10 Empaquetage et Emballage (Étapes de transformation n° 11 & 13)
Dangers potentiels: |
peu probables |
Défauts potentiels: |
déshydratation ultérieure |
Conseils techniques: |
|
• les matériaux d’emballage devraient être propres, solides, durables, adaptés à l’usage prévu et convenant aux aliments ;
• il faudra veiller à ce que l’extrémité thoracique de la queue soit complètement empaquetée pour éviter la déshydratation.
13.3.1.11 Congélation (Étape de transformation n° 12)
Voir section 8.3.1 – Congélation
Dangers potentiels: |
peu probables |
Défauts potentiels: |
peu probables |
Conseils techniques: |
|
• il faudrait utiliser des systèmes de congélation à circulation d’air rapide ou à nitrogène liquide pour obtenir des queues de homards de grande qualité ;
• il n’est pas recommandé de congeler ou d’entreposer les homards entiers non cuits.
13.3.1.12 Étiquetage (Étape de transformation n° 14)
Voir Section 8.2.3 « Étiquetage ».
Dangers potentiels: |
Absence d’étiquetage des additifs allergisants |
Défauts potentiels: |
Étiquetage incorrect |
Conseils techniques: |
|
• en cas d’utilisation de sulfites dans le procédé, il faut veiller à ce que cet additif soit correctement indiqué sur l’étiquette.
13.3.1.13 Entreposage frigorifique (Étape de transformation n° 15)
Voir Section 8.1.3 – entreposage frigorifique
Dangers potentiels: |
peu probables |
Défauts potentiels: |
peu probables |
Conseils techniques: |
|
13.3.1.14 Réception des additifs, des emballages et des étiquettes (Étapes de transformation n° 16 & 18)
voir section 8.5.1 – Réception – Emballages, étiquettes & ingrédients
Dangers potentiels: |
contamination biologique, chimique et physique |
Défauts potentiels: |
description erronée |
Conseils techniques: |
|
13.3.1.15 Entreposage des additifs, des emballages et des étiquettes (Étapes de transformation 17 & 19)
voir section 8.5.2 – Entreposage – Emballages, étiquettes & ingrédients
Dangers potentiels: |
contamination biologique et chimique |
Défauts potentiels: |
peu probables |
Conseils techniques: |
|
![]()
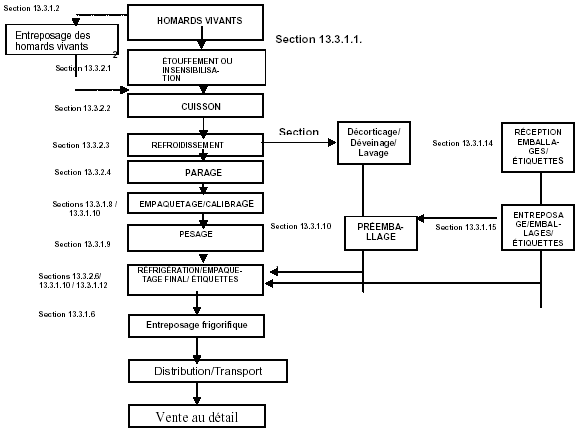

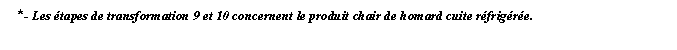
13.3.2 Homard entier cuit réfrigéré et chair de homard cuite réfrigérée
Cette section comprend les étapes de transformation concernant de manière spécifique le homard entier cuit réfrigéré et la chair de homard cuite réfrigérée.
13.3.2.1 Étouffement ou insensibilisation (Étape de transformation n° 3)
Dangers potentiels: |
Peu probables | |
Défauts potentiels: |
Peu probables | |
Conseils techniques: |
||
• on peut préparer certaines espèces (sauf Homarus) en provoquant leur étouffement par suffocation dans de l’eau propre à faible teneur en oxygène ou en les plongeant dans de l’eau propre réfrigérée ;
• on peut également procéder par choc électrique (impulsion) dans l’eau potable, l’eau de mer propre ou la saumure.
13.3.2.2 Cuisson (Étape de transformation n° 4)
Dangers potentiels: |
Survie de micro-organismes pathogènes du fait de cuisson insuffisante |
Défauts potentiels: |
trop ou pas assez cuit |
Conseils techniques: |
|
• il faudrait concevoir un programme pour la cuisson à l’eau ou à la vapeur qui tienne compte des paramètres appropriés pouvant avoir une incidence, comme la durée et la température et la taille du homard;
• la cuisson devrait être effectuée par un personnel dûment formé ayant acquis les compétences nécessaires pour veiller à ce que tous les homards soient cuits dans des conditions de durée et de température semblables et de pénétration de la chaleur adéquate;
• les appareils de cuisson devraient être munis de thermomètres indiquant la température de cuisson. L’installation de thermomètres enregistreurs est fortement recommandée. Il faudrait également un dispositif simple indiquant le temps de cuisson.
• les homards devraient être cuits en fonction de leur taille et jusqu’à ce qu’ils prennent une couleur rouge orangée uniforme et, selon le produit, jusqu’à ce que la chair puisse être ôtée facilement de la carapace. Une cuisson trop prolongée entraîne une contraction excessive de la chair et une cuisson insuffisante rend difficile la séparation de la chair et de la carapace;
13.3.2.3 Refroidissement (Étape de transformation n°5)
Dangers potentiels: |
Peu probables |
Défauts potentiels: |
Peu probables |
Conseils techniques: |
|
• la durée du refroidissement devrait être aussi brève que possible, en prenant toutes les précautions utiles afin d’éviter la contamination du produit au cours de cette période;
• le refroidissement devrait être effectué de manière appropriée, immédiatement après la cuisson, afin de terminer celle-ci de façon uniforme pour l’ensemble du lot et pour éviter de maintenir les homards à des températures susceptibles d’encourager la croissance de bactéries;
13.3.2.4 Parage (Étape de transformation n° 6)
Dangers potentiels: |
contamination microbiologique |
Défauts potentiels: |
Peu probables |
Conseils techniques: |
|
• un approvisionnement suffisant en eau de mer propre, eau potable ou [eau chlorée] doit permettre d’éliminer les protéines coagulées qui adhèrent aux homards. Il suffit en général de laver par pulvérisation sur une bande transporteuse, mais il peut se révéler nécessaire de les brosser à la main. Ces méthodes peuvent être combinées;
• toutes les surfaces et les brosses devraient être nettoyées fréquemment pendant l’opération afin de réduire au minimum l’activité microbienne des surfaces de contact et des ustensiles ;
13.3.2.5 Décorticage, déveinage et lavage (étape de transformation n° 10)
Dangers potentiels: |
recontamination microbiologique pendant le décortiquage et le déveinage, prolifération microbienne, développement de toxines microbiennes |
Défauts potentiels: |
présence de fragments de carapace |
Conseils techniques: |
|
• le décorticage et le déveinage des homards cuits devraient être effectués rapidement et avec soin, de manière que le produit obtenu soit attrayant et d’éviter la contamination croisée du produit cuit avec des crustacés crus ou tout matériel douteux ;
• selon le déroulement des opérations sur le bateau ou dans l’usine de transformation, et lorsqu’un seuil critique pour le régime temps/température a été fixé pour la maîtrise des dangers, les homards décortiqués ou déveinés devraient être lavés et refroidis dans des récipients propres et entreposés dans des zones conçues à cet effet dans l’usine de transformation;
• la chair de homard devrait être soigneusement lavée sur toutes ses faces dans de l’eau potable froide, de l’eau de mer propre ou de [l’eau chlorée];
13.3.2.6 Refroidissement, emballage final, étiquetage (étape de transformation n° 11)
Voir Section 8.2.3 « Étiquetage ».
Dangers potentiels: |
Peu probables |
Défauts potentiels: |
Étiquetage incorrect |
Conseils techniques: |
|
• les matériaux d’emballage devraient être propres, solides, durables, adaptés à l’usage prévu et convenant aux aliments ;
• il faudrait procéder immédiatement à la réfrigération des homards entiers ou de la chair de homard, destinés à être vendus frais après cuisson et les maintenir à la température de la glace fondante ;
• la glace utilisée pour la réfrigération devrait être fabriquée à l’aide d’eau potable, d’eau de mer propre ou d’[eau chlorée] ;

![]()
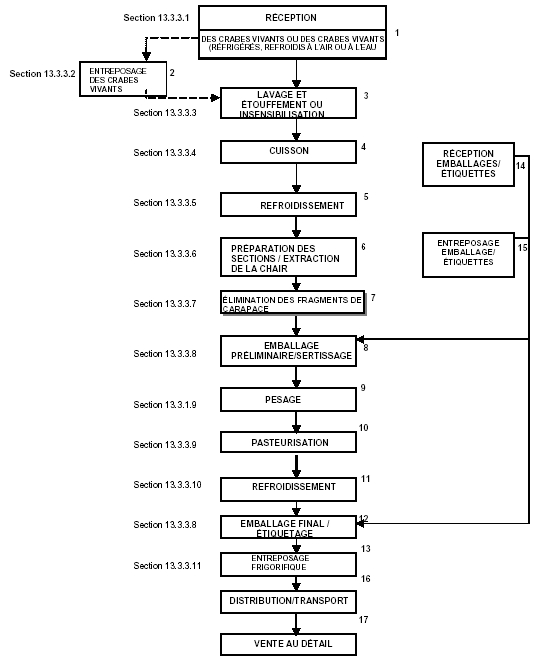

13.3.3 Chair de crabe pasteurisée réfrigérée
13.3.3.1 Réception des crabes vivants (Étape de transformation 1)
Voir aussi section 13.3.1.1 du présent document.
Dangers potentiels: |
Phycotoxines (IPM et IAM), parasite (Paragonimus westerman) |
Défauts potentiels: |
Réception de crabes faibles ou blessés, mortalité des crabes |
Conseils techniques: |
|
• les crabes vivants devraient être inspectés dès réception afin de vérifier qu’ils sont en vie, ce que montre l’activité vigoureuse des pattes.
• ceux qui manipulent les crabes et le personnel approprié devraient recevoir une formation sur l’identification des espèces et avoir communication des spécifications du produit afin de garantir la salubrité des crabes à leur arrivée. Il faudra être particulièrement attentif à la réception et au tri des espèces de crabes présentant un risque de toxines IPM et IAM et de parasites ainsi qu’aux défauts, tels que ectoparasites et noircissement de la carapace;
• dans les usines de transformation des crabes, tout crabe mort devrait être rejeté. Lorsqu’on transforme des sections de crabe, toute partie défectueuse ou détériorée devrait être ôtée et éliminée de manière appropriée ;
• les crabes faibles devraient être transformés immédiatement.
13.3.3.2 Conservation des crabes vivants (Étape de transformation 2)
Voir aussi [Section 6.1.2 – Qualité de l’eau] et section 13.3.1.2 – Conservation des homards vivants
Dangers potentiels: |
Peu probables |
Défauts potentiels: |
Mortalité des crabes |
Conseils techniques: |
|
• les crabes vivants devraient être placés dans de l’eau de mer recyclée, aux températures de leur milieu naturel ou légèrement inférieures, selon les espèces. Certaines espèces (par exemple, Ucides cordatus cordatus) peuvent être entreposées, pendant de brèves périodes, dans des réservoirs, sans eau;
• les crabes morts ne devraient pas êtres transformés et devraient être rejetés et éliminés de manière appropriée.
13.3.3.3 Lavage et étouffement ou insensibilisation (Étape de transformation 3)
Dangers potentiels: |
Peu probables |
Défauts potentiels: |
Pertes de pattes et de pinces, détérioration |
Conseils techniques: |
|
• les crabes devraient être lavés dans de grandes quantités d’eau potable courante, ou d’eau de mer propre, [ou d’eau chlorée] pour éliminer toutes les impuretés. Pour certaines espèces, il peut être nécessaire d’utiliser des brosses. Ces méthodes peuvent être associées;
• les crabes qui doivent être transformés entiers pour en tirer des produits frais ou congelés devraient être insensibilisés ou tués juste avant la cuisson afin d’éviter qu’ils perdent leurs pattes et leurs pinces. On peut procéder de l’une des façons ci-après:
• refroidir les crabes à 0° C au maximum, pendant [vingt minutes ou jusqu’à deux heures] , selon les espèces;
• immerger les crabes dans de l’eau potable ou de l’eau de mer propre dont la température dépasse de 10° C à 15° C celle du milieu naturel de l’espèce;
• transpercer les deux centres nerveux à l’aide d’une aiguille ou d’une baguette d’acier inoxydable. La baguette est introduite dans l’un des deux yeux et enfoncée dans l’orbite;
• étourdir les crabes en faisant passer un courant électrique de faible intensité par l’eau de mer ou l’eau potable dans laquelle les crabes sont immergés;
• les crabes morts se détériorant très rapidement et tout retard avant cuisson étant susceptible de réduire la qualité de la chair, les crabes insensibilisés ou tués devraient être cuits immédiatement;
13.3.3.4 Cuisson (Étape de transformation 4)
Dangers potentiels: |
Survie de micro-organismes pathogènes du fait de cuisson insuffisante. |
Défauts potentiels: |
trop ou pas assez cuit |
Conseils techniques: |
|
• lorsque le produit fini doit être commercialisé sous forme de crabes cuits dans leur carapace ou de chair décortiquée, il devrait être amené à une température voisine de celle de la glace fondante, puis être soit introduit dans la chaîne de distribution ou transformé dans les 18 heures ;
• la cuisson des crabes dans l’eau bouillante est généralement préférable à la cuisson à la vapeur. Celle-ci tend à dessécher la chair qui risque alors d’adhérer à la carapace. Il est recommandé de faire cuire les crabes en continu sur convoyeurs ;
• la cuisson devrait être effectuée par un personnel dûment formé qui a acquis les compétences nécessaires pour veiller à ce que tous les crabes soient exposés à la même température pendant la même durée au cours de l’opération ;
• une cuisson appropriée et uniforme est essentielle. Une cuisson trop prolongée entraîne une contraction excessive de la chair, une perte d’eau et une diminution des rendements, et une cuisson insuffisante rend malaisée la séparation de la chair et de la carapace ;
• il est difficile de préciser des conditions de temps et de température de cuisson générales par suite des différences de taille, de structure et de physiologie entre les crabes. En conséquence, il faudrait déterminer au préalable le temps et la température de l’opération de cuisson afin d’atteindre les niveaux microbiologiques requis de bactéries pathogènes. Dans l’ensemble, il faudrait que la chair atteigne une température minimum de 82 à 93° C (180 à 200 ° F).
• [On trouvera ci-après une récapitulation des méthodes actuellement utilisées dans l’industrie pour différentes espèces de crabe :
Crabe bleu (crabes entiers):
- autoclave à la vapeur pendant 10 minutes, une fois que la température de l’autoclave a atteint 121° C
- ébouillantage ou cuisson à la vapeur pendant 15 minutes au maximum, à 100°.
Sections de crabe royal:
- cuisson en une étape : environ 22 à 25 minutes dans de l’eau de mer à 100° C ;
- cuisson en deux étapes : environ 10 minutes à une température de 71 à 75° C, puis décorticage, et seconde cuisson pendant environ 10 minutes à 100° C, dans de la saumure
- cuisson partielle, pour les crabes destinés à être mis en boîte; les sections sont blanchies à 100° C pendant 10 à 15 minutes.
Sections de crabe de Tanner et de Geryon:
- cuisson en une étape : 7 à 15 minutes à 100° C, suivant la taille du crabe
- cuisson en deux étapes : 4 à 5 minutes dans de l’eau à la température de 71 à 82° C, décorticage puis deuxième cuisson dans la vapeur à 100° C, pendant 3 à 5 minutes.
Genre cancer:
- sections parées : 10 à 15 minutes à 100° C, dans de l’eau ou de la vapeur
- crabes entiers : suffocation, puis cuisson ou passage à la vapeur à 100° C, pendant 15 à 25 minutes, selon la taille.]
13.3.3.5 Refroidissement (Étape de transformation 5)
Dangers potentiels: |
Contamination microbiologique |
Défauts potentiels: |
peu probables |
Conseils techniques: |
|
• le refroidissement des crabes devrait se faire à l’air froid circulant, dans de l’eau potable ou de l’eau de mer propre courante ;
• lorsque la cuisson des crabes se fait de manière continue, le refroidissement continu est la meilleure procédure ;
• le refroidissement devrait être complété le plus rapidement possible, en prenant toutes les précautions utiles afin d’éviter la contamination du produit au cours de cette opération ;
• la même eau ne devrait être utilisée qu’une seule fois pour le refroidissement ;
• dans certaines espèces, la cavité ventrale contient une grande quantité d’eau, il est donc souhaitable de les égoutter suffisamment dans une zone réservée à cet usage ;
13.3.3.6 Préparation des sections/extraction de la chair (Étape de transformation 6)
Dangers potentiels: |
Recontamination par des micro-orgarnimes pathogènes, développement microbien, développement de toxines microbiennes, présence de fragments de carapace. |
Défauts potentiels: |
Peu probables |
Conseils techniques: |
|
• après le parage, il faudrait éliminer tous les restes de viscères et de branchies par brossage et par lavage. Un nettoyage soigneux à cette étape est fortement recommandé car il élimine le risque de retrouver des matières étrangères dans le produit fini ;
• il est recommandé d’utiliser du personnel différent pour les opérations concernant les crabes cuits et non cuits, afin d’éviter la contamination croisée ;
• il importe de contrôler avec soin les opérations de décorticage manuel ou mécanique de manière à éviter l’altération bactérienne et/ou la contamination par des matières étrangères;
• il est recommandé de procéder au décorticage, à l’emballage et à la réfrigération [(température interne de 4,5° C/40° F au maximum) ou congélation de tous les types de chair en deux heures au maximum] ;
• selon le déroulement des opérations sur le bateau ou dans l’usine de transformation, et lorsqu’un seuil critique pour le régime temps/température a été fixé pour la maîtrise des dangers, la chair de crabe devraient être réfrigérée de manière appropriée dans des récipients propres et entreposés dans des zones conçues à cet effet au sein de l’usine de transformation;
• étant donné les possibilités de contamination microbiologique, la transformation mécanique en continu de la chair blanche est préférable au décorticage, manuel ou non, en discontinu ;
• les pinces, les morceaux de pattes et de carapace contenant de la chair récupérable devraient être séparés, de manière rapide et efficace, de tous les autres déchets pendant toute la durée des opérations de décorticage et devraient être réfrigérés et tenus à l’abri de la contamination;
• il faudrait récupérer continuellement la chair subsistant dans les déchets;
13.3.3.7 Élimination des fragments de carapace (Étape de transformation 7)
Dangers potentiels: |
Présence de fragments de carapace, développement de toxines microbiennes |
Défauts potentiels: |
Peu probables |
Conseils techniques: |
|
• il faudrait veiller particulièrement à ce que les fragments de carapace soient éliminés de la chair de crabe car ils indisposent les consommateurs et peuvent parfois se révéler dangereux;
• afin de réduire le plus possible les retards, la chaîne pour l’extraction de la chair et l’élimination des fragments de carapace devrait être conçue en continu afin de permettre un déroulement des opérations sans arrêt ou ralentissement et l’élimination des déchets;
• selon le déroulement des opérations sur le bateau ou dans l’usine de transformation, et lorsqu’un seuil critique pour le régime temps/température a été fixé pour la maîtrise des dangers, la chair de crabe devraient être réfrigérée de manière appropriée dans des récipients propres et entreposés dans des zones conçues à cet effet au sein de l’usine de transformation.
• l’utilisation d’une lumière ultraviolette peut améliorer la détection des fragments de carapace dans la chair de crabe. Si elle est utilisée, elle devrait satisfaire aux spécifications de l’autorité compétente ;
13.3.3.8 Emballage préliminaire/sertissage/Emballage final/étiquetage (Étapes de transformation 8 et 12)
Voir Section 8.2.3 « Étiquetage » (NOTE: vérifier qu’il s’agisse du libellé de la norme)
Voir section 16.4.7 – Conditionnement en récipients (remplissage, sertissage et refroidissement)
Dangers potentiels: |
Contamination microbiologique ultérieure due à un sertissage défectueux |
Défauts potentiels: |
Étiquetage incorrect |
Conseils techniques: |
|
• les matériaux d’emballage devraient être propres, solides, durables, adaptés à l’usage prévu et convenant aux aliments ;
• le fonctionnement, l’entretien, l’inspection régulière et le réglage des sertisseuses devraient faire l’objet d’une attention particulière ;
• le sertissage devrait être effectué par du personnel qualifié dûment formé à cet effet ;
• l’intégrité du conditionnement du produit fini devrait être inspectée à intervalles réguliers par un personnel dûment formé afin de vérifier l’efficacité de la soudure et le fonctionnement correct de l’appareil de conditionnement;
13.3.3.9 Pasteurisation (Étape de transformation 10)
Dangers potentiels: |
Survie des pathogènes |
Défauts potentiels: |
Détérioration |
Conseils techniques: |
|
• la pasteurisation du produit devrait être effectuée par un personnel dûment formé ayant acquis les compétences nécessaires pour surveiller et garantir que tous les emballages soient exposés aux mêmes conditions de temps/température au cours de l’opération;
• la pasteurisation devrait être réalisée dans des récipients hermétiques;
• la chair de crabe devrait être pasteurisée immédiatement après décorticage manuel et emballage ;
• pour éviter toute détérioration possible du produit, la chair de crabe devrait être pasteurisée immédiatement. Il est préférable que la température de la chair de crabe soit de l’ordre de 18° C (64.4ºF) lorsque le récipient est fermé hermétiquement, ce qui laisse subsister un petit espace vide après qu’il soit ramené aux températures de l’entreposage frigorifique;
• il faudrait établir un régime temps/température pour la pasteurisation des différents produits de crabe, compte tenu du matériel de pasteurisation et de sa capacité, des propriétés physiques du crabe et des récipients de conditionnement, notamment la conductivité thermique, l’épaisseur, la forme et la température, afin de garantir que la pénétration de la chaleur a été la même pour tous les récipients du lot;
• la chair de crabe devrait être exposée à une température minimum de 85° C (185° F), pendant une minute au moins, au centre géométrique du récipient;
• le bain d’immersion devrait être préchauffé à 90° C (194° F) avant que les corbeilles chargées n’y soient placées. Il faudrait se préoccuper tout particulièrement d’assurer une circulation d’eau appropriée à l’intérieur du bain et autour de chaque boîte devant être pasteurisée. La température du bain d’eau chaude doit rester constante jusqu’à la fin des opérations;
• [les opérations de pasteurisation du crabe bleu supposent une durée de cuisson de 110 à 115 minutes pour les boîtes basses à fond circulaire de 570 cm3.];
• une fois établie les durées et températures appropriées, il faut s’y tenir; les opérations de pasteurisation devraient être normalisées et il faudrait à cette fin utiliser des thermomètres à thermocouple précis. Il est recommandé que le matériel neuf soit étalonné lors de son installation et étalonné à nouveau une fois par an ou chaque fois que des difficultés se présentent ;
• l’étalonnage et l’entretien approprié du matériel enregistrant la température devraient être effectués régulièrement pour assurer son exactitude ;
13.3.3.10 Refroidissement (Étape de transformation 11)
Dangers potentiels: |
Recontamination microbiologique due à un mauvais sertissage, mauvaise/brutale manipulation et eau contaminée, formation de toxines Clostridium botulinum. |
Défauts potentiels: |
Peu probables |
Conseils techniques: |
|
• le récipient de chair pasteurisée devrait être refroidi immédiatement après transformation.
• le refroidissement se fait dans de meilleures conditions dans un bain d’eau glacée. Le bain de refroidissement devrait être plus abondant que le bain de pasteurisation, pour lui permettre de contenir de la glace, ce qui se révèle nécessaire si la température de l’eau doit être maintenue en dessous de 8° C (46.4ºF) et si le refroidissement doit être le plus rapide possible. Il est inutile d’agiter l’eau car la différence de température entre le bain et le produit crée des courants de convection suffisants;
• l’eau utilisée pour le refroidissement devrait être [chlorée] afin d’éviter la recontamination du produit;
• le produit devrait être enlevé du bain de glace lorsque sa température a été ramenée en dessous de 3° C (38° F); il doit alors être transféré dans l’entrepôt frigorifique le plus rapidement possible;
• les caisses dans lesquelles sont placés les récipients maintenus en entreposage réfrigéré doivent permettre la libre circulation de l’air afin que le cycle de refroidissement soit complet;
• l’usine de transformation devrait mettre en place un système de contrôle des mouvements afin que le produit non pasteurisé ne puisse être mélangé avec tout produit pasteurisé.
13.3.3.11 Entreposage frigorifique (Étape de transformation 13)
Dangers potentiels: |
Formation de toxines Clostridium botulinum. |
Défauts potentiels: |
Peu probables |
Conseils techniques: |
|
• la chair de crabe pasteurisée devrait être transférée dans l’entrepôt frigorifique dans les délais les plus brefs ;
• le produit pasteurisé est périssable et à moins qu’il ne soit maintenu à l’état réfrigéré à une température minimale inférieure à 3° C (38° F), il est possible que Clostridium botulinum se développe et produise des toxines ;
• la chambre froide devrait être équipée avec un thermomètre indicateur étalonné. L’installation d’un thermomètre enregistreur est fortement recommandée;
SECTION 14 – TRANSFORMATION DES CREVETTES
Compte tenu des contrôles nécessaires aux différentes étapes de transformation, cette section présente des exemples de dangers et de défauts potentiels et contient des lignes directrices à caractère technique qui pourront servir pour élaborer des mesures de maîtrise et des actions correctrices. À une étape donnée seuls sont énumérés les dangers et les défauts qui risquent d’être introduits ou maîtrisés à cette même étape. Il convient de noter que, lors de la mise au point d’un plan HACCP et/ou DAP, il est impératif de consulter la section 5 qui donne des conseils pour l’application des principes HACCP et de l’analyse DAP. Cependant, dans le cadre du présent code d’usages, il est impossible de donner des détails sur les seuils critiques, la surveillance, la tenue des registres et la vérification relatifs à chaque étape, car ils diffèrent selon les dangers et les défauts.
14.1 CREVETTES CONGELÉES- GÉNÉRALITÉS
• le terme crevette est le nom générique, admis sur le plan international, des espèces Paneus, Pandalus et Palamindae.
• les crevettes destinées à la congélation proviennent de sources très diverses, qui peuvent aller des mers froides profondes, des eaux continentales tropicales de faible profondeur et des rivières jusqu’à l’aquaculture dans les régions tropicales et semi-tropicales.
• les méthodes de capture ou de récolte et de transformation sont également variées. Les espèces des régions du nord peuvent être capturées par des bateaux frigorifiques modernes, cuites, surgelées individuellement et emballées à bord sous leur forme finale pour la commercialisation. Toutefois, elles seront le plus souvent surgelées crues individuellement à bord pour transformation ultérieure dans les usines à terre, ou même débarquées réfrigérées sur glace. Une fois à terre, les crevettes de ces espèces sont invariablement précuites dans des chaînes de transformation en ligne intégrées; elles sont ensuite décortiquées mécaniquement, cuites, congelées, givrées et emballées. Par contre, l’espèce Paneus, ou les crevettes tropicales sont en général décortiquées à la main avant cuisson et congélation. Le plus souvent ces crevettes sont commercialisées crues, présentées sans la tête avec la carapace, ou comme crevettes en papillon, la tête et la carapace, sauf les nageoires caudales, sont ôtées et le corps est ouvert ventralement et en long, ce qui lui donne une présentation attirante.
• les crevettes tropicales peuvent être soumises à d’autres procédés comme le marinage et l’enrobage de pâte à frire et de panure.
• certains produits crus à base de crevettes, tout comme les produits cuits, pouvant être consommés sans autre transformation, les considérations de sécurité sanitaire sont d’une importance primordiale.
• les procédés décrits ci-dessus sont présentés dans deux diagrammes des opérations, mais il faut savoir que, du fait des caractéristiques différentes des méthodes de production, des plans HACCP/DAP doivent être conçus pour chaque produit.
• sauf la description ci-dessus de la cuisson à bord, il n’est fait aucune référence à la transformation des crevettes en mer ou dans les exploitations. On suppose que le produit est manipulé et transformé comme il convient, conformément aux sections pertinentes du code d’usage et que, si nécessaire, les étapes voulues de pré-préparation, comme l’étêtage, ont été effectuées avant réception dans les usines de transformation.
• les crevettes fraîches provenant d’estuaires et des eaux côtières peu profondes devraient être transformées dans les plus brefs délais après réception, en particulier si elles sont de source artisanale avec des moyens limités.
Figure 14.2 Diagramme des opérations pour la préparation de crevettes congelées selon les étapes ordinaires pour des produits cuits, entiers, cuits et décortiqués, crus préparés et semi-préparés.
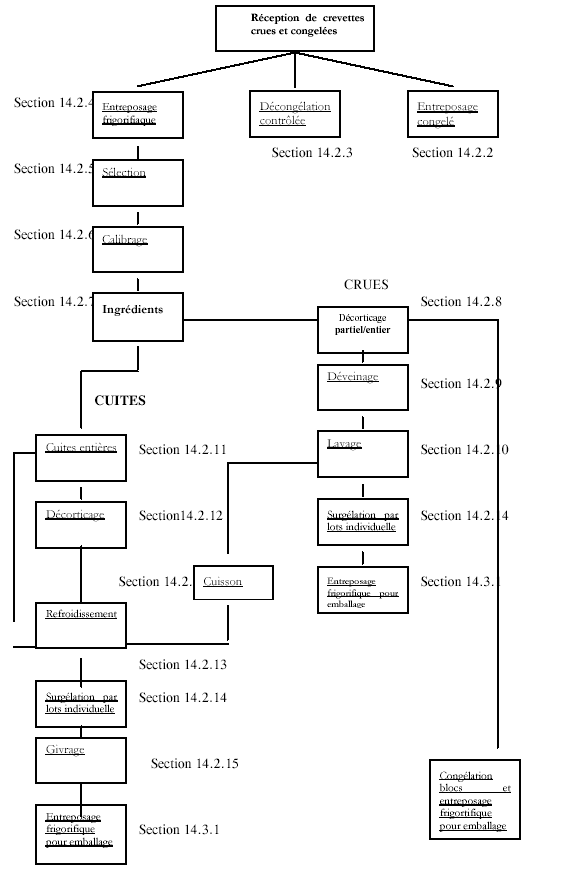
PRÉPARATION DES CREVETTES [ÉTAPES DE TRANSFORMATION 14.2.1 À 14.2.15]
14.2.1 Réception des crevettes crues fraîches et congelées (Étapes de transformation)
Dangers potentiels: phytotoxines (par exemple, IPM)
pathogènes/contamination microbiologique
antibiotiques/pesticides
Défauts potentiels: qualité variable du lot, mélange d’espèces, altérations
Conseils techniques:
• il faudrait définir des protocoles d’inspection qui couvrent les paramètres de qualité déterminés des plans HACCP et DAP et assurer la formation appropriée du personnel chargé de ces tâches.
• les crevettes devraient être contrôlées à la réception afin de garantir la traçabilité; il faut aussi vérifier qu’elles sont correctement mises dans la glace ou surgelées.
• les contrôles nécessaires seront fonction de l’origine et des antécédents connus concernant, par exemple, les phytotoxines dans les crevettes capturées en mer, la présence éventuelle d’antibiotiques dans les crevettes d’aquaculture, notamment en l’absence de certification de la part du fournisseur. On peut aussi appliquer des indicateurs chimiques pour les métaux lourds, les pesticides et des indicateurs de décomposition, par exemple TVBN.
• des contrôles microbiologiques devraient être effectués.
• Il faudrait entreposer les crevettes dans des installations appropriées et leur attribuer une date limite de transformation afin de garantir que les produits finis sont conformes aux paramètres de qualité.
14.2.2 Entreposage frigorifique
Dangers potentiels: peu probables
Défauts potentiels: dénaturation des protéines, déshydratation
Conseils techniques:
• l’emballage de protection devrait être intact, sinon il faudrait réemballer pour exclure toute possibilité de contamination et de déshydratation.
• les températures d’entreposage frigorifique devraient convenir à l’entreposage avec le moins possible de variations.
• le produit doit être transformé au mieux avant la date limite de l’emballage ou avant comme déterminé à la réception.
14.2.3 Décongélation contrôlée
Dangers potentiels: - détérioration/contamination microbiologique
- contamination provenant de l’emballage,
Défauts potentiels: détérioration de la qualité
Conseils techniques:
• les processus de décongélation peuvent s’appliquer à des crevettes congelées en blocs ou surgelées individuellement selon l’origine du produit cru. Les emballages externes et internes devraient être ôtés avant la décongélation pour éviter la contamination; il faudrait veiller notamment à ce que les blocs de crevettes congelées ne contiennent pas de restes de cartons paraffinés ou d’emballage de polyéthylène.
• les bacs de décongélation devraient être conçus à cet effet et permettre la décongélation par une eau à contre- courant si nécessaire afin de maintenir des températures les plus basses possibles. Il n’est pas recommandé de réutiliser l’eau.
• il faut pour la décongélation de la glace et de l’eau potable ou de l’eau de mer propre à une température maintenue à 20°C (68°F) au maximum en rajoutant de la glace.
• la décongélation devrait être effectuée le plus rapidement possible pour conserver la qualité.
• il convient d’équiper le convoyeur de sortie partant du bac de décongélation d’une série de pulvérisateurs à faible vitesse pour laver les crevettes avec de l’eau propre glacée.
• immédiatement après la décongélation, les crevettes devraient être mises dans de la glace ou rester réfrigérées avant transformation ultérieure pour éviter la rupture de la chaîne du froid.
14.2.4 Entreposage frigorifique
Dangers potentiels: peu probables
Défauts potentiels: détérioration de la qualité
Conseils techniques:
• entreposage frigorifique, de préférence sous glace dans des chambres froides à moins de 4oC après réception.
14.2.4 Sélection
Dangers potentiels: peu probables
Défauts potentiels: détérioration de la qualité
Conseils techniques:
• les crevettes peuvent être triées selon différentes catégories de qualité conformément aux spécifications. Cette opération devrait être réalisée dans les plus brefs délais et suivie de la remise dans la glace des crevettes
14.2.6 Calibrage
Dangers potentiels: microbiologique
Défauts potentiels: détérioration de la qualité
Conseils techniques:
• le calibrage des crevettes est en général effectué à l’aide de calibreurs mécaniques plus ou moins complexes. Des crevettes risquant d’être coincées entre les barres des calibreurs, un contrôle régulier est donc nécessaire pour éviter la présence de vieilles crevettes et la contamination bactériologique.
• les crevettes devraient être mises à nouveau dans la glace et entreposées au froid avant une transformation ultérieure.
14.2.7 Adjonction d’ingrédients et utilisation d’additifs
Dangers potentiels: contamination chimique et microbiologique
Défauts potentiels: détérioration de la qualité
qualité des ingrédients non conforme aux normes
Conseils techniques:
• certains traitements, conformes aux spécifications et à la législation, peuvent être appliqués aux crevettes afin d’améliorer les qualités organoleptiques, préserver les rendements ou les conserver pour une transformation ultérieure.
• on peut citer à titre d’exemple, le métabisulphite de sodium pour réduire le noircissement de la carapace, le benzoate de sodium pour prolonger la durée de conservation entre les processus et les polyphosphates de sodium pour ne pas perdre la succulence pendant la transformation et éviter les tâches noires après décorticage, tandis qu’on peut ajouter du sel ordinaire sous forme de saumure pour la saveur.
• ces ingrédients peuvent être ajoutés à différents stades, par exemple le sel ordinaire et les polyphosphates de sodium aux étapes de décongélation ou la saumure refroidie comme canal de déversement entre la cuisson et la congélation, ou comme givrage.
• quel que soit le stade auquel sont ajoutés les ingrédients, il est essentiel de surveiller le processus et le produit pour garantir que les normes en vigueur et les paramètres de qualité sont respectés et que, lorsque des solutions de trempage sont utilisées, celles-ci sont changées régulièrement conformément aux plans mis en place.
• les conditions de refroidissement doivent être maintenues tout au long du processus.
14.2.8 Décorticage total ou partiel
Dangers potentiels: contamination microbiologique croisée, matières étrangères
Défauts potentiels: détérioration de la qualité
fragments de carapace
Conseils techniques:
• ce procédé s’applique principalement aux crevettes tropicales et peut consister simplement à vérifier et préparer de grosses crevettes entières pour la congélation et à réserver les crevettes présentant un défaut pour un décorticage complet.
• les autres étapes du décorticage pourraient inclure le décorticage total ou le décorticage partiel laissant les nageoires caudales intactes.
• quel que soit le procédé, il faut s’assurer que les tables de décorticage sont nettoyées à l’aide de jets d’eau pour éliminer les crevettes contaminées et les fragments de carapace et que les crevettes sont rincées pour éviter la présence de fragments de carapace.
14.2.9 Déveinage
Dangers potentiels: contamination microbiologique croisée, contamination par les métaux, par des matières étrangères
Défauts potentiels: présence de matières inadmissibles, détérioration de la qualité
Conseils techniques:
• la veine est constituée par l’intestin qui apparaît comme une ligne noire dans la région dorsale supérieure de la chair des crevettes. Dans les grosses crevettes tropicales, elle est parfois invisible, granuleuse et peut être une source de contamination.
• le déveinage consiste à pratiquer une ouverture le long de la région dorsale à l’aide d’un rasoir et à ôter la veine en tirant. Cette opération peut aussi se faire partiellement avec des crevettes étêtées avec la carapace.
• cette opération est considérée comme mécanique bien qu’elle ait une forte composante de main-d'oeuvre, il faudra donc:
• mettre en place des programmes de nettoyage et d’entretien prévoyant l’approbation d’un personnel dûment formé avant, pendant et après la transformation.
• garantir également que les crevettes détériorées et contaminées sont retirées de la chaîne et qu’il n’y a pas d’accumulation de débris.
14.2.10 Lavage
Dangers potentiels: contamination microbiologique
Défauts potentiels: détérioration de la qualité, contamination
Conseils techniques:
• le lavage des crevettes décortiquées et déveinées est essentiel pour garantir l’élimination des fragments de veine et de carapace.
• il faudrait égoutter et refroidir les crevettes dans les plus brefs délais avant transformation ultérieure.
14.2.11 Procédés de cuisson
Dangers potentiels: manque de cuisson, contamination microbiologique croisée
Défauts de qualité potentiels: trop ou pas assez cuit
Conseils techniques:
• la procédure de cuisson, en particulier la durée et la température, devrait être définie avec précision conformément aux spécifications du produit fini, par exemple s’il doit être consommé sans autre transformation et la nature et l’origine de la crevette crue et l’uniformité de calibrage.
• le plan de cuisson doit être contrôlé avant chaque lot et, lorsque des installations de cuisson en continu sont utilisées, l’enregistrement continu des paramètres du processus devrait être disponible.
• il ne faudrait utiliser que de l’eau potable pour la cuisson, sous forme d’eau ou d’injection de vapeur.
• les températures de cuisson devraient être contrôlées, par prélèvement d’échantillons et enregistrement du processus pour les crevettes les plus grosses.
• des plans d’entretien et de nettoyage devraient être prévus pour les installations de cuisson et toutes les opérations devraient être confiées uniquement à un personnel dûment formé.
• à la sortie du cycle de cuisson, les crevettes devraient être séparées de manière adéquate à l’aide d’instruments différents afin d’éviter toute contamination croisée.
14.2.12 Décorticage des crevettes cuites
Dangers potentiels: contamination croisée
Défauts potentiels: présence de carapace
Conseils techniques:
• concerne surtout l’espèce Pandalus de crevettes d’eaux froides ; il s’agit d’un procédé très mécanisé en chaîne avec cuisson, refroidissement et congélation.
• les plans de nettoyage et d’entretien devraient être mis en place et appliqués par un personnel dûment qualifié afin de garantir l’efficacité et la sécurité sanitaire de la transformation.
14.2.13 Refroidissement
Dangers potentiels: contamination microbiologique
Défauts potentiels: peu probables
Conseils techniques:
• il faudrait refroidir les crevettes cuites aussi vite que possible pour amener le produit à une fourchette de température limitant la prolifération bactérienne ou la production de toxines.
• les plans de refroidissement devraient permettre de contrôler la température et la durée de l’opération, des plans d’entretien et de nettoyage devraient être mis en place et appliqués par un personnel dûment formé.
• seule de l’eau potable froide/glacée devrait être utilisée pour le refroidissement. On n’utilisera pas la même eau pour plusieurs lots mais, pour les opérations en continu on définira une procédure complémentaire et une durée maximale d’utilisation.
• la séparation entre produit cru et produit cuit est indispensable.
• après cuisson et égouttage les crevettes devraient être congelées le plus rapidement possible, en évitant toute contamination ambiante.
14.2.14 Processus de congélation
Dangers potentiels: microbiologique
Défauts potentiels: congélation lente – texture et agglutination des crevettes
Conseils techniques:
• la congélation est une opération qui varie énormément selon le type de produit. Le procédé le plus simple consistera à congeler des crevettes entières ou sans tête en bloc ou en plaque dans des cartons conçus à cet effet dans lesquels de l’eau est versée pour former un bloc de glace protecteur.
• à l’opposé, les crevettes d’eaux froides de l’espèce Pandalus, cuites et décortiquées, sont congelées en général par de systèmes de lits fluidifiés, tandis qu’un grand nombre des produits de crevettes tropicales sont surgelés individuellement soit sur des plateaux dans des congélateurs à air ou dans des congélateurs à courroie continue.
• quel que soit le procédé de congélation, les conditions de congélation spécifiées devront être respectés et , en ce qui concerne les produits surgelés individuellement, il ne doit pas y avoir d’agglutination, c’est-à-dire, de pièces congelées ensemble. Placer des produits dans un congélateur à air avant qu’il n’ait atteint la température voulue peut entraîner le givrage, la congélation lente et la contamination.
• les congélateurs sont des appareils complexes qui nécessitent des plans de nettoyage et d’entretien appliqués par un personnel dûment formé.
14.2.15 Givrage
Dangers potentiels: contamination microbiologique croisée
Défauts potentiels: givrage défectueux, givrage trop épais, agglutination, étiquetage erroné.
Conseils techniques:
• le givrage est appliqué aux crevettes congelées pour les protéger de la déshydratation et conserver la qualité pendant l’entreposage et la distribution.
• les crevettes congelées en blocs de glace est la forme la plus simple de givrage, suivi ensuite de l’immersion et de l’égouttage des crevettes congelées dans de l’eau potable refroidie. Un processus plus complexe consiste à pulvériser de l’eau froide sur des crevettes calibrées congelées qui sont placées sur des courroies vibrantes de sorte que les crevettes passent à une vitesse constante pour recevoir une pellicule de givre régulière et calculée.
• l’idéal serait que les crevettes givrées subissent une recongélation secondaire avant l’emballage, ou alors elles devraient être emballées dans les plus brefs délais et transférées dans l’entreposage frigorifique. Dans le cas contraire, les crevettes risquent de se congeler ensemble et de s’agglutiner quand le givrage se durcit.
• il existe des méthodes Codex permettant de déterminer le givrage.
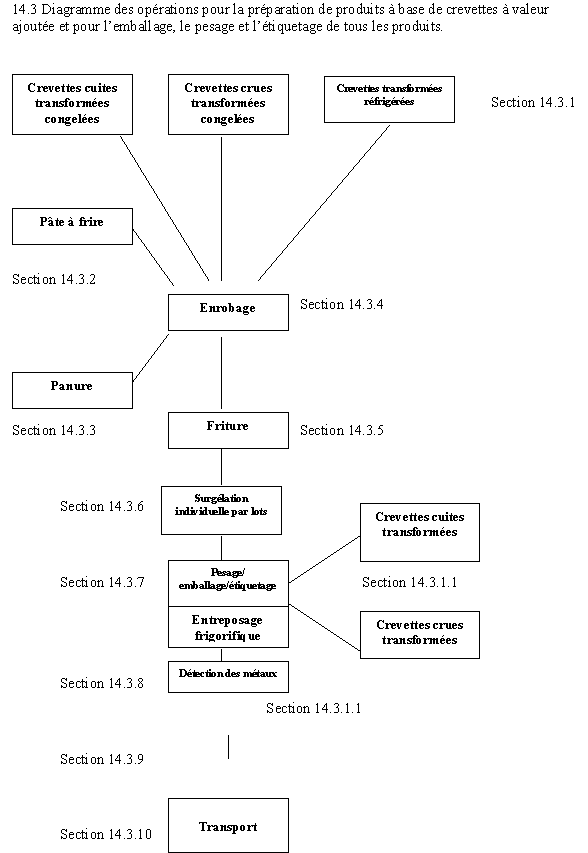
14.3.1 Autres transformations et emballage
Dangers potentiels: contamination microbiologique et production de toxine
Défauts potentiels: contamination par des matières étrangères
enrobages défectueux
14.3.4 Production de produits enrobés
Dangers potentiels: risques de feu dus à l’huile
toxines microbiologiques
Défauts potentiels: enrobage défectueux et questions d’étiquetage
panure brûlée, texture de mauvaise qualité
Conseils techniques:
• les principales opérations en ce qui concerne les produits enrobés à valeur ajoutée comprennent l’utilisation de crevettes cuites congelées, de crevettes crues congelées ou de crevettes de l’une ou l’autre sorte retirées réfrigérées immédiatement de la chaîne de transformation.
• lorsqu’on utilise des produits réfrigérés, les questions de qualité et de détérioration continue des protéines doivent être prises en compte.
• lorsqu’on utilise des produits congelés, des mesures doivent être prises pour qu’ils restent congelés afin de préserver la qualité et la texture. Il faut noter que les produits à base de crevettes congelées ne devraient pas être givrés sous peine de voir l’enrobage éclater au moment de la friture ou de la cuisson.
14.3.2 Pâte à frire
• il faudrait vérifier que les ingrédients de pâte à frire en poudre sont conformes aux spécifications d’achat et, de préférence, les tamiser avant usage afin d’éliminer tout reste d’emballage ou matières étrangères.
• l’eau devrait être potable et refroidie
• les mélanges pour pâte à frire devraient être conformes aux recettes et à la viscosité prévues afin de garantir que l’enrobage adhère de manière correcte au produit.
• la formation de toxines bactériennes étant possible dans les mélanges pour pâte à frire, il faudrait établir les durées et les températures d’utilisation, et déterminer et appliquer des plans de nettoyage du matériel.
• les pâtes à frire de type tempura peuvent être utilisées, auquel cas il est probable qu’il n’y aura pas de panage. Les températures et durées de la friture seront toutefois déterminantes pour assurer une texture correcte.
• lorsque la pâte à frire sert à faire adhérer la panure, la formulation et la viscosité seront différentes que pour les types tempura.
14.3.3 Panure
• il convient de vérifier que la formulation et la mouture de la panure sont conformes aux spécifications d’achat et que son entreposage répond aux instructions du fournisseur afin d’éviter l’altération du produit.
14.3.5 Friture
• la friture est nécessaire pour les enrobages de pâte à frire de type tempura, mais ce n’est pas toujours le cas pour la panure bien qu’elle en assure l’adhésion.
• les installations de friture devraient être utilisées par un personnel dûment formé. L’huile devra être changée régulièrement pour éviter le rancissement par oxydation.
• la température de l’huile devrait être contrôlée pour éviter de brûler la panure ou les risques de feu.
14.3.6 SURGÉLATION INDIVIDUELLE
• les conditions de congélation sont analogues à celles décrites au paragraphe 14.2.14
14.3.7 Pesage, emballage et étiquetage de tous les produits
Dangers potentiels: peu probables
Défauts potentiels: étiquetage incorrect
détérioration de la qualité
Conseils techniques:
• tous les matériels pour l’emballage des produits y compris les colles et encres doivent être de qualité alimentaire, sans odeur et ne pas présenter le risque que des substances dangereuses pour la santé puissent être transférées à l’aliment emballé.
• tous les produits devraient être pesés dans leur emballage, les balances étant tarées de façon appropriées pour garantir que le poids est correct.
• lorsque les produits sont givrés, enrobés ou préparés d’une autre façon, il convient de vérifier que leur composition est conforme à la législation et aux indications de l’emballage.
• la liste des ingrédients figurant sur l’emballage devrait énumérer les ingrédients présents dans le produit par ordre décroissant de poids, y compris les additifs utilisés et encore présents dans le produit.
• tous les emballages devraient être réalisés de manière à garantir que les produits restent congelés et qu’ils sont soumis à des hausses de température minimales avant d’être à nouveau transférés dans l’entreposage frigorifique.
14.3.8 Détection des métaux
Dangers potentiels: contamination par des résidus métalliques
Défauts potentiels:
Conseils techniques:
• il faudrait vérifier la présence éventuelle de métaux dans l’emballage final à l’aide d’équipements réglés à la plus haute sensibilité possible.
• les emballages les plus importants seront contrôlés à une sensibilité plus faible que pour les emballages plus petits, il faudrait donc envisager de vérifier le produit avant l’emballage. Toutefois, à moins que l’on puisse éliminer la possibilité d’une nouvelle contamination avant l’emballage, il est encore préférable de contrôler le produit emballé.
14.3.9 Entreposage du produit fini
Dangers potentiels: peu probable
Défauts potentiels: défauts de texture et de saveur dues à des variations de la température, à des brûlures dues au froid, goût de réfrigérateur, goût de carton
• tous les produits finis devraient être entreposés à température de congélation dans un milieu propre, salubre et hygiénique.
• on évitera de fortes fluctuations de température durant l’entreposage (supérieures à 3°C).
• une durée d’entreposage trop longue (selon la teneur en graisse de l’espèce utilisée et le type d’enrobage) devrait être évitée.
• l’installation devrait pouvoir maintenir la température du poisson à -18°C ou moins avec des variations de température minimales.
• l’aire d’entreposage devrait être équipée d’un thermomètre précis étalonné. On recommande vivement l’emploi d’un thermomètre enregistreur.
• un plan de rotation systématique des stocks devrait être élaboré et suivi.
• les produits doivent être adéquatement protégés de la déshydratation, de la saleté et d’autres formes de contamination.
• tous les produits finis devraient être entreposés au congélateur pour permettre une bonne circulation de l’air.
14.3.11 Transport du produit fini
Dangers potentiels: peu probables
Défauts potentiels: altération de la qualité
Conseils techniques:
• durant toutes les étapes du transport, les conditions de surgélation doivent être maintenues à -18°C (fluctuation maximale ± 3°C) jusqu’à la destination finale du produit.
• il faudrait vérifier la propreté et l’adéquation du véhicule de transport pour les produits alimentaires congelés.
• on recommande l’emploi d’instruments d’enregistrement des températures avec le chargement.
SECTION 15 – TRANSFORMATION DES CÉPHALOPODES
Compte tenu des contrôles nécessaires aux différentes étapes de transformation, cette section présente des exemples de dangers et de défauts potentiels et contient des lignes directrices à caractère technique qui pourront servir pour élaborer des mesures de maîtrise et des actions correctrices. À une étape donnée seuls sont énumérés les dangers et les défauts qui risquent d’être introduits ou maîtrisés à cette même étape. Il convient de noter que, lors de la mise au point d’un plan HACCP et/ou DAP, il est impératif de consulter la section 5 qui donne des conseils pour l’application des principes HACCP et de l’analyse DAP. Cependant, dans le cadre du présent code d’usages, il est impossible de donner des détails sur les seuils critiques, la surveillance, la tenue des registres et la vérification relatifs à chaque étape, car ils diffèrent selon les dangers et les défauts.
Le présent code d’usages s’applique aux céphalopodes frais et transformés, dont les seiches (Sepia et Sepiella), les calmars (Alloteuthis, Berryteuthis, Dosidicus, Ilex, Lolliguncula, Loligo, Loliolus, Nototodarus, Ommastrephes, Onychoteuthis, Rossia, Sepiola, Sepioteuthis, Symplectoteuthis et Todarodes) et les pieuvres (Octopus et Eledone) destinés à la consommation humaine.
Les céphalopodes frais sont extrêmement périssables et devraient être manipulés à tout moment avec un grand soin et de manière à éviter la contamination et à inhiber la croissance des micro-organismes. Les céphalopodes ne devraient pas être exposés à la lumière directe du soleil ni aux effets desséchants des vents ou à tous les autres effets nocifs des éléments, mais devraient être soigneusement nettoyés et refroidis à la température de la glace fondante, soit 0°C (32°F), aussi vite que possible.
Le présent code donne un exemple d’un procédé de transformation des céphalopodes. La Figure 15.1 présente les étapes concernant la réception et la transformation des calmars frais. Il y a lieu de noter que les opérations de transformation des céphalopodes sont très variées et qu’elles ne sont décrites qu’à titre d’exemple.
Le diagramme ci-après est présenté uniquement à titre d’exemple. Pour
mettre en œuvre un plan HACCP, chaque usine devra établir un diagramme
complet et détaillé pour chaque procédé.

![]()
15.1 RÉCEPTION DES CÉPHALOPODES (ÉTAPE DE TRANSFORMATION 1)
Dangers potentiels: |
micro-organismes pathogènes, contamination chimique, parasites |
Défauts potentiels: |
Produits endommagés, matières étrangères |
Conseils techniques: |
|
• L’usine de transformation devrait mettre en place un programme pour l’inspection des céphalopodes au moment de la prise ou à leur arrivée dans l’établissement. Seuls les produits sains seront retenus pour être transformés.
• Les spécifications du produit pourraient inclure:
- caractéristiques organoleptiques comme l’apparence, l’odeur, la texture etc.
- indicateurs chimique de décomposition et / ou contamination comme par exemple TVBN, métaux lourds (cadmium)
- critères microbiologiques
- parasites, tels que Anasakis
- la présence de lacérations, de déchirures et de défauts de coloration de la peau, ou une teinte jaunâtre partant du foie et des organes de digestion à l’intérieur dans le manteau, sont les premières indications de la détérioration du produit.
• Le personnel chargé d’inspecter le produit devrait être formé et expérimenté en ce qui concerne les espèces pertinentes afin de reconnaître tous dangers ou défauts potentiels.
On trouvera d’autres renseignements à la Section 8 « Transformation du poisson frais, congelé ou haché » et dans les directives Codex concernant l’évaluation organoleptique du poisson et des crustacés en laboratoire.
15.2 ENTREPOSAGE DES CÉPHALOPODES
15.2.1 Entreposage frigorifique (Étape de transformations 2 et 10)
Dangers potentiels: |
Pathogènes microbiologiques |
Défauts potentiels: |
Décomposition, dommages physiques |
Conseils techniques: |
|
Voir Section 8.1.2 « Entreposage frigorifique »
15.2.2 Entreposage en congélation (Étape de transformations 2 et 10)
Dangers potentiels: |
Métaux lourds tels migration de cadmium depuis les viscères. |
Défauts potentiels: |
brûlure de congélation |
Conseils techniques: |
|
Voir section 8.1.3 « Entreposage frigorifique ».
• Il faudra tenir compte du fait que lorsqu’il y a de fortes concentrations de cadmium dans les viscères il peut y avoir migration de celui-ci dans la chair.
15.3 DÉCONGÉLATION CONTRÔLÉE (ÉTAPE DE TRANSFORMATION 3)
Dangers potentiels: |
Pathogènes microbiologiques |
Défauts potentiels: |
Décomposition, défaut de coloration |
Conseils techniques: |
|
• les paramètres de décongélation devront être définis clairement y compris la durée et la température, ce qui est important pour éviter l’apparition d’une coloration rose pale.
• des seuils critiques de durée et de température devront être déterminés pour la décongélation. Une attention particulière sera apportée au volume du produit décongelé afin de maîtriser la décoloration.
• lorsqu’on utilise l’eau pour la décongélation, elle doit être de qualité potable
• lorsqu’il s’agit d’eau recyclée, il faut prendre soin d’éviter l’accumulation de micro-organismes
Pour de plus amples détails voir Section 8.1.4 « Décongélation contrôlée ».
15.4 TRANCHAGE, ÉVISCÉRATION ET LAVAGE (ÉTAPE DE TRANSFORMATIONS 4, 5, 6, 11, 12 &13)
Dangers potentiels: |
Peu probables |
Défauts potentiels: |
présence de viscères, de parasites, de coquilles et de défauts de coloration. |
Conseils techniques: |
|
• l’éviscération doit enlever toutes les parties intestinales et éventuellement la coquille du céphalopode.
• tous les produits résultant de cette opération, c’est-à-dire ceux destinés à la consommation humaine, par exemple les tentacules, le manteau, doivent être manipulés de manière appropriée et hygiénique.
• il faut laver les céphalopodes dans de l’eau de mer propre ou de l’eau potable tout de suite après l’éviscération afin d’éliminer tout résidu de la cavité du tube et de réduire la quantité de micro-organismes présents sur le produit.
• il faudrait assurer un approvisionnement en eau de mer propre ou en eau potable suffisant pour laver les céphalopodes entiers ou les produits à base de céphalopodes
15.5 ÉPIAUTAGE, PARAGE (ÉTAPE DE TRANSFORMATION 7)
Dangers potentiels: |
peu probables |
Défauts potentiels: |
présence de matières inadmissibles, dommages dus à des morsures, dommages à la peau |
Conseils techniques: |
|
• la méthode d’épiautage ne devrait pas contaminer le produit ni permettre le développement de micro-organismes, par exemple l’épiautage enzymatique ou des techniques à l’eau chaude devraient avoir des paramètres relatifs à la durée et à la température bien précis pour empêcher le développement de micro-organismes.
• il faudrait prendre soin d’éviter la contamination croisée des produits par les déchets.
• il faudrait assurer un approvisionnement en eau de mer propre ou en eau potable suffisant pour laver le produit Durant et après l’épiautage.
15.6 CALIBRAGE/EMBALLAGE (ÉTAPE DE TRANSFORMATIONS 8 & 9)
Voir Section 8.2.3 « Étiquetage ».
Dangers potentiels: |
contamination microbiologique, chimique ou physique durant l’empaquetage |
Défauts potentiels: |
étiquetage incorrect, poids incorrect |
Conseils techniques: |
|
• les matériaux d’emballage devraient être propres, suffisants pour l’emploi auquel ils sont destinés et de qualité alimentaire;
• les opérations de calibrage et d’emballage devraient être effectuées dans les plus brefs délais afin d’éviter la détérioration des céphalopodes;
15.7 CONGÉLATION (ÉTAPE DE TRANSFORMATION 10)
Dangers potentiels: |
Parasites |
Défauts potentiels: |
brûlure par congélation, décomposition, perte de qualité due à une congélation lente. |
Conseils techniques: |
|
Les céphalopodes devraient être congelés aussi rapidement que possible afin d’éviter la détérioration du produit et la réduction de la durée de conservation qui s’en suit du fait de développement microbien et de réactions chimiques.
• les paramètres de durée et de température devraient garantir une congélation rapide du produit et tenir compte du matériel de congélation, de sa capacité, de la taille et de la forme du produit et du volume de production. La production devrait être fonction de la capacité de l’usine de transformation;
• si la congélation est utilisée comme point de contrôle des parasites, il faut établir des paramètres de durée et de température afin de garantir que les parasites ne sont plus viables;
• la température centrale du poisson congelé devrait être vérifiée régulièrement pour assurer que la congélation soit complète;
• il faudrait tenir des registres détaillés de toutes les opérations de congélation et d’entreposage frigorifique;
Pour d’autres orientations voir Section 8.3.1 « Congélation ».
15.8 EMBALLAGES, ÉTIQUETAGE ET INGRÉDIENTS – RÉCEPTION ET ENTREPOSAGE
Il faudrait prendre en compte les dangers et les défauts potentiels associés à l’emballage, l’étiquetage et la réception des ingrédients. Il est recommandé aux utilisateurs du présent code de consulter la Section 8.5 « Emballage, étiquettes et ingrédients ».
SECTION 17 - TRANSPORT
Le transport s’applique à toutes les sections et représente une étape du diagramme des opérations qui nécessite des compétences particulières et doit être considérée avec les mêmes soins que les autres étapes de transformation. Cette section présente des exemples de dangers et de défauts potentiels et contient des lignes directrices à caractère technique qui pourront servir pour élaborer des mesures de maîtrise et des actions correctrices. À une étape donnée seuls sont énumérés les dangers et les défauts qui risquent d’être introduits ou maîtrisés à cette même étape. Il convient de noter que, lors de la mise au point d’un plan HACCP et/ou DAP, il est impératif de consulter la section 5 qui donne des conseils pour l’application des principes HACCP et de l’analyse DAP. Cependant, dans le cadre du présent code d’usages, il est impossible de donner des détails sur les seuils critiques, la surveillance, la tenue des registres et la vérification relatifs à chaque étape, car ils diffèrent selon les dangers et les défauts.
Il est particulièrement important durant le transport des poissons et des produits de la pêche frais, congelés ou réfrigérés de veiller à réduire au minimum la hausse de température du produit et à ce que la température de 0° ou moins, selon le cas, soit maintenue dans des conditions contrôlées. De plus, des mesures appropriées devraient être appliqués pour réduire le plus possible les dommages aux produits ainsi qu’à leur emballage.
Dangers potentiels: |
Développement biochimique (histamine). Développement et contamination microbienne |
Défauts potentiels: |
Décomposition, dommage physique. Contamination chimique (carburants) . |
Conseils techniques: |
|
17.1 POUR LES PRODUITS FRAIS, RÉFRIGÉRÉS ET CONGONGELÉS
• refroidir les véhicules avant le chargement;
• éviter une exposition inutile à des températures élevées durant le chargement et le déchargement des poissons, mollusques et crustacées et de leurs produits;
• charger en veillant à ce que l’air circule librement entre les produits et les parois, planchers et plafonds; il est recommandé d’installer des dispositifs de stabilisation de la charge
• contrôler la température de l’air à l’intérieur de la cargaison durant le transport; il est recommandé d’installer un thermomètre enregistreur
• pendant le transport
- les produits congelés devraient être maintenus à –18°C ou moins (fluctuation maximale de +3°C)
- le poisson, les mollusques et les crustacées et leurs produits devraient être conservés à une température aussi proche que possible de 0°C. Les poissons entiers frais devraient être conservés en couches peu épaisses et entourés de quantités suffisantes de glace finement pilée; prévoir un écoulement adéquat pour assurer que l’eau provenant de la fonte de la glace ne reste pas au contact des produits ou ne soit pas une source de contamination croisée pour les produits dans d’autres conteneurs.
- [le transport du poisson frais dans des conteneurs avec des sacs de congélation à sec et sans glace devrait être envisagé le cas échéant;]
- [le transport du poisson dans une saumure réfrigérante, de l’eau de mer glacée ou réfrigérée (par exemple pour les poissons pélagiques devrait le cas échéant être envisagé;]
- Les produits transformés réfrigérés devraient être maintenus à la température indiquée par le transformateur [ne devrait pas, en général, dépasser 4° C].
- protéger comme il convient les poissons, crustacés, mollusques et leurs produits de la contamination par la poussière, de l’exposition à des températures plus élevées et aux effets desséchant du soleil et du vent.
17.2 POUR LES POISSONS, MOLLUSQUES ET CRUSTACéES VIVANTS
• voir les dispositions spécifiques énoncées dans les sections pertinentes du présent code.
17.3 POUR LES POISSONS, MOLLUSQUES ET CRUSTACéES EN CONSERVE
• voir les dispositions spécifiques énoncées à la section 16.
17.4 POUR TOUS LES PRODUITS
• avant d’effectuer le chargement, on vérifiera la propreté, l’adéquation et l’hygiène des conteneurs du camion;
• le chargement et le transport devraient être effectués de manière à éviter les dommages et la contamination des produits et à assurer l’intégrité de l’emballage.
SECTION 18 – VENTE AU DÉTAIL
Compte tenu des contrôles nécessaires aux différentes étapes de transformation, cette section présente des exemples de dangers et de défauts potentiels et contient des lignes directrices à caractère technique qui pourront servir pour élaborer des mesures de maîtrise et des actions correctrices. À une étape donnée seuls sont énumérés les dangers et les défauts qui risquent d’être introduits ou maîtrisés à cette même étape. Il convient de noter que, lors de la mise au point d’un plan HACCP et/ou DAP, il est impératif de consulter la section 5 qui donne des conseils pour l’application des principes HACCP et de l’analyse DAP. Cependant, dans le cadre du présent code d’usages, il est impossible de donner des détails sur les seuils critiques, la surveillance, la tenue des registres et la vérification relatifs à chaque étape, car ils diffèrent selon les dangers et les défauts.
Le poisson, les mollusques et les crustacées et leurs produits au détail devraient être reçus, manipulés, entreposés et présentés aux consommateurs de façon à réduire le plus possible les dangers et défauts relatifs à la sécurité sanitaire alimentaire et à maintenir les qualités essentielles. Conformément aux principes HACCP et DAP pour la sécurité sanitaire et la qualité des aliments, les produits devraient être achetés auprès de sources approuvées ou connues sous le contrôle des autorités sanitaires compétentes qui peuvent vérifier les contrôles. Les opérateurs de détail devraient élaborer et utiliser des spécifications écrites d’achat conçues pour garantir les niveaux requis de sécurité sanitaire et de qualité des aliments.
Une température d’entreposage appropriée après reception est fondamentale pour maintenir la sécurité sanitaire et les qualités essentielle du produit. Les produits réfrigérés devraient être entreposés dans de bonnes conditions d’hygiène à une température inférieure ou égale à 4°C (40°F), les produits conditionnés sous atmosphère modifiée (MAP) à 3°C (28°F) ou moins, tandis que les produits congelés devraient être entreposés à des températures inférieures ou égales à -18°C (0°F).
La préparation et l’emballage devraient être effectués conformément aux principes et recommandations énoncés à la Section 3, Programmes de conditions préalables et aux normes Codex d’étiquetage. Les produits présentés sur un étalage ouvert devrait être protégés du milieu ambiant par des dispositifs appropriés (protection contre les éternuements). Les poissons, mollusques et crustacés présentés devraient en permanence être maintenus à des températures et dans des conditions qui excluent le développement potentiel de bactéries, de toxines et d’autres dangers outre la perte de qualités essentielles.
L’information des consommateurs au point d’achat est importante pour garantir que la sécurité et la qualité des produits sont préservées; il peut s’agir, par exemple, d’écriteaux ou de dépliants, donnant des renseignements sur les procédés d’entreposage et de préparation et sur les risques que peuvent présenter les produits de la mer en cas de manipulation ou de préparation incorrectes.
Il faudrait établir un système permettant le traçage de l’origine et des codes des poissons, mollusques, crustacés et de leurs produits afin de faciliter le rappel des produits ou les enquêtes de santé publique en cas d’échec des procédés et des mesures mis en place pour la protection de la santé publique. Des systèmes de ce type existent dans certains pays pour les mollusques qui sont soumis à des obligations de marquage.
18.1 RÉCEPTION DU POISSON, DES MOLLUSQUES, DES CRUSTACéS ET DE LEURS PRODUITS POUR LA VENTE AU DÉTAIL – GÉNÉRALITÉS
Dangers potentiels: |
voir Réception 7.1, 8.1 | |
Défauts potentiels: |
voir Réception 7.1, 8.1 | |
Conseils techniques: |
||
• les bonnes conditions générales d’hygiène du véhicule de transport devraient être contrôlées régulièrement. Les produits présentant des signes d’impuretés, d’altération ou de contamination devraient être rejetés.
• il faudrait vérifier qu’il n’y a pas de risque de contamination croisée pour les produits se trouvant dans le véhicule de transport. Les produits cuits prêts à être consommés ne doivent pas avoir été au contact de produits crus, de jus ou de mollusques vivants et les mollusques crus ne doivent pas avoir été au contact d’autres poissons ou autres fruits de mer crus.
• la conformité des poissons, mollusques et crustacés aux spécifications d’achat devrait être contrôlée régulièrement.
• il faudrait vérifier à la réception qu’il n’y a pas décomposition ou altération des produits. Les produits présentant des signes de décomposition devrait être refusés.
18.1.1 Réception des produits réfrigérés pour la vente au détail
Dangers potentiels: |
Développement de pathogènes, pathogènes microbiologiques, contamination chimique et physique, formation de scombrotoxines, formation de C. botulinum | |
Défauts potentiels: |
altération (décomposition), contaminants, impuretés | |
Conseils techniques: |
||
• la température des produits devrait être relevée à différents endroits de la livraison et enregistrée. Les poissons, mollusques et crustacées et leurs produits réfrigérés devraient être maintenus à une température égale ou inférieure à 4°C (40°F). Les produits MAP, s’ils ne sont pas congelés, devraient être conservés à une température égale ou inférieure à 3°C (28°F).
18.1.2 Réception des produits congelés pour la vente au détail
Dangers potentiels: |
Peu probables |
Défauts potentiels: |
Décongélation, contaminants, impuretés |
Conseils techniques: |
|
• il faudrait vérifier à la réception que les produits ne présentent pas de signes de décongélation, d’impuretés ou de contamination. Les livraisons douteuses devraient être refusées.
• la température interne des produits devrait être vérifiée, relevée et enregistrée en plusieurs points de la livraison. Les poissons, mollusques et crustacées et leurs produits congelés devraient être conservés à une température égale ou inférieure à -18°C (0°F) et rejetés lorsque la température interne excède 0°C (32°F).
18.1.3 Entreposage frigorifique des produits pour la vente au détail
Dangers potentiels: |
Formation de scombrotoxines, pathogènes microbiologiques, croissance de pathogène, contamination chimique, formation de C. botulinum |
Défauts potentiels: |
Décomposition, contaminants, impuretés |
Conseils techniques: |
|
• les produits en entreposage frigorifique devraient être maintenus à 4°C (40°F). Les produits MAP devraient être conservés à 3°C (28°F) ou moins.
• les poissons et fruits de mer devraient être protégés correctement des impuretés et autres contaminants par un emballage adéquat et être entreposés au-dessus du plancher.
• il est recommandé d’enregistrer en permanence les températures des installations de réfrigération pour les poissons et fruits de mer.
• la chambre frigorifique devrait être dotée d’un système d’écoulement approprié afin d’éviter la contamination des produits.
• les articles prêts à consommer et les mollusques devraient être séparés les uns des autres ainsi que des autres aliments crus dans les entrepôts frigorifiques. Les produits crus devraient être placés sur des étagères en dessous des produits cuits afin d’éviter la contamination croisée par égouttage.
• un système de rotation devrait être établi afin de garantir que les produits sont utilisés selon le principe « premier entré, premier sorti ».
18.1.4 Entreposage en congélateur des produits pour la vente au détail
Dangers potentiels: |
Peu probables |
Défauts potentiels: |
décomposition chimique (rancissement), déshydratation |
Conseils techniques: |
|
• les produits devraient être maintenus à une température de -18°C (0°F) ou moins. Il faudrait contrôler les températures régulièrement. Il est recommandé d’utiliser un thermomètre enregistreur.
• les poissons et fruits de mer ne devraient pas être entreposés directement sur le fond du congélateur. Les produits devraient être rangés de manière à ce que l’air puisse circuler convenablement.
18.1.5 Préparation et emballage des produits réfrigérés pour la vente au détail
Voir Section 8.2.3, « Étiquetage ».
Dangers potentiels: |
Pathogènes microbiologiques, formation de scombrotoxines, développement de pathogènes, contamination physique et chimique, allergènes |
Défauts potentiels: |
Décomposition, étiquetage défectueux |
Conseils techniques: |
|
• les produits devraient être manipulés et emballés conformément aux directives de la Section 3, Programmes de conditions préalables.
• l’étiquetage devrait être effectué conformément aux directives de la Section 3, Programmes de conditions préalables et aux normes Codex d’étiquetage notamment en ce qui concerne les allergènes connus.
• les produits ne devraient pas être soumis à des conditions de température inappropriées pendant l’emballage et la manipulation.
• il faudrait éviter la contamination croisée entre les mollusques et crustacés prêts à consommer et crus, et leurs produits dans l’espace de travail, ou du fait des ustensiles ou du personnel.
[NOTE: une nouvelle section est nécessaire pour l’étiquetage des produits vendus en vrac sur les étals de poisson etc.]
18.1.6 Préparation et emballage des produits congelés pour la vente au détail
voir Section 8.2.3, « Étiquetage ».
Dangers potentiels: |
Pathogènes microbiologiques, contamination physique et chimique, allergènes |
Défauts potentiels: |
Décongélation, étiquetage erroné |
Conseils techniques: |
|
• il faudrait s’assurer que les allergènes sont indiqués, conformément aux prescriptions de la Section 3, Programmes de conditions préalables et des normes Codex d’étiquetage.
• la contamination croisée devrait être évitée entre les produits prêts à consommer et les produits crus.
• les poissons, mollusques et crustacés congelés ne devraient pas être exposés aux températures ambiantes pendant un laps de temps prolongé.
18.1.7 Présentation des produits réfrigérés pour la vente au détail
Dangers potentiels: |
Formation de scombrotoxines, développement microbien, contamination par des pathogènes microbiologique, formation de C. botulinum. |
Défauts potentiels: |
Décomposition, déshydratation |
Conseils techniques: |
|
• les produits en étalage réfrigéré devraient être maintenus à une température de 4°C (40°F) ou moins. La température des produits devrait être relevée à intervalles réguliers.
• les articles prêts à consommer et les mollusques devraient être séparés les uns des autres et des autres produits alimentaires crus dans un étalage réfrigéré de points de vente à service complet. Il est recommandé d’établir un graphique de l’étalage afin de garantir qu’il n’y a pas de contamination croisée.
• en cas d’utilisation de glace, il faudrait installer un système d’égouttage de la glace fondue. Les étalages pour la vente au détail devraient être munis d’un système d’égouttage automatique. Remplacer la glace tous les jours et vérifier que les produits prêts à consommer ne sont pas placés sur de la glace ayant déjà servi pour des produits crus.
• dans les points de vente au détail à service complet chaque produit devrait être présenté dans son propre récipient et servi avec ses propres ustensiles afin d’éviter la contamination croisée.
• il faudrait aussi éviter de présenter les produits en quantité ou en épaisseur telles qu’il devienne impossible d’assurer une réfrigération correcte et de garantir la qualité du produit.
• dans les points de vente au détail à service complet, il faudrait éviter que les produits non protégés ne se dessèchent. Il est recommandé d’utiliser à cet effet un atomiseur dans de bonnes conditions d’hygiène.
• les produits ne devraient pas dépasser la ligne de chargement au-dessus de laquelle il n’est pas possible de maintenir une réfrigération appropriée des produits emballés présentés en étalage à self-service.
• les produits ne devraient pas être soumis à la température ambiante pendant un laps de temps prolongé lors du remplissage des meubles d’étalage.
18.1.8 Présentation des produits congelés pour la vente au détail
Dangers potentiels: |
Peu probables |
Défauts potentiels: |
Décongélation, déshydratation (brûlure de congélation) |
Conseils techniques: |
|
• les produits devraient être maintenus à une température de -18°C (0°F) ou moins. Il est recommandé de surveiller régulièrement la température et d’utiliser à cet effet un thermomètre enregistreur.
• Les produits ne devraient pas dépasser la ligne de chargement dans les meubles d’étalage à self-service. Les congélateurs verticaux où sont présentés les produits devraient être munis de portes automatiques ou de rideaux d’air pour préserver la congélation.
• les produits ne devraient pas être soumis à la température ambiante pendant un laps de temps prolongé lors du remplissage des meubles d’étalage.
• un système de rotation devrait être établi afin de garantir que les poissons, mollusques et crustacés congelés sont utilisés selon le principe « premier entré, premier sorti ».
• les meubles d’étalage pour la vente au détail des poissons, mollusques et crustacés congelés devraient être examinés périodiquement afin de vérifier l’intégrité des emballages et le niveau de déshydratation ou brûlure de congélation.
APPENDICE I
IL EST INDISPENSABLE DE CONTRÔLER L’EFFICACITÉ DES PROCÉDÉS DURANT LE CONDITIONNEMENT DES FILETS DE POISSON ET PRODUITS ANALOGUES SOUS ATMOSPHÈRE MODIFIÉE
Le conditionnement sous atmosphère modifiée (MAP), dans lequel la composition de l’atmosphère entourant les filets est différente de la composition normale de l’air, peut être une technique efficace pour retarder la détérioration d’origine microbienne et le rancissement par oxydation des poissons.
Pour le poisson blanc, on recommande des mélanges de gaz contenant 35-45 % de CO2, 25-35 % d’O2 et 25-35 % de N2. Pour le poisson à chair grasse, on recommande des mélanges de gaz contenant jusqu’à 60 % de CO2 en combinaison seulement avec N2. Il est nécessaire d’incorporer du CO2 pour inhiber les bactéries aérobies communes de détérioration telles que les espèces Pseudomonas ou Acinetobacter/Moraxella. Toutefois, pour les filets ou produits analogues emballés au détail, une proportion trop grande de CO2 dans le mélange de gaz peut provoquer un affaissement de l’emballage, un suintement excessif ou une décoloration. D’autres gaz, N2 et O2, sont incorporés comme diluants pour empêcher ces effets. On évite d’utiliser O2 pour les poissons à chair grasse dans les emballages sous atmosphère modifiée de manière à inhiber le rancissement par oxydation. On recommande en général un rapport gaz/produit de 3:1. Toute réduction de ce rapport risque de diminuer la durée de conservation du produit.
La mesure dans laquelle la conservation du produit peut être prolongée par la procédure MAP dépendra de l’espèce, de la teneur en graisses, de la charge bactérienne initiale, du mélange de gaz, du type de matériau d’emballage et, principalement, de la température d’entreposage. Il incombera à une personne qualifiée, par exemple un technologue des aliments ou un microbiologiste, de déterminer la durée de conservation d’un produit particulier. Étant donné que les poissons peuvent être contaminés par Clostridium botulinum du type E, il faudra veiller attentivement à déterminer la durée de conservation. Bien que l’on reconnaisse généralement que Clostridium botulinum ne se développe pas à des températures inférieures à +3° C, d’autres facteurs, par exemple la teneur en sel ou le pH, etc., peuvent aussi avoir un effet inhibiteur. Ainsi, lorsqu’on détermine la durée de conservation du poisson frais conditionné sous atmosphère modifiée, il est conseillé de procéder à des tests de provocation qui renseigneront fidèlement sur l’état du produit et les conditions d’entreposage et de distribution. Il est très important de noter que l’incorporation de O2 n’empêche pas le développement de Clostridium botulinum du type E et que le contrôle de la température pendant toute la durée de conservation du produit est essentiel. Dans de nombreux cas, au lieu d’utiliser de la glace pour refroidir les paquets, il sera préférable d’opter pour des méthodes de réfrigération mécanique.
L’intégrité de la fermeture des emballages sous atmosphère modifiée est un point critique pour la maîtrise puisqu’il détermine si ces emballages sont sensibles à la contamination microbienne externe et à la déperdition dans l’air du mélange de gaz. Les contrôles indispensables de la soudure thermique devraient porter sur l’alignement correct des griffes et des mâchoires de fermeture, le temps de maintien, la température, la pression et la vitesse de la machine. Il faudrait faire en sorte que la zone de soudure ne soit pas contaminée par le produit, le suintement du produit ou l’humidité, car l’intégrité de la fermeture pourrait être réduite. En outre, la qualité du film utilisé est importante, particulièrement pour ce qui concerne la perméabilité du gaz, et seul un film accompagné d’une spécification clairement définie par des fabricants agréés devrait être utilisé.
Il est indispensable de maintenir le mélange correct de gaz injecté dans les emballages sous atmosphère modifiée pour assurer la qualité, la bonne présentation et la prolongation de la conservation du produit. On procédera donc régulièrement à des analyses des gaz présents dans les emballages sous atmosphère modifiée, dans le cadre du contrôle du processus. Cette analyse des gaz peut révéler des défauts dans l’intégrité des soudures, les matériaux de conditionnement, les machines ou le mélange des gaz avant l’injection. L’emploi d’analyseurs de gaz continus est recommandé. Une analyse des gaz immédiatement après le conditionnement est nécessaire car l’absorption de CO2 est rapide.
APPENDICE II - PRESCRIPTIONS FACULTATIVES CONCERNANT LE PRODUIT FINI - MOLLUSQUES [À TERMINER]
APPENDICE III
PRESCRIPTIONS FACULTATIVES CONCERNANT LE PRODUIT FINI3 - POISSON FRAIS, CONGELÉ OU HACHÉ
Ces prescriptions concernant le produit fini décrivent les défauts potentiels pour le poisson surgelé. La description des défauts potentiels aidera acheteurs et vendeurs à formuler les dispositions relatives aux défauts, qui sont souvent prises en compte lors des transactions commerciales ou de l’élaboration de spécifications pour les produits finis.
Les définitions suivantes sont des recommandations à l’usage des acheteurs et des vendeurs de poisson surgelé qui serviront à élaborer des spécifications concernant les produits finis. Ces spécifications sont facultatives et viennent s’ajouter aux prescriptions essentielles énoncées dans les différentes normes Codex sur les produits et peuvent être appliquées de manière appropriée pour les achats ou les ventes de poisson frais.
1.1 Poisson surgelé, non éviscéré ou éviscéré
Défauts |
Description recommandée des défauts |
a) Déformation corporelle |
Déformation du dos (bosse) ou de la tête si elle n’a pas été enlevée (museau crochu), due à l’apparition dans ces zones de tissu cartilagineux lorsque le poisson approche la période du frai. |
b) Détérioration du revêtement protecteur |
Zones vides dans la pellicule du givre ou déchirures de la membrane protectrice. |
c) Défauts superficiels: Défauts de coloration provenant de meurtrissures
|
Défauts de coloration localisés, faciles à discerner, causés par un épanchement sanguin dans la chair du poisson.
|
d) Défauts d’éviscération et de parage
|
Lavage insuffisant.
|
1.2 Filets de poisson surgelés4
Défauts |
Description recommandée des défauts |
a) Déshydratation modérée |
Déperdition d’eau à la surface du bloc qui masque la couleur mais ne pénètre pas la surface et peut être facilement éliminée par grattage. a) unités <200 g > 25 cm2 |
b) Filets écorchés et déchirés |
Tranches longitudinales notablement et excessivement irrégulières. |
c) Petits morceaux |
Morceau de filet pesant moins de 25 g. |
d) Peau et membrane noire (ne concerne pas la membrane sous-cutanée). Dans le cas du poisson plat, la membrane blanche n’est pas considérée comme un défaut. |
Filets sans peau.
|
e) Membrane noire ou paroi abdominale (ne comprend pas la membrane blanche) |
Filets avec peau.
|
f) Écailles: attachées à la peau |
Filets avec peau - écaillés |
Écailles libres et facilement repérables |
Filets sans peau |
g) Caillots de sang (taches) |
Tout grumeau ou masse de sang de plus de 5 mm de diamètre. |
h) Meurtrissures |
Sang diffus causant des zones manifestement décolorées de couleur rougeâtre, brunâtre ou grisâtre. Chaque zone compacte décolorée ou meurtrie dépassant 3 cm2. |
i) Nageoires ou fragments de nageoires |
Rayons extérieurs ou intérieurs de nageoires, réunies en amas de deux ou plus par une membrane. |
j) Arêtes |
Toute arête d’une longueur égale ou supérieure à 10 mm et de diamètre égal ou supérieur à 1 mm; une arête d’une longueur égale ou supérieure à 5 mm n’est pas considérée comme un défaut si son diamètre ne dépasse pas 2 mm. Le pied de l’arête (extrémité où celle-ci est attachée à une vertèbre) n’est pas pris en considération si son épaisseur est inférieure à 2 mm où s’il peut être facilement enlevé avec l’ongle. |
Défaut « arête » |
Toute arête dont le profil maximum ne peut pas s’insérer dans un rectangle tracé sur une superficie plane solide de 40 mm sur 10 mm. |
k) Matériau d’emballage
|
Chaque cas.
|
1.3 Blocs surgelés de filets de poisson, de chair de poisson hachée et de mélanges de filets et de chair de poisson hachée
Défauts |
Description recommandée des défauts |
a) Irrégularité des blocs (ne s’applique qu’aux blocs destinés à être découpés en bâtonnets ou portions de poisson) |
Non-respect des dimensions déclarées (par exemple, longueur, largeur et épaisseur d’un bloc), manque d’uniformité de forme, angles émoussés, bords déchiquetés, poches de glace, poches d’air ou autre défectuosité pouvant entraîner une perte de produit.
|
b) Poches de glace |
Chaque poche de glace d’une superficie supérieure à 10 cm2. |
c) Poches d’air |
Chaque poche d’air d’une superficie supérieure à 2 cm2 et d’une profondeur supérieure à 3 mm |
d) Déshydratation modérée |
Déperdition d’humidité à la surface de l’échantillon masquant la couleur, mais qui n’a pas pénétré la superficie et qui peut être facilement enlevée par grattage.
Dimensions des paquets Superficie défectueuse
|
e) Peau et membrane noire (ne comprend pas la membrane sous-cutanée). Dans le cas des poissons plats, la peau blanche n’est pas considérée comme une défectuosité. |
Blocs de filets sans peau
|
f) Membrane noire ou paroi abdominale (ne comprend pas la membrane blanche) |
Blocs de filets avec peau
|
g) Écailles attachées à la peau |
Blocs de filets avec peau (écaillés)
|
Écailles (détachées facilement repérables) |
Blocs de filets sans peau
|
h) Caillots (taches) de sang |
Tout grumeau ou masse de sang coagulé. |
i) Meurtrissures et décoloration |
Présence de sang provoquant une tache nettement visible de couleur rougeâtre, brunâtre ou grisâtre indiquant un défaut de coloration important dû à des dépôts de mélanine, des taches de bile, taches de foie ou d’autres causes.
|
Fraction de hachis des blocs mélangés: |
Défaut de coloration déplaisant, taches ou particules provenant de peau, membrane noire, caillots de sang, moelle épinière ou viscères.
|
j) Nageoires ou fragments de nageoires |
Deux ou plusieurs rayons reliés par une membrane, y compris les arêtes internes ou externes, ou les deux, constituant un paquet.
|
k) Arêtes |
Toute arête dont la longueur est égale ou supérieure à 10 mm ou dont le diamètre est égal ou supérieur à 1 mm; une arête dont la longueur est égale ou supérieure à 5 mm n’est pas considérée comme un défaut si son diamètre ne dépasse pas 2 mm. La partie initiale d’une arête (par laquelle elle tenait à une vertèbre) n’est pas prise en considération si sa largeur ne dépasse pas 2 mm ou s’il est possible de l’extraire facilement avec l’ongle. |
Défaut « arête» |
Toute arête dont le profil maximum ne peut pas s’insérer dans un rectangle tracé sur une surface plane et solide de 40 mm de long et 10 mm de large. |
l) Viscères |
Chaque cas. |
m) Matériau d’emballage |
Chaque cas. |
APPENDICE IV
PRESCRIPTIONS FACULTATIVES CONCERNANT LE PRODUIT FINI - SURIMI CONGELÉ
Ces prescriptions concernant le produit fini décrivent les défauts potentiels pour le surimi congelé. La description des défauts potentiels aidera acheteurs et vendeurs à formuler les dispositions relatives aux défauts qui sont souvent prises en compte lors des transactions commerciales ou de l’élaboration des spécifications pour les produits finis.
Le surimi congelé est un concentré de protéines myofibrillaires à base de chair de poisson, mais qui ne conserve pas la forme originale du poisson, de sorte qu’il est difficile de déterminer sa qualité en se fondant sur son aspect. De plus, en général, il n’est pas consommé directement, mais est soumis à un traitement ultérieur. Cela signifie que la qualité du surimi congelé est évaluée à la fois par les propriétés de composition et les propriétés fonctionnelles pour les produits à base de surimi. Il est donc vivement recommandé d’examiner ces propriétés fonctionnelles, comme les attributs de qualité ci-après, qui sont différents de ceux des autres produits de la pêche.
Il est très important d’évaluer les attributs primaires suivants: teneur en eau, pH et matières indésirables de surimi cru et force du gel, aptitude au formage et couleur du gel de surimi cuit. D’autres attributs secondaires pourront aussi être évalués à volonté.
1. Attributs primaires de qualité
1.1 Essais sur surimi cru
Préparation de l’échantillon pour essai:
Mettre dans un sac en polyéthylène 2 à 10 kg de surimi congelé, fermer le sac et faire décongeler partiellement à température ambiante (20°C) ou moins de manière que la température du surimi atteigne approximativement -5°C. Ne pas presser la surface de l’échantillon pour la ramollir.
1.1.1 Teneur en eau
Il faudrait prélever l’échantillon à l’intérieur d’un bloc de surimi pour s’assurer qu’il ne subira pas de brûlure de congélation (dessiccation de la surface). Placer cet échantillon dans un sac ou une bouteille de polyéthylène, fermer le sac ou la bouteille et laisser décongeler partiellement jusqu’à ce que la température du produit atteigne la température ambiante. Mesurer la teneur en eau à l’aide de l’une des méthodes suivantes:
Si l’on utilise un four de séchage, se reporter à la méthode AOAC;
Si l’on utilise un doseur d’humidité à lampe à infrarouge, prendre 5 g de l’échantillon pour essai pesé précisément sur un plateau de balance pour échantillon, et faire sécher immédiatement [les détails de la méthode seront fournis ultérieurement]; ou
Si l’on utilise un doseur d’humidité avec séchage par micro-ondes, se reporter à la méthode AOAC [des détails d’une méthode de remplacement seront fournis ultérieurement].
Calculer la teneur en eau suivant la formule suivante à une décimale près.
En utilisant l’une quelconque des méthodes de mesure, faire un essai sur deux morceaux au moins de l’échantillon et indiquer la valeur moyenne obtenue.
Quand on mesure un échantillon gras avec un doseur d’humidité avec séchage par micro-ondes, il faut couvrir le plateau contenant l’échantillon avec de la fibre de verre pour que la graisse n’éclabousse pas, pendant le séchage.
Teneur en eau (%) = poids avant séchage (g) - poids après séchage (g)
poids avant séchage
1.1.2 pH
Ajouter 90 ou 190 ml, selon les besoins, pour diluer l’échantillon d’eau distillée à 10 g de l’échantillon pour essai. Homogénéiser le mélange et mesurer le pH de la suspension à l’aide d’un pH mètre à électrode de verre à deux décimales près. Indiquer la valeur ainsi obtenue.
1.1.3 Matières indésirables
L’expression « matières indésirables » telle qu’on l’emploie ici signifie de la peau, des petites arêtes et toute matière indésirable autre que la chair de poisson.
Étaler 10 g de l’échantillon pour essai sur une épaisseur de 1 mm ou moins, et compter les matières indésirables visibles s’y trouvant. Indiquer la valeur ainsi obtenue, en tenant compte du fait qu’une matière indésirable de 2 mm ou plus devra être comptée pour une et qu’une matière indésirable de moins de 2 mm sera comptée pour une demie, respectivement, et que toute matière indésirable de moins de 1 mm sera ignorée.
La méthode d’inspection pour distinguer les écailles invisibles à l’œil nu est décrite à la section 2.1.1 de la présente Annexe.
1.2 Essais sur le gel de surimi cuit
1.2.1 Force du gel et aptitude au formage
On présente ici deux méthodes. L’acheteur et le vendeur décideront de concert quel essai effectuer.
1.2.1.1 Essai de résistance à la pénétration
Préparation de l’échantillon:
Mettre dans un sac de polyéthylène 2 à 10 kg de surimi congelé, fermer le sac et faire décongeler partiellement à température ambiante (20° C) ou moins de manière que la température du surimi atteigne approximativement - 5° C. Ne pas presser la surface de l’échantillon pour la ramollir.
Préparation du gel de surimi pour les essais. Gel de surimi non additionné d’amidon
A. Pulvérisation
La quantité de produit à prélever sur l’échantillon pour préparer la pâte de surimi dépend de la capacité du mélangeur utilisé. Il faut prendre au moins 1,5 kg du produit pour représenter la propriété d’un bloc de 10 kg. Compte tenu du fait qu’il faut disposer d’une quantité suffisante de surimi pour assurer la cohérence de l’essai, un appareil de grande capacité pouvant mélanger 1,5 kg de surimi ou plus doit être installé dans le laboratoire. Si l’appareil a de plus grandes dimensions, il faut augmenter la quantité de surimi de manière à obtenir une pâte de bonne texture. Écraser 1,5 kg ou plus de l’échantillon avec un couteau rotatif, ajouter 3 % de sel, et broyer encore et pétrir pendant 10 minutes ou plus jusqu’à obtention d’une pâte homogène. Ne pas oublier de maintenir la température du matériau à l’essai à 10° C ou moins.
Le bon moment pour ajouter le sel est lorsque la température est de -1,5°C.
La température idéale du matériau d’essai est de 5-8° C.
B. Remplissage
Remplir un tube en plastique PVDC de 48 mm de largeur (30 mm de diamètre) quand il est aplati, avec environ 150 g (il aura alors à peu près 20 cm de long) de pâte de chair en utilisant un poussoir muni d’un tube de 18 mm de diamètre, et nouer les deux extrémités du tube.
C. Traitement thermique
Chauffer le matériau d’essai dans de l’eau chaude à 84-90° C pendant 30 minutes.
Au moment où le matériau d’essai est mis dans l’eau, la chute de température ne devrait pas dépasser 3°C.
D. Refroidissement
Tout de suite après le traitement thermique, placer le matériau d’essai dans de l’eau froide et le faire refroidir complètement, puis laisser à température ambiante pendant au moins 3 heures.
Méthode d’essai
Attendre 24 - 48 heures après la cuisson, puis prendre les mesures suivantes de l’échantillon de gel de surimi préparé pour l’inspection; sa température devrait être égale à la température ambiante et noter la température de l’échantillon au moment de la mesure.
Mesurer la force du gel et l’aptitude au formage de l’échantillon de gel de surimi inspectée avec un rhéomètre. Utiliser un plongeur sphérique de 5 mm de diamètre et régler la vitesse sur 60 mm/minute.
Enlever le film de l’échantillon de gel de surimi à inspecter et couper pour obtenir un spécimen d’essai de 25 mm de long et placer ce spécimen sur le plateau de l’appareil de manière que le centre du spécimen à essayer se trouvera juste au-dessous du plongeur. Pousser sur le plongeur et mesurer la force de pénétration en g et la capacité de formage en mm à la rupture.
Consigner la valeur obtenue de la pénétration et de l’aptitude au formage en grammes, en nombre entier. Enregistrer la valeur de la déformation en mm à une décimale près.
Préparer six spécimens d’essai ou plus à partir de l’échantillon d’inspection du gel de surimi et soumettre chacun à un essai. Enregistrer les valeurs moyennes ainsi obtenues.
1.2.1.2 Essai de torsion
Préparation de spécimens d’essai de gel de surimi
A. Pulvérisation
Laisser décongeler partiellement le surimi à température ambiante (environ 25° C) pendant 1 heure, ou dans une pièce de remise en température réfrigérée à environ -5°C. Découper les blocs de surimi partiellement décongelé en tranches ou en gros morceaux et les mettre dans un récipient muni d’un mélangeur-cutter pouvant être utilisé sous vide. Réduire d’abord le surimi en une poudre en le pulvérisant à petite vitesse sans vide. Ajouter du chlorure de sodium (2 % sur la base du poids total du lot) et de la glace/eau (de façon à obtenir une teneur en eau finale de 78 % sur la base du poids total du lot). Placer le couvercle et recommencer à broyer à petite vitesse sans vide, passant peu à peu (si possible) à grande vitesse (environ 2 000 tours/minute). Lorsque le mélange commence à former une masse homogène, arrêter la pompe à vide et laisser un vide d’environ 70/80 % du vide total (environ 20-25 pouces Hg ou 500-650 mm Hg). Durant le broyage, il faut faire en sorte que la pâte se détache bien des parois et que les boulettes de pâte passent bien entre les lames du mélangeur/cutter. Arrêter de broyer quand la température atteint 5-8° C. On recommande de broyer pendant au moins 6 minutes.
B. Remplissage
Transférer la pâte dans l’embosseuse en incorporant le moins d’air possible. Maintenir constamment la température de la pâte au-dessous de 10° C. Remplir des tubes de polycarbonate ou en acier inoxydable de 1,9 cm d’une longueur appropriée, en général environ 20 cm. Avant de remplir les tubes, il faudrait les pulvériser d’un agent de démoulage à base de lécithine. Remplir uniformément de pâte le tube sans laisser de poches d’air. Capsuler ou fermer les deux extrémités et placer dans un bain de glace jusqu’à ce que le produit soit près pour être chauffé (une heure).
C. Traitement thermique
Le traitement thermique se fait par immersion des tubes remplis dans un bain d’eau à la température voulue. Le rapport durée-température pour le traitement thermique est le suivant: capacité de prise à basse température: 0-4° C pendant 12-18 heures, puis à 90° C pendant 15 min; capacité de prise à moyenne température: 25° C pendant 3 heures, puis immédiatement à 90° C pendant 15 min; capacité de prise à température élevée: 40° C pendant 30 minutes, puis immédiatement à 90° C pendant 15 min; évaluation de l’activité protéasique: 60° C pendant 30 minutes, puis immédiatement à 90° C pendant 15 min; effet de cuisson rapide: 90° C pendant 15 minutes. Il est recommandé de chauffer l’eau des bains jusqu’à ce que leur température dépasse d’environ 5° C celle fixée pour le traitement, afin de prendre en compte la perte de chaleur pendant le chargement; la température doit être réglée en 2 minutes à peu près, parfois en ajoutant de la glace.
Seules les espèces d’eau froide afficheront une bonne capacité de prise à basse température. Il faudrait spécifier le traitement thermique utilisé pour préparer les échantillons; sinon on suppose que seul l’effet de cuisson rapide est évalué. L’activité protéolytique relative sera évaluée en comparant des essais menés sur des gels préparés à 60/90° C avec ceux traités seulement à 90° C.
Le chauffage ohmique peut être utilisé pour le traitement thermique. La chaleur est produite uniformément par une résistance électrique. La pâte mise dans un tube en PVC-C est chauffée entre deux électrodes. La température interne de 90° C peut être atteinte en 1 min. La vitesse d’échauffement (rapide et lente) peut être contrôlée de façon linéaire. Cette méthode offre un autre avantage: le surimi de merlan du Pacifique ou d’autres poissons contenant des enzymes protéolytiques peut être gelé avec succès (sans utiliser d’inhibiteurs d’enzymes) sous chauffage ohmique car l’échauffement rapide peut inactiver l’enzyme.
D. Refroidissement
Après le traitement thermique, transférer rapidement les tubes dans un bain d’eau glacée et porter à 0° C. Retirer les gels des tubes à l’aide d’un plongeur et fermer dans des sacs de plastique. Conserver les échantillons réfrigérés jusqu’au moment des essais (dans les 48 heures).
Méthode d’essai
Prendre dans les 24 heures les mesures suivantes de l’échantillon de gel de surimi préparé pour l’inspection, qui sera porté à température ambiante (20-25° C).
Mesure de la tension/contrainte:
La capacité gélifiante du surimi est mise en évidence par les propriétés rhéologiques du produit à tester lorsqu’il est soumis à une contrainte jusqu’à se briser (rupture). Porter les échantillons réfrigérés à température ambiante (près de 25° C) avant l’essai. Préparer des spécimens d’environ 30 mm de long. Attacher les spécimens sur des disques mobiles à chaque extrémité plate avec du cyanoacrylate, en veillant à placer les échantillons au centre des disques. Donner aux spécimens la forme d’un cabestan, la partie travaillée ayant un centimètre de diamètre. Placer le spécimen d’essai dans le rhéomètre de torsion. Tourner le sommet de l’échantillon au point de rupture de l’échantillon et enregistrer les moments de torsion et la distance de rotation à ce point. Calculer et consigner les valeurs relatives à la tension et la contrainte au point de rupture de l’échantillon comme suit: tension = t = 1581 x (unités de torsion); contrainte = ln [1+(g2/2) + g(1+g2/4)0.5], où g = 0,150 x (distance de rotation, mm) – 0,00847 x (unités de torsion). Dans la pratique, ces équations sont normalement programmées dans un ordinateur relié à un rhéomètre de torsion pour l’obtention et l’analyse de données, fournissant ainsi directement les mesures de la tension/contrainte.
1.2.2 Couleur
Couper l’échantillon de gel de surimi à inspecter en tranches plates et lisses de 15 mm d’épaisseur ou plus, et mesurer immédiatement avec un spectrocolorimètre la section transversale des tranches dans les valeurs de L*(clarté), a* (rouge-vert) et b* (jaune-bleu) à une décimale près. Faire l’essai sur trois tranches au minimum, et indiquer les moyennes des valeurs ainsi obtenues.
2. Attributs secondaires de qualité
2.1 Essais sur surimi cru
Préparation de l’échantillon pour essai:
Mettre dans un sac de polyéthylène 2 à 10 kg de surimi congelé, fermer le sac et faire décongeler partiellement à température ambiante (20° C) ou moins de manière que la température du surimi atteigne environ -5°C. Ne pas presser la surface de l’échantillon pour la ramollir.
2.1.1 Matières indésirables (écailles)
Après les mesures prises selon les indications données au point 1.1.3 de la présente annexe, ajouter 100 ml d’eau au même échantillon pour essai, homogénéiser et ajouter 100 ml de solution 0.2M-NaOH, et mélanger avec un agitateur. Filtrer la solution dissoute avec un papier filtre (N° 2), laver le résidu à l’eau puis faire sécher à 105 pendant deux heures. Compter les écailles ainsi obtenues, et indiquer entre parenthèses leur nombre après celui des matières indésirables conformément à la section 1.1.3.
Après l’avoir dissoute, laisser reposer la solution pour assurer la précipitation, et écumer autant que possible avant de filtrer.
2.1.2 Teneur en protéines brutes
Méthode Kjeldahl (AOAC)
2.1.3 Teneur en sucre
Peser précisément 10 g de l’échantillon pour essai, mettre dans un vase à bec de 50 ml, ajouter 10 ml d’une solution d’acide trichloracétique (TCA) à 2 %, et bien mélanger. Laisser reposer pendant environ 10 minutes, mélanger de nouveau, et laisser reposer encore pendant 10 minutes. Filtrer avec du papier filtre (N° 2), verser une petite partie du liquide filtré sur un réfractomètre (pour utilisation Brix 0-10 %), et lire l’indice sur le réfractomètre. Appliquer à la formule suivante et calculer la valeur à une décimale près. Indiquer la valeur ainsi obtenue.
Étalonner à l’avance le réfractomètre à une température spécifiée avec de l’eau distillée.
Sucre (%)=2,04 x Brix (%) - 2,98
2.1.4 Teneur en graisse brute
Mettre dans un mortier 5 à 10 g de l’échantillon pour essai avec à peu près la même quantité de sulfate de sodium anhydre et une petite quantité de sable marin raffiné. Écraser uniformément le matériau en une poudre sèche et placer dans un papier filtre en forme de cylindre. Prendre bien soin de recueillir toute la poudre restant au fond du mortier à l’aide de coton hydrophile imbibé d’éther et la mettre dans le cylindre. Extraire et déterminer les graisses selon la méthode Soxhlet, et calculer la valeur selon la formule suivante à une décimale près. Indiquer la valeur ainsi obtenue.
Boucher les extrémités du cylindre en papier filtre avec un petit morceau de coton hydrophile de sorte que le matériau ne puisse sortir du cylindre.
Faire sécher à l’avance le récipient d’extraction à 100 - 106° C, et le peser.
La vitesse d’extraction sera 20 fois/heure.
(W1 - W0)
graisse brute (%) = S X 100
S = Quantité de l’échantillon prélevée (g)
W0 = Poids du récipient (g)
W1= Poids du récipient après extraction des graisses (g)
2.1.5 Couleur et blancheur
Couleur: Laisser décongeler le surimi congelé à température ambiante (environ 25° C). Verser dans un vase de verre à bec de 50 ml (4 cm de diamètre, 5,5 cm de hauteur) et mesurer les valeurs des couleurs de L*, a*, et b* (système du laboratoire CIE) à une décimale près. Pour obtenir des résultats fiables, on recommande un contact complet entre le spécimen d’essai et le bras de mesure du colorimètre, ainsi que le remplissage du vase sans laisser de vide. Mesurer trois ou quatre échantillons et consigner les valeurs obtenues.
Blancheur: la blancheur peut être calculée comme suit: blancheur = L* - 3b* ou blancheur = 100 - [(100 - L*)2 + a*2 + b*2]0.5.
2.1.6 Égouttage par pression
Décongeler 50 g de l’échantillon pour essai et le mettre dans un cylindre dont le diamètre intérieur est de 35 mm et la longueur de 120-150 mm, fait d’acier inoxydable ou de résine synthétique et muni de 21 trous de 1,5 mm de diamètre distants de 3 mm l’un de l’autre, ouvert au sommet. Appliquer immédiatement une charge de 1 kg à l’aide d’un tube cylindrique de pressurisation de 34 mm de diamètre, dont le poids doit être inclus dans la charge. Maintenir pendant 20 minutes, puis mesurer le poids du liquide égoutté. Calculer son pourcentage par rapport au poids de l’échantillon pour essai à une décimale près. Indiquer la valeur ainsi obtenue.
2.2 Essais sur surimi cuit
2.2.1 Préparation de l’échantillon pour essai
2.2.1.1 Gel de surimi additionné d’eau:
A. Pulvérisation
La quantité de produit à prélever sur l’échantillon pour préparer la pâte de surimi dépend de la capacité du mélangeur utilisé. Il faut prendre au moins 1,5 kg de produit pour représenter la propriété d’un bloc de 10 kg. Compte tenu du fait qu’il faut disposer d’une quantité suffisante de surimi pour assurer la cohérence de l’essai, un appareil de grande capacité pouvant mélanger 1,5 kg de surimi ou plus doit être installé dans le laboratoire. Si l’appareil a de plus grandes dimensions, il faut augmenter la quantité de surimi de manière à obtenir une pâte de bonne texture. Écraser 1,5 kg ou plus de l’échantillon avec un couteau rotatif, ajouter 3 % de sel et 20 % de 3 % d’eau salée refroidie, et continuer de broyer et d’écraser pendant 10 minutes ou plus jusqu’à obtention d’une pâte homogène. Toutefois, si vous utilisez ce qui reste de l’échantillon non additionné d’eau et non additionné d’amidon (section 1.2.1.1. A de la présente Annexe), ajouter 20 % de 3 % d’eau salée refroidie seulement, et continuer de broyer et d’écraser pendant 5 minutes jusqu’à obtention d’une pâte homogène, tout en maintenant la température à 10° C ou moins pour les espèces d’eau froide, comme le lieu de l’Alaska (Theragra chalcogramma). Les espèces d’eau chaude peuvent être traitées à une température légèrement plus basse (ne dépassant pas [15°C]). Néanmoins, on obtiendra une meilleure qualité à une température plus basse.
B. Remplissage
Voir Section 1 2.1.1.B de la présente Annexe.
C. Traitement thermique
Voir Section 1.2.1.1.C de la présente Annexe.
D. Refroidissement
Voir Section 1.2.1.1.D de la présente Annexe
2.2.1.2 Gel de surimi additionné d’amidon
A. Pulvérisation
Ajouter 5 % de fécule de pomme de terre à de la pâte de surimi préparée selon la méthode décrite à la Section 1.2.1.1.A de la présente Annexe, et mélanger (homogénéiser) pendant 5 minutes. Il faudrait veiller à maintenir la température du matériau d’essai à 10°C ou moins pendant toute l’opération. La température idéale pour le matériau d’essai est de 7-8°C.
B. Remplissage
Voir Section 1.2.1.1.B de la présente Annexe
C. Traitement thermique
Voir Section 1.2.1.1.C de la présente Annexe. Toutefois, si on effectue le traitement dans le but d’obtenir une prise Suwari, se reporter à la Section 2.2.1.3.C de la présente Annexe sur le gel de surimi traité pour prise Suwari.
D. Refroidissement
Voir Section 1.2.1.1.D de la présente Annexe.
2.2.1.3 Gel de surimi traité pour prise Suwari
A. Pulvérisation
Voir Section 1.2.1.1.A de la présente Annexe.
B. Remplissage
Voir Section 1.2.1.1.B de la présente Annexe.
C. Traitement thermique
Après traitement à l’eau chaude pour obtenir une prise Suwari à 30 (28-32)° C pendant 60 minutes, suivre les indications données pour le traitement thermique à la Section 1.2.1.1.C de la présente Annexe.
D. Refroidissement
Voir Section 1.2.1.1.D de la présente Annexe.
2.2.2 Méthode d’essai
Prendre, 24 à 48 heures après la cuisson, les mesures suivantes de l’échantillon de gel de surimi préparé pour l’inspection dont la température devrait être celle de la pièce et enregistrer la température de l’échantillon au moment de la mesure.
2.2.2.1 Blancheur
La blancheur, comme indice de l’aspect général d’un gel de surimi, peut être calculée comme suit: blancheur = L* - 3b*. ou: blancheur = 100 - [(100 - L*)2 + a*2 + b*2]0.5.
2.2.2.2 Eau à exprimer
Mettre une tranche de gel de surimi (de 2 cm de diamètre x 0,3 cm d’épaisseur et pesant environ 1 g) entre deux papiers filtre et, à l’aide d’un appareil à pression d’huile, exercer une pression fixe (10 kg/cm2) pendant 20 secondes.
Calculer l’eau à exprimer sur la base de la formule suivante à une décimale près.
Répéter l’opération avec au minimum trois morceaux ou plus de l’échantillon pour essai et indiquer la valeur ainsi obtenue.
Poids avant pressage (g)- poids après pressage (g)
Eau à exprimer (%) = Poids avant pressage (g)
La capacité de rétention d’eau est aussi utilisée comme un indice du gel de surimi et comme l’eau à exprimer.
La capacité de rétention d’eau est calculée comme suit:
Teneur en eau à exprimer (g)
Capacité de rétention d’eau (%) = Teneur totale en eau de l’échantillon avant pressage (g)
2.2.2.3 Essai de pliage:
Cet essai est effectué en pliant une tranche de gel de 5 mm d’épaisseur à moitié puis à moitié encore tout en examinant les signes de défauts structurels (craquelures). Assurez-vous que l’échantillon est plié complètement à moitié. Laissez plié pendant cinq secondes puis évaluez le changement dans la forme en attribuant une note d’appréciation suivant une échelle de 1 à 5. Le nombre minimal de fois où il faut plier pour produire une craquelure dans le gel détermine la note pour cet essai. Faire l’essai sur au moins trois autres tranches prélevées sur le même échantillon, et indiquer la note moyenne obtenue. Si l’on effectue le pliage à la main, il faut appliquer constamment la même force sur la surface pliée.
Note d’appréciation Propriété
5 Pas de craquelures même après pliage en quatre.
4 Pas de craquelures après pliage en deux, mais une ou plusieurs craquelures après pliage en quatre.
3 Pas de craquelures après pliage en deux mais fentes après pliage en quatre.
2 Craquelures après pliage en deux.
1 Fente en deux après pliage en deux.
2.2.2.4 Essai organoleptique (effet sous la dent)
Mordre une tranche de 5 mm d’épaisseur prélevée sur l’échantillon de gel et évaluer sa résistance sous la dent et son degré de cohésion par des notes d’appréciation allant de 1 à 10. Un groupe de trois ou quatre experts fera un essai sur trois tranches au moins du même échantillon et indiquera la note moyenne obtenue. Les notes d’appréciation 2, 3, 4, 5 et 6 correspondent aux notes d’appréciation du pliage 1, 2, 3, 4 et 5 sous le point 2), respectivement.
Note d’appréciation « Force Ashi »
10 Extrêmement forte
9 Très forte
8 Forte
7 Légèrement forte
6 Moyenne
5 Légèrement faible
4 Faible
3 Très faible
2 Extrêmement faible
1 Incapable de former un gel
Type de produit |
Défaut |
Description recommandée |
État congelé |
Présence d’excédent d’enrobage détaché |
Une quantité excessive d’enrobage détaché dans le paquet en pourcentage du poids net déclaré |
Matière grasse (huile) en excès |
Huile en quantité perceptible ayant taché l’intérieur et imprégné l’emballage | |
Facilité de séparation |
Lorsqu’on retire du paquet les unités, elles devraient se séparer facilement par une légère pression de la main, sans causer de dommage et sans que le matériau d’emballage n’adhère à la surface, pourcentage des bâtonnets ou des portions affectés. | |
Produits brisés |
Produits brisés, qui ont été séparés en plusieurs morceaux. Chaque cas. | |
Produits endommagés |
Produits endommagés, qui ont été écrasés, aplatis ou autrement abîmés au point que l’aspect s’en trouve sensiblement altéré.
| |
Défauts de coloration de l’enrobage |
Couleur des unités présentant une teinte noire ou brun très foncé Couleur sensiblement différente de celle d’autres unités de l’échantillon Nombreuses taches noires occasionnées par des miettes de pain brûlées | |
Dimensions irrégulières (en cas de déclaration) |
Irrégularité des dimensions des bâtonnets ou portions exprimée en pourcentage du poids | |
Enrobage |
Bâtonnets, portions ou filets de poisson dont la surface n’est pas complètement recouverte par la panure et/ou la pâte à frire | |
Poches de glace (pouvant endommager l’enrobage à la cuisson) |
Poches de glace sur une surface > 1 cm² (chaque cas).
| |
Déshydratation profonde |
Il s’agit d’une perte excessive d’humidité à la surface de l’échantillon qui apparaît de façon visible à la surface et qui ne se laisse pas facilement éliminer par grattage. Chaque cas > 5 cm². | |
État décongelé |
Peau et membranes noires (ne comprend pas la membrane sous-cutanée - paroi argentée) |
Filet sans peau. Chaque fragment > 3 cm². |
Membrane noire ou paroi abdominale (entraîne des dommages à la cuisson) |
Filet avec peau. Chaque fragment de plus de 3 cm² (membrane blanche non comprise). | |
Écailles (attachées à la peau)
|
Filet avec peau - écaillé. Chaque zone couverte d’écailles supérieure à 3 cm².
| |
Caillots (taches) de sang |
Tout grumeau ou masse de sang coagulé. Chaque caillot d’un diamètre supérieur à 5 mm. | |
Meurtrissures et défauts de coloration |
Présence de sang provoquant une tache nettement visible de couleur rougeâtre, brunâtre ou autre défaut de coloration. Ensemble de zones décolorées ou meurtries de plus de 3 cm². | |
Nageoires ou fragments de nageoires |
Deux ou plusieurs rayons reliés par une membrane, y compris les arêtes internes ou externes, ou les deux, constituant un paquet. Chacun des cas où la nageoire contient une arête de plus de 40 mm de long. | |
Viscères |
Toute portion de viscères. Chaque cas. | |
Matériau d’emballage adhérent |
Chaque cas. | |
APPENDICE VI - PRESCRIPTIONS FACULTATIVES CONCERNANT LE PRODUIT FINI – POISSON SALÉ
[À TERMINER]
Ces spécifications concernant le produit fini décrivent les défauts potentiels pour le poisson salé. La description des défauts potentiels aidera acheteurs et vendeurs à formuler les dispositions relatives à ces défauts. Ces prescriptions sont facultatives et viennent s’ajouter aux prescriptions essentielles énoncées dans les différentes normes Codex sur les produits.
1. DÉNOMINATION DES POISSONS SALÉS DE LA FAMILLE DES GADIDAE
Renvoi à la Norme pour les poissons salés et les poissons salés séchés de la famille des Gadidae (Codex Stan. 167-1989, Rév. 1-1995).
Produits obtenus à partir des espèces ci-après, appartenant toutes à la famille des Gadidae qui ont été saignées, éviscérées, étêtées et fendues de sorte qu’environ deux tiers de la colonne vertébrale est enlevé, lavées et présentant une saturation en sel de 90-100 %.
Nom français |
Nom latin |
Morue de l’Atlantique |
Gadus morhua |
Morue du Pacifique |
Gadus macrocephalus |
Morue polaire |
Boreogadus saida |
Morue ogac |
Gadus ogac |
Lieu noir |
Pollachius virens |
Lingue |
Molva molva |
Lingue bleue |
Molva dypterygia |
Brosme |
Brosmius brosme |
Églefin |
Gadus aeglefinus / Melanogrammus aeglefinus |
Catégories de qualité
Impériale/supérieure
Les produits de cette catégorie commerciale sont obtenus à partir de poissons entièrement saignés, bien lavés et rincés afin d’éliminer les restes de sang et d’entrailles, et dont la peau du collet reste attachée.
Le poisson doit être fendu correctement et salé de manière régulière, bien pressé et réempilé pendant la transformation. Le poisson doit être peu coloré et ferme, et ne pas présenter de taches.
Cette catégorie commerciale peut inclure des poissons présentant les caractéristiques suivantes:
1. ventres mal saignés
2. petites déchirures ou fissures longitudinales
3. mal rincés
4. quelques caillots de sang
5. salés de manière pas très régulière
Lors de l’évaluation du poisson de cette catégorie, il faudra examiner en particulier si le poisson a été complètement saigné et réempilé correctement pendant la production. Dans ce cas, des défauts relativement plus importants seront tolérés si l’impression générale le justifie, en particulier si le poisson est peu coloré et ferme.
Universelle
Les poissons qui ne répondent pas aux spécifications de la catégorie Impériale/Supérieure entrent dans la catégorie Universelle.
Cette catégorie commerciale peut inclure des poissons présentant les caractéristiques suivantes:
1. mal fendus
2. queue ronde
3. mal lavés ou rincés
4. élimination insuffisante de la colonne vertébrale
5. caillots de sang en quantité modérée
6. grandes déchirures ou fissures longitudinales
7. fissures modérées
8. taches mineures de sang, foi et/ou de bile
Le poisson doit conserver sa forme naturelle. Les défauts marquants comme par exemple les taches/masses de sang séché ou les restes d’entrailles doivent être supprimés.
Courante
Les poissons ne répondant pas aux critères de la catégorie Universelle mais qui néanmoins sont propres à la consommation humaine doivent être classés comme de qualité Courante. Cette catégorie commerciale ne doit cependant pas contenir de poisson fermenté, ayant été exposé à la contamination, dont le ventre est écorché, contenant de la bile ou des viscères, de poisson présentant d’importantes fissures ou dont la chair se détache, ou encore avec des traces visibles de bactéries halophiles rouges (couleur rose) ou d’importantes moisissures halophiles (moisissures brunes).
2. Dénomination des produits ….
APPENDICE VII PRESCRIPTIONS FACULTATIVES CONCERNANT LE PRODUIT FINI – POISSON FUMé
[À TERMINER]
Les définitions suivantes sont des recommandations à l’usage des acheteurs et des vendeurs de langoustes, homards, cigales de mer et crabes, qui serviront à élaborer des spécifications concernant les produits finis. Ces spécifications sont facultatives et viennent s’ajouter aux prescriptions essentielles énoncées dans la norme Codex sur le produit visé.
1. Langoustes, homards, cigales de mer et crabes surgelés
Les
Défauts |
Description recommandée des défauts |
a) Aspect |
i) non facilement détachable sans décongélation quand il est déclaré surgelé en unités individuelles |
ii) couleur généralement non uniforme et non caractéristique du produit, de l’espèce et de l’habitat ou des zones de capture. | |
iii) dans le cas des produits non décortiqués, la carapace n’est pas ferme ni intacte | |
b) Animaux endommagés |
Telson brisé, coupures ou déchirures pénétrant dans la carapace, carapace écrasée ou fêlée. |
c) Carapace molle |
La carapace fléchit facilement sous la pression des doigts |
La chair crue n’a pas l’aspect translucide caractéristique | |
d) Opacité |
La chair des langoustes, homards et cigales de mer est |
e) Texture |
dure, fibreuse, molle ou gélatineuse. (% affecté en poids) |
A. CREVETTES DECORTIQUÉES ET DÉVEINÉES - CONGELÉES OU SURGELÉES INDIVIDUELLEMENT
FACTEUR DE QUALITÉ
Détermination de la qualité
Pour déterminer la qualité, il faut examiner le produit à l’état congelé, à l’état décongelé et après cuisson, à l’aide du tableau des déductions de points
100 à 90 Première qualité
89 à 80 Deuxième qualité
Saveur: |
Caractéristique, sans saveurs déplaisantes |
À l’état congelé: |
Lorsque la température maximale du produit a atteint - 18°C (0°F) au centre thermique |
Odeur: |
Caractéristique. Une odeur d’iodoforme n’est pas considérée comme un défaut. |
Déshydratation: |
La carapace et/ou la chair des crevettes présentent des zones qui en altèrent gravement l’aspect, la texture et la saveur. |
Texture: |
La texture doit être ferme, mais tendre et humide. |
Légère: assez ferme, seulement légèrement dure ou caoutchouteuse et ne forme pas une masse fibreuse dans la bouche, humide mais non spongieuse. | |
Modérée: modérément dure ou caoutchouteuse, a une tendance perceptible à former une masse fibreuse dans la bouche, humide mais non spongieuse | |
Excessive: excessivement dure ou caoutchouteuse, a une tendance marquée à former une masse fibreuse dans la bouche, ou est très sèche ou très spongieuse. | |
Taches noires: |
La carapace et/ou la chair des crevettes ne devraient pas présenter de taches noires qui en altèrent gravement l’aspect. |
Crevette brisée: |
Crevette dont la partie brisée dépasse ¾ de sa taille. |
Morceau: |
Partie de crevette, au minimum ¼ de sa taille. |
Matière étrangère: |
Toute matière étrangère non nocive se trouvant dans le paquet. |
Uniformité du calibre: |
Choisir 10 crevettes parmi les plus grosses et 10 crevettes parmi les plus petites et diviser le poids le plus grand par le poids le plus petit pour obtenir un rapport de poids. |
Évaluation de la saveur et de l’odeur :
Pour évaluer l’odeur, tenir les crevettes près du nez. Si les résultats de l’évaluation de l’odeur du produit cru indiquent l’existence de toute odeur anormale, faire cuire l’échantillon pour vérifier la saveur et l’odeur.
Méthode de cuisson à la vapeur:
Mettre l’échantillon dans un sac de plastique et le placer sur une grille mécanique posée sur de l’eau en ébullition dans un récipient fermé. Cuire à la vapeur le produit empaqueté pendant 5 à 10 minutes.
Examen des défauts physiques:
Il faut examiner chaque crevette de l’échantillon pour déceler les défauts à l’aide de la liste des définitions des défauts.
BARÈME DES DÉDUCTIONS DE POINTS PAR ÉCHANTILLON
Type de produit |
Facteur classé |
Méthode de classement |
Déduction |
État congelé |
Déshydratation |
Jusqu’à 5 %
|
0
|
État décongelé |
Taches noires seulement sur la carapace |
Absence
|
0
|
Taches noires dans la chair |
Absence
|
0
| |
Brisé, endommagé et en morceaux |
Jusqu’à 1%
|
1
| |
Déshydratation |
Absence
|
0
| |
Déshydratation de la chair |
Absence
|
0
| |
Têtes et crevettes inacceptables |
Jusqu’à 1%
|
2
| |
Matières étrangères, non nocives |
1 morceau
|
1
| |
Uniformité du calibre |
Légèrement plus grande ou plus petite. Chaque surface de 3% ou fraction.
|
1 2 | |
Odeur |
Caractéristique.
|
0 6 12 21 | |
Décorticage et déveinage inappropriés |
Absence
|
0
| |
Fragments de carapace |
Jusqu’à 3%
|
0
| |
Après cuisson |
Texture |
Ferme, mais plus tendre et humide
|
0
|
Odeur |
Caractéristique
|
0
| |
B. CREVETTES PANÉES
FACTEUR DE QUALITÉ
Détermination de la qualité
On déterminera la qualité en examinant le produit à l’état congelé et après cuisson à l’aide du tableau des déductions de points.
100 à 85 Première qualité
84 à 75 Deuxième qualité
Barème des déductions de points par échantillon
Type de produit |
Facteur classe |
Méthode de classement |
Déduction | |
A l’état congelé |
Brisé |
Déchirure ou coupure > ¾ de la surface |
15 | |
Uniformité du calibre |
Plus de 1,0; pas plus de 1,35
|
0
| ||
Facilité de séparation |
Légère: Séparation à la main difficile. Chaque unité affectée Modérée: Séparée avec un couteau. Chaque unité affectée |
1 2 | ||
Après cuisson |
Tache noire dans la chair |
Absence
|
0
2 | |
Défauts d’enrobage |
Absence
|
0
2 | ||
Texture |
Chair de crevette |
Ferme, mais tendre et humide
|
0
| |
Enrobage |
Modérément sèche, vitreuse ou dure
|
5
| ||
APPENDICE X - PRESCRIPTIONS FACULTATIVES CONCERNANT LE PRODUIT FINI -CÉPHALOPODES
[À TERMINER]
APPENDICE XI
PRESCRIPTIONS FACULTATIVES CONCERNANT LE PRODUIT FINI – POISSON EN CONSERVE
Les définitions suivantes sont des recommandations à l’usage des acheteurs et des vendeurs de poisson en conserve, qui serviront à élaborer des spécifications concernant les produits finis. Ces spécifications sont facultatives et viennent s’ajouter aux prescriptions essentielles énoncées dans les différentes normes Codex sur les produits.
1. Poisson en conserve
Défauts |
Description recommandée des défauts |
a) Poids égoutté ou poids égoutté lavé |
Le poids égoutté du poisson (conditionné en liquide), ou le poids égoutté lavé de poisson (conditionné en sauce) ne doit pas être inférieur au pourcentage (m/m) suivant de la capacité en eau du récipient lorsque le milieu de couverture est l’un de ceux indiqués ci-après:
|
Eau exsudée |
Teneur en eau (exprimée en % du contenu net de la boîte). |
Séparation de la sauce |
Sauce séparée en phase solide et en phase liquide (sauf huile) |
b) Aspect |
Le poisson contenu dans les boîtes doit présenter l’aspect et la couleur caractéristique du genre traité et doit être conditionné de la manière indiquée. |
Poissons parés et tranches conditionnés dans divers milieux de couverture |
Découpage, parage et éviscération
|
Morceaux non caractéristiques
| |
Filets, fragments et flocons conditionnés dans divers milieux de couverture |
Découpage et parage
|
Peau (filets étiquetés sans peau) - Chaque pièce > 3 cm² | |
Membrane noire - Chaque pièce > 5 cm² | |
Morceaux non caractéristiques (uniquement pour les filets et les morceaux)
| |
Défaut de coloration, milieu de couverture |
Le milieu de couverture n’a pas une couleur ni une texture normale pour le type de paquet |
Remplissage du récipient |
Une boîte n’est pas entièrement remplie de poisson et le milieu de couverture n’est pas adapté au type du paquet. |
2. Conserves de sardines et de produits du type sardine
Défauts |
Description recommandée des défauts |
a) Aspect |
Le contenu d’une boîte se compose de poissons:
|
b) Eau exsudée (conditionnements à l’huile uniquement) |
Teneur en eau exprimée en % du contenu net de la boîte |
3. Thon et bonite en conserve
Aucun défaut potentiel n’a été décrit pour ces produits.
4. Saumon en conserve
Défauts |
Description recommandée des défauts |
a) Aspect
|
i) la boîte n’est pas bien remplie de poisson.
|
b) Arêtes |
Arête dure |
c) Couleur de la chair |
Poisson ayant l’aspect et la couleur ci-après: |
d) Meurtrissures et taches de sang |
Présence de meurtrissures ou de taches de sang exprimées en % du contenu net de la boîte. |
5. Chair de crabe en conserve
Défauts |
Description recommandée des défauts |
Aspect |
La boîte ouverte ne paraît pas bien remplie et le produit n’est pas disposé conformément au mode de présentation. |
6. Crevettes en conserve
Aucun défaut potentiel n’a été décrit pour ce produit.
.
APPENDICE XII
Code d’usages international recommandé pour le traitement et la manutention des denrées surgelées |
CAC/RCP 8-1976 |
Méthodes de contrôle de la température des denrées surgelées |
Addendum 1, 1978 à CAC/RCP 8-1976 |
Code d’usages international recommandé pour le poisson frais |
CAC/RCP 9-1976 |
Code d’usages international recommandé pour le poisson, les crustacés et les mollusques en conserve (appertisés) |
CAC/RCP 10-1976 |
Code d’usages international recommandé pour le poisson congelé |
CAC/RCP 16-1978 |
Code d’usages international recommandé pour les crevettes |
CAC/RCP 17-1978 |
Code d’usages international recommandé en matière d’hygiène pour les mollusques |
CAC/RCP 18-1978 |
Code d’usages international recommandé pour les homards, les langoustes et les espèces apparentées |
CAC/RCP 24- 1979 |
Code d’usages international recommandé pour le poisson fumé |
CAC/RCP 25-1979 |
Code d’usages international recommandé pour le poisson salé |
CAC/RCP 26-1979 |
Code d’usages international recommandé pour le poisson haché préparé par séparation mécanique |
CAC/RCP 27-1983 |
Code d’usages international recommandé pour les crabes |
CAC/RCP 28-1983 |
Norme pour les calmars surgelés |
CODEX STAN 191-1995 |
Norme pour le poisson salé et le poisson salé séché de la famille des Gadidées |
CODEX STAN 167-1989, Rév.1-1995 |
Norme pour le saumon en conserve |
CODEX STAN 3-1981, Rév. 1-1995 |
Norme pour le poisson en conserve |
CODEX STAN 36-1981, Rév.1-1995 |
Norme pour les crevettes en conserve |
CODEX STAN 37-1981, Rév. 1-1995 |
Norme pour les filets de poissons surgelés |
CODEX STAN 190-1995 |
Norme pour le thon et la bonite en conserve |
CODEX STAN 70-1981, Rév. 1-1995 |
Norme pour la chair de crabe en conserve |
CODEX STAN 90-1981, Rév. 1-1995 |
Norme pour les crevettes surgelées |
CODEX STAN 92-1981, Rév. 1-1995 |
Norme pour les sardines et produits du type sardines en conserve |
CODEX STAN 94-1981, Rév. 1-1995 |
Norme pour les langoustes, homards et cigales de mer surgelés |
CODEX STAN 95-1981, Rév. 1-1995 |
Norme pour le poisson en conserve |
CODEX STAN 119-1981, Rév. 1-1995 |
Norme pour les blocs surgelés de filets de poissons, de chair de poisson hachée et de mélanges de filets et de chair de poisson hachée |
CODEX STAN 165-1989, Rév. 1-1995 |
Norme pour les bâtonnets, les portions et les filets de poisson surgelés - panés ou enrobés de pâte à frire |
CODEX STAN 166-1989, Rév. 1-1995 |
Manuel d’hygiène des fruits de mer par P.C. Wood |
Publication offset de l’OMS N°31 (1976) |
Code d’usages international recommandé - Principes généraux d’hygiène alimentaire, y compris une Annexe sur le système HACCP et les directives pour son application: |
CAC/VOL.A-Ed.1 |
Directives Codex pour l’évaluation organoleptique en laboratoire du poisson et des mollusques et crustacés
|
CAC/GL 31-1999 OMS, 2e édition, 1993 |
1 Norme Codex pour le poisson fumé à froid préemballé (en cours d’élaboration)
2 On trouvera la liste des additifs pour les sulfites et les phosphates dans la Norme Codex pour les langoustes, homards et cigales de mer surgelés (Codex Stan 95-1981, Rév. 1-1995)
3 Les prescriptions facultatives concernant le produit fini pour le poisson surgelé, non éviscéré ou éviscéré, ont été élaborées sur la base de la Norme Codex pour les saumons du Pacifique éviscérés surgelés (Codex Stan 36 1981).
4 Dans le cas des poissons plats sans peau, les petits fragments de peau blanche ne sont pas considérés comme des défauts, à condition que la peau ne représente pas plus de 10 pour cent de la surface des filets dans l’échantillon.